过渡元素(一) 钛分族 钒分族 铬分族 锰分族 本章要求
过渡元素(一) 通 性 钛 分 族 作 业 本 章 要 求 钒 分 族 锰 分 族 铬 分 族
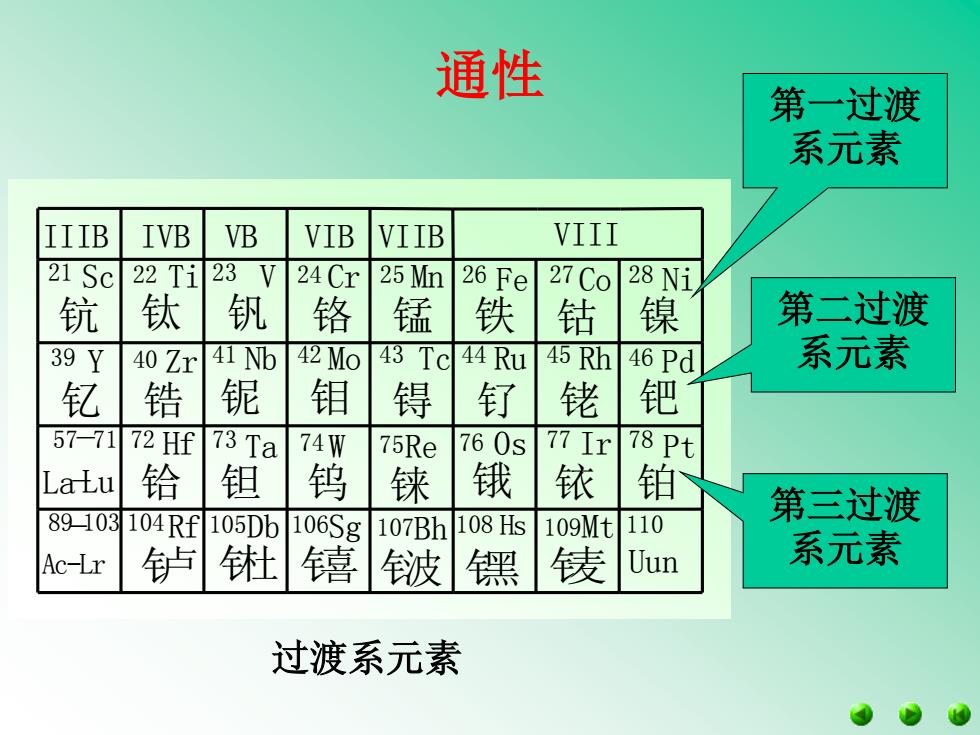
通性 第一过渡 系元素 IIIB IVB VB VIB VIIB VIII 21 Sc 22T1 23V 24 Cr 25 Mn 26 Fe 27 Co 28 Ni 钪 钛 钒 铬 锰 铁 钴 镍 第二过渡 39Y 40 Zr 41 Nb 42 Mo 43 Tc44 Ru 45 Rh 46 Pd 系元素 钇 锆 铌 钼 锝 钉 铑 钯 57-7172Hf 73 Ta 74 75Re 760S 77 78 Pt LaLu 铪 钽 钨 铼 锇 铱 铂 89▣103 104Rf105Db 第三过渡 106Sg 107Bh 108Hs 109Mt 110 Ac-Lr 轳 波镙 债 Uun 系元素 过渡系元素
过渡系元素 通性 钅卢 钅杜 钅喜 钅波 钅黑 钅麦 铌 钽 钇 锆 铪 钼 钨 锝 铼 钌 铑 钯 锇 铱 铂 钪 钛 钒 铬 锰 铁 钴 镍 Zr Nb Mo Tc Ru Rh Pd Hf Ta W Re Os Ir Pt IIIB IVB VB VIB VIIB VIII Rf Db Sg Bh Hs Mt Ac-Lr Uun Sc Ti V Cr Mn Fe Co Ni Y La-Lu 21 22 23 24 25 26 27 28 39 40 41 42 43 44 45 46 72 73 74 75 76 77 78 104 105 106 107 108 109 110 57 89 -103 -71 第一过渡 系元素 第二过渡 系元素 第三过渡 系元素

通性 一、共性 1、都有较大的硬度、熔点和沸点。它们的导电性、 导热性好,相互间可形成合金。 2、大多数溶于酸,只是有些“贵”金属电极电势 较大,难与普通的酸反应。 3、除B族外,都有多种氧化态,水合离子和酸 根离子常呈现一定颜色。 4、由于d电子不满,化合物通常是顺磁性化合物。 5、原子半径从左到右逐渐减小
通性 一、共性 1、都有较大的硬度、熔点和沸点。它们的导电性、 导热性好,相互间可形成合金。 2、大多数溶于酸,只是有些“贵”金属电极电势 较大,难与普通的酸反应。 3、除IIIB族外,都有多种氧化态,水合离子和酸 根离子常呈现一定颜色。 4、由于d电子不满,化合物通常是顺磁性化合物。 5、原子半径从左到右逐渐减小

通性 二、电子构型 除Pd外,它们都有未充满的d轨道,最外层也仅 有1-2个电子,过渡元素通常指价电子层结构即: (n-1)dl-9nsl-2。 三、氧化态 它们的(n-1)d和ns轨道能级的能量相差很小,d电 子也可部分或全部作为价电子参加成键。一般由+2价 直到与族数相同的氧化态(VⅡ例外)。 四、单质的化学性质 B族是它们中最活泼的金属,性质与碱土金属 接近。同族元素的活泼性从上到下依次减弱
通性 二、电子构型 除Pd外,它们都有未充满的d轨道,最外层也仅 有1-2个电子,过渡元素通常指价电子层结构即: (n-1)d1-9ns1-2 。 三、氧化态 它们的(n-1)d和ns轨道能级的能量相差很小,d电 子也可部分或全部作为价电子参加成键。一般由+2价 直到与族数相同的氧化态(VIII例外)。 四、单质的化学性质 IIIB族是它们中最活泼的金属,性质与碱土金属 接近。同族元素的活泼性从上到下依次减弱

通性 五、氧化物及其水合物的酸碱性 同种元素,不同氧化态的氧化物,其酸碱性随氧 化数的降低酸性减弱,碱性增强。 Mn207 MnO; MnO2 Mn203 MnO 强酸性 酸性 两性 弱碱性 碱性 这是由于其水合物中非羟基氧的数目减少。 同一过渡系内各元素的最高氧化态的氧化物及水 合物,从左到右碱性减弱,酸性增强。 Sc2O3 TiO CrO; Mn207 强碱 两性 酸性 强酸 同族元素,自上而下各元素相同氧化态的氧化物 及其水合物,通常是酸性减弱,碱性增强。 H,CrO H,MoO H,WO 中强酸 弱酸 两性偏酸性
通性 五、氧化物及其水合物的酸碱性 同种元素,不同氧化态的氧化物,其酸碱性随氧 化数的降低酸性减弱,碱性增强。 Mn2O7 MnO3 MnO2 Mn2O3 MnO 强酸性 酸性 两性 弱碱性 碱性 这是由于其水合物中非羟基氧的数目减少。 同一过渡系内各元素的最高氧化态的氧化物及水 合物,从左到右碱性减弱,酸性增强。 Sc2O3 TiO2 CrO3 Mn2O7 强碱 两性 酸性 强酸 同族元素,自上而下各元素相同氧化态的氧化物 及其水合物,通常是酸性减弱,碱性增强。 H2CrO4 H2MoO4 H2WO4 中强酸 弱酸 两性偏酸性