
爸中国斜草技术大车 第1章 气体、液体和溶液的性质 Chapter 1 The behaviors of Gas,Liquid Solution
第1章 气体、液体和溶液的性质 Chapter 1 The behaviors of Gas, Liquid & Solution

本章重点 >常见的物质存在状态: ·气体(gas):性质较简单,研究最深入 √状态参量:p,V,T,n √分压定律、分体积定律、气体扩散定律 ·液体(liquid):性质较复杂 √液体的蒸气压、沸点和凝固点 √溶液的性质:稀溶液的依数性,胶体 ·固体(solid):(后续章节) >不同物质存在状态的产生原因: ·分子间作用力不同 ·温度和压力等条件不同 2
本章重点 ¾常见的物质存在状态: • 气体 (gas):性质较简单,研究最深入 9状态参量:p, V, T, n 9分压定律、分体积定律、气体扩散定律 • 液体 (liquid):性质较复杂 9液体的蒸气压、沸点和凝固点 9溶液的性质:稀溶液的依数性,胶体 • 固体 (solid):(后续章节) ¾不同物质存在状态的产生原因: • 分子间作用力不同 • 温度和压力等条件不同 2

§1.1气体的性质 一、理想气体(Ideal gas):简单气体模型 >什么样的气体称为理想气体? ·气体分子间无相互作用(除碰撞时) ·气体分子为无几何尺寸的质点 >理想气体在实际中存在吗? ·抽象的概念,实际上不存在 ·反映了实际气体在一定条件下的最一般性质 >实际气体在什么情况下可被视为理想气体? ·温度高且压力无限低p→0) ·分子间距大,相互作用力→0 ·分子所占体积可忽略 3
§1.1 气体的性质 一、理想气体 (Ideal gas):简单气体模型 ¾ 什么样的气体称为理想气体? • 气体分子间无相互作用(除碰撞时) • 气体分子为无几何尺寸的质点 ¾ 理想气体在实际中存在吗? • 抽象的概念,实际上不存在 • 反映了实际气体在一定条件下的最一般性质 ¾ 实际气体在什么情况下可被视为理想气体? • 温度高且压力无限低 (po0) • 分子间距大,相互作用力o0 • 分子所占体积可忽略 3
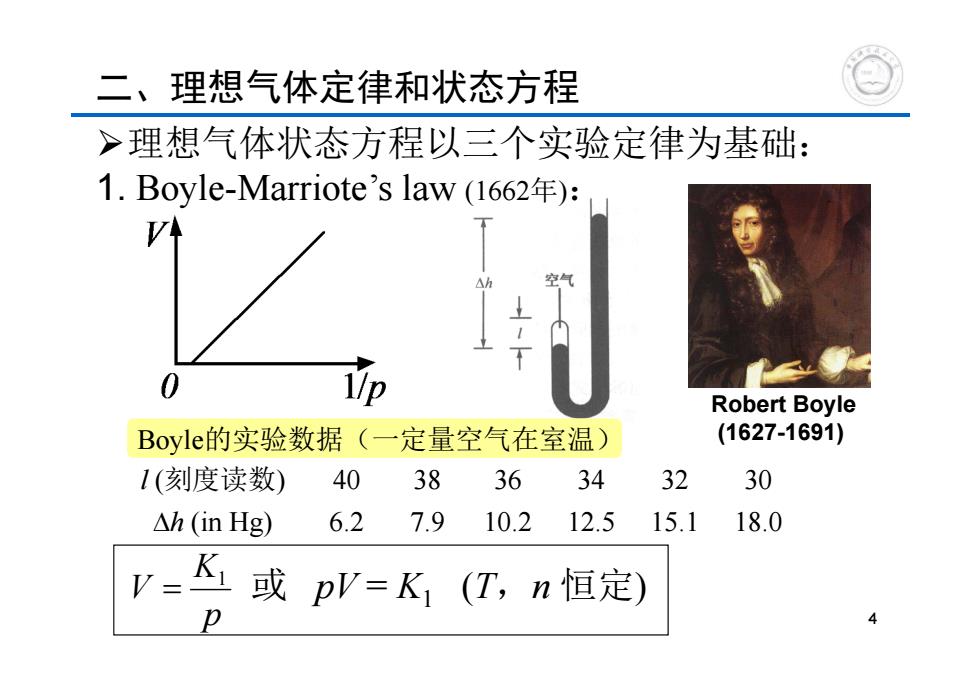
二、理想气体定律和状态方程 >理想气体状态方程以三个实验定律为基础: 1.Boyle-Marriote'slaw(I662年): V 0 b Robert Boyle Boyle的实验数据(一定量空气在室温) (1627-1691) 1(刻度读数) 40 38 36 34 32 30 △h(inHg) 6.2 7.9 10.2 12.5 15.1 18.0 V-K 或pV=K1(T,n恒定) p
4 二、理想气体定律和状态方程 ¾理想气体状态方程以三个实验定律为基础: 1. Boyle-Marriote’s law (1662 年 ) : Robert Boyle (1627-1691) l (刻度读数 ) 40 38 36 34 32 30 ' h (in Hg) 6.2 7.9 10.2 12.5 15.1 18.0 Boyle的实验数据(一定量空气在室温) p K V 1 或 pV = K 1 ( T ,n 恒定 )

2.Charles-Gay-Lussac'slaw(1802年): rKT或K:,恒定) T(Kelvin温标,K)=t(Celsius温标,C)+273.15 Jacques Charles (1746-1823) 3.Avogadro's hypothesis(1811年): V=K,n(T,p恒定) 同温同压下,同体积各气体有相同粒子数 ·物质的量:摩尔mol,NA=6.022×1023 Amedeo Avogadro (1776-1856)
5 2. Charles-Gay-Lussac’s law (1802年) : T (Kelvin温标, K) = t (Celsius温标, qC) + 273.15 3. Avogadro’s hypothesis (1811年) : • 同温同压下,同体积各气体有相同粒子数 • 物质的量:摩尔mol,NA = 6.022 u 1023 Jacques Charles (1746-1823) Amedeo Avogadro (1776-1856) V K3n (T,p 恒定) K2 TV V = K 2T 或 (p,n恒定)