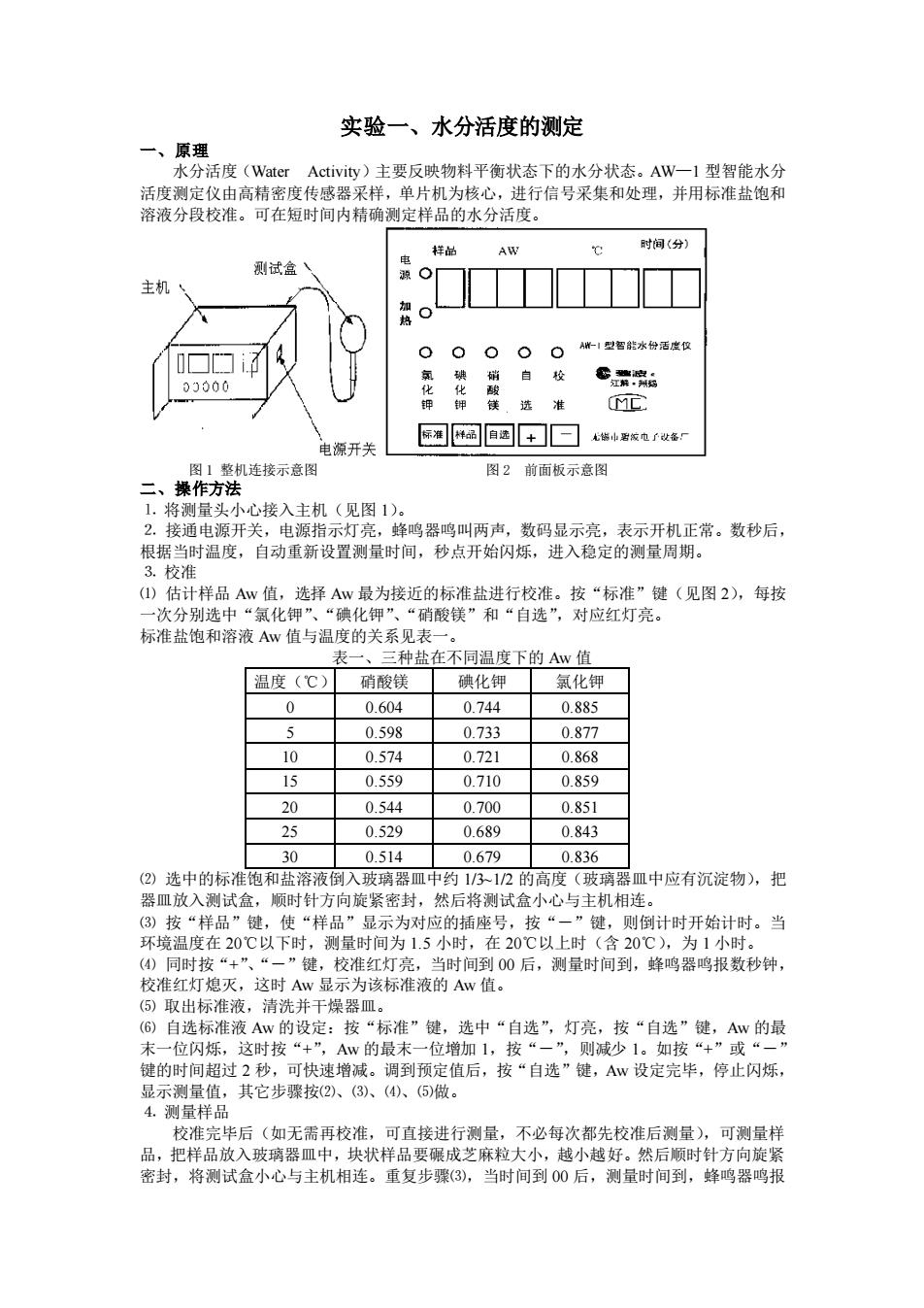
实验一、水分活度的测定 一、原理 水分活度(Water Activity)主要反映物料平衡状态下的水分状态。AW—1 型智能水分 活度测定仪由高精密度传感器采样,单片机为核心,进行信号采集和处理,并用标准盐饱和 溶液分段校准。可在短时间内精确测定样品的水分活度。 图 1 整机连接示意图 图 2 前面板示意图 二、操作方法 ⒈ 将测量头小心接入主机(见图 1)。 ⒉ 接通电源开关,电源指示灯亮,蜂鸣器鸣叫两声,数码显示亮,表示开机正常。数秒后, 根据当时温度,自动重新设置测量时间,秒点开始闪烁,进入稳定的测量周期。 ⒊ 校准 ⑴ 估计样品 Aw 值,选择 Aw 最为接近的标准盐进行校准。按“标准”键(见图 2),每按 一次分别选中“氯化钾”、“碘化钾”、“硝酸镁”和“自选”,对应红灯亮。 标准盐饱和溶液 Aw 值与温度的关系见表一。 表一、三种盐在不同温度下的 Aw 值 温度(℃) 硝酸镁 碘化钾 氯化钾 0 0.604 0.744 0.885 5 0.598 0.733 0.877 10 0.574 0.721 0.868 15 0.559 0.710 0.859 20 0.544 0.700 0.851 25 0.529 0.689 0.843 30 0.514 0.679 0.836 ⑵ 选中的标准饱和盐溶液倒入玻璃器皿中约 1/3~1/2 的高度(玻璃器皿中应有沉淀物),把 器皿放入测试盒,顺时针方向旋紧密封,然后将测试盒小心与主机相连。 ⑶ 按“样品”键,使“样品”显示为对应的插座号,按“-”键,则倒计时开始计时。当 环境温度在 20℃以下时,测量时间为 1.5 小时,在 20℃以上时(含 20℃),为 1 小时。 ⑷ 同时按“+”、“-”键,校准红灯亮,当时间到 00 后,测量时间到,蜂鸣器鸣报数秒钟, 校准红灯熄灭,这时 Aw 显示为该标准液的 Aw 值。 ⑸ 取出标准液,清洗并干燥器皿。 ⑹ 自选标准液 Aw 的设定:按“标准”键,选中“自选”,灯亮,按“自选”键,Aw 的最 末一位闪烁,这时按“+”,Aw 的最末一位增加 1,按“-”,则减少 1。如按“+”或“-” 键的时间超过 2 秒,可快速增减。调到预定值后,按“自选”键,Aw 设定完毕,停止闪烁, 显示测量值,其它步骤按⑵、⑶、⑷、⑸做。 ⒋ 测量样品 校准完毕后(如无需再校准,可直接进行测量,不必每次都先校准后测量),可测量样 品,把样品放入玻璃器皿中,块状样品要碾成芝麻粒大小,越小越好。然后顺时针方向旋紧 密封,将测试盒小心与主机相连。重复步骤⑶,当时间到 00 后,测量时间到,蜂鸣器鸣报
实验一、水分活度的测定 一、原理 水分活度(Water Activity)主要反映物料平衡状态下的水分状态。AW—1 型智能水分 活度测定仪由高精密度传感器采样,单片机为核心,进行信号采集和处理,并用标准盐饱和 溶液分段校准。可在短时间内精确测定样品的水分活度。 图 1 整机连接示意图 图 2 前面板示意图 二、操作方法 ⒈ 将测量头小心接入主机(见图 1)。 ⒉ 接通电源开关,电源指示灯亮,蜂鸣器鸣叫两声,数码显示亮,表示开机正常。数秒后, 根据当时温度,自动重新设置测量时间,秒点开始闪烁,进入稳定的测量周期。 ⒊ 校准 ⑴ 估计样品 Aw 值,选择 Aw 最为接近的标准盐进行校准。按“标准”键(见图 2),每按 一次分别选中“氯化钾”、“碘化钾”、“硝酸镁”和“自选”,对应红灯亮。 标准盐饱和溶液 Aw 值与温度的关系见表一。 表一、三种盐在不同温度下的 Aw 值 温度(℃) 硝酸镁 碘化钾 氯化钾 0 0.604 0.744 0.885 5 0.598 0.733 0.877 10 0.574 0.721 0.868 15 0.559 0.710 0.859 20 0.544 0.700 0.851 25 0.529 0.689 0.843 30 0.514 0.679 0.836 ⑵ 选中的标准饱和盐溶液倒入玻璃器皿中约 1/3~1/2 的高度(玻璃器皿中应有沉淀物),把 器皿放入测试盒,顺时针方向旋紧密封,然后将测试盒小心与主机相连。 ⑶ 按“样品”键,使“样品”显示为对应的插座号,按“-”键,则倒计时开始计时。当 环境温度在 20℃以下时,测量时间为 1.5 小时,在 20℃以上时(含 20℃),为 1 小时。 ⑷ 同时按“+”、“-”键,校准红灯亮,当时间到 00 后,测量时间到,蜂鸣器鸣报数秒钟, 校准红灯熄灭,这时 Aw 显示为该标准液的 Aw 值。 ⑸ 取出标准液,清洗并干燥器皿。 ⑹ 自选标准液 Aw 的设定:按“标准”键,选中“自选”,灯亮,按“自选”键,Aw 的最 末一位闪烁,这时按“+”,Aw 的最末一位增加 1,按“-”,则减少 1。如按“+”或“-” 键的时间超过 2 秒,可快速增减。调到预定值后,按“自选”键,Aw 设定完毕,停止闪烁, 显示测量值,其它步骤按⑵、⑶、⑷、⑸做。 ⒋ 测量样品 校准完毕后(如无需再校准,可直接进行测量,不必每次都先校准后测量),可测量样 品,把样品放入玻璃器皿中,块状样品要碾成芝麻粒大小,越小越好。然后顺时针方向旋紧 密封,将测试盒小心与主机相连。重复步骤⑶,当时间到 00 后,测量时间到,蜂鸣器鸣报

数秒钟,这时 Aw 显示为该样品的 Aw 值。 ⒌ 从玻璃器皿中取出样品,清洗并干燥器皿。 三、使用注意事项 ⒈ 测量头(测试盒内器件)为贵重的精密器件,需轻拿轻放,严禁直接接触样品和水,不 能用手触摸。如不小心接触了液体,需自动蒸发干后方能使用。 ⒉ 为提高测量精度,测试盒及玻璃器皿应是干燥和清洁的,每次用毕后应清洗干燥处理。 测量 Aw>0.95 样品时,测量 Aw 结束后应立即把测量头放在通风处,经 10 分钟后方能重新 测量。 ⒊ 配制饱和盐溶液时,应用蒸馏水稀释,放置几天后有固体沉淀物,才能使用。不必每次 测量之前校准,一般在隔几天或要求测量结果特别正确时进行校准
数秒钟,这时 Aw 显示为该样品的 Aw 值。 ⒌ 从玻璃器皿中取出样品,清洗并干燥器皿。 三、使用注意事项 ⒈ 测量头(测试盒内器件)为贵重的精密器件,需轻拿轻放,严禁直接接触样品和水,不 能用手触摸。如不小心接触了液体,需自动蒸发干后方能使用。 ⒉ 为提高测量精度,测试盒及玻璃器皿应是干燥和清洁的,每次用毕后应清洗干燥处理。 测量 Aw>0.95 样品时,测量 Aw 结束后应立即把测量头放在通风处,经 10 分钟后方能重新 测量。 ⒊ 配制饱和盐溶液时,应用蒸馏水稀释,放置几天后有固体沉淀物,才能使用。不必每次 测量之前校准,一般在隔几天或要求测量结果特别正确时进行校准

实验二、总糖的测定 一、原理 样品中原有的和水解后产生的转化糖都具有还原性质,在碱性溶液中能将铁氰化钾还 原。根据铁氰化钾的浓度和检液滴定量可以计算出样品中糖的含量。 反应式如下: C6H12O6+6K3Fe(CN)6+6KOH → (CHOH)4·(COOH)2+6K4Fe(CN)6+4H2O 当滴定到终点时,稍微过量的转化糖立即将次甲基蓝还原为无色的隐色体,此时颜色消 失。反应如下: 二、试剂与器材 ⒈ 1%的次甲基蓝指示剂。 ⒉ 盐酸:分析纯。 ⒊ 20%和 30%氢氧化钠溶液。 ⒋ 1%铁氰化钾溶液:置棕色瓶中保存。每次使用前按下述方法标定铁氰化钾的浓度。 准确称取经105℃烘干并冷却之后的蔗糖1.000g,用少量水溶解并移入500ml容量瓶中, 用水稀释至刻度,摇匀。取出此液 50ml 于 100ml 容量瓶中,加盐酸 5ml 摇匀,置 65~70℃ 水浴上加温 30min,取出,迅速冷却至室温。用 30%氢氧化钠溶液中和,加水至刻度,摇匀, 倒入滴定管中。 吸取已配制好的铁氰化钾溶液 5ml 于 150ml 三角瓶中,加入 2.5ml10%氢氧化钠溶液、 12.5ml 水和洁净的玻璃珠数个,于石棉网上加热至沸腾,保持 1min。然后加入次甲基蓝指 示剂 1 滴,立即以糖液滴定至蓝色消失为止,记录用量。正式滴定时,先加入比预实验少 0.5ml 的糖液,煮沸 1min,加入次甲基蓝指示剂 1 滴,再用糖液滴定至无色。 按下述公式计算铁氰化钾的浓度: 式中 C:相当于 5ml 铁氰化钾溶液的转化糖的重量(g); V:滴定时消耗糖液的体积(ml); W:称取的蔗糖重量(g); 0.95:换算系数(1g 蔗糖可转化为 0.95g 转化糖)。 主要器材:滴定管,容量瓶、三角瓶。 三、操作步骤 称取样品 5~10g(视含糖量多少而增减),用 200ml 左右的水洗入 250ml 容量瓶内(样 品中如含有较多的蛋白质、色素、胶体等可逐渐加入 20%醋酸铅溶液 10~15ml,至沉淀完全 为止。并加入 10~15ml10%磷酸二氢钠溶液,至不再产生沉淀为止)。加水至刻度,摇匀过 滤。 吸取滤液 50ml 于 100ml 容量瓶中,按上述铁氰化钾标定方法进行转化、中和及滴定(以 样液代替糖液,其余操作相同)。 按下述公式计算总糖含量: 式中 A:相当于 5ml 铁氰化钾溶液的转化糖的重量(g); V:滴定试样液消耗体积(ml)。 四、注意事项 ⒈ 当滴定到达终点时,过量的转化糖将指示剂次甲基蓝还原为无色的隐色体。这种隐色体 容易受空气中的氧所氧化,很快又变为次甲基蓝而显色。 ⒉ 整个加温过程应在低温电炉上操作,这样重现性好、准确、误差小。滴定要迅速,否则
实验二、总糖的测定 一、原理 样品中原有的和水解后产生的转化糖都具有还原性质,在碱性溶液中能将铁氰化钾还 原。根据铁氰化钾的浓度和检液滴定量可以计算出样品中糖的含量。 反应式如下: C6H12O6+6K3Fe(CN)6+6KOH → (CHOH)4·(COOH)2+6K4Fe(CN)6+4H2O 当滴定到终点时,稍微过量的转化糖立即将次甲基蓝还原为无色的隐色体,此时颜色消 失。反应如下: 二、试剂与器材 ⒈ 1%的次甲基蓝指示剂。 ⒉ 盐酸:分析纯。 ⒊ 20%和 30%氢氧化钠溶液。 ⒋ 1%铁氰化钾溶液:置棕色瓶中保存。每次使用前按下述方法标定铁氰化钾的浓度。 准确称取经105℃烘干并冷却之后的蔗糖1.000g,用少量水溶解并移入500ml容量瓶中, 用水稀释至刻度,摇匀。取出此液 50ml 于 100ml 容量瓶中,加盐酸 5ml 摇匀,置 65~70℃ 水浴上加温 30min,取出,迅速冷却至室温。用 30%氢氧化钠溶液中和,加水至刻度,摇匀, 倒入滴定管中。 吸取已配制好的铁氰化钾溶液 5ml 于 150ml 三角瓶中,加入 2.5ml10%氢氧化钠溶液、 12.5ml 水和洁净的玻璃珠数个,于石棉网上加热至沸腾,保持 1min。然后加入次甲基蓝指 示剂 1 滴,立即以糖液滴定至蓝色消失为止,记录用量。正式滴定时,先加入比预实验少 0.5ml 的糖液,煮沸 1min,加入次甲基蓝指示剂 1 滴,再用糖液滴定至无色。 按下述公式计算铁氰化钾的浓度: 式中 C:相当于 5ml 铁氰化钾溶液的转化糖的重量(g); V:滴定时消耗糖液的体积(ml); W:称取的蔗糖重量(g); 0.95:换算系数(1g 蔗糖可转化为 0.95g 转化糖)。 主要器材:滴定管,容量瓶、三角瓶。 三、操作步骤 称取样品 5~10g(视含糖量多少而增减),用 200ml 左右的水洗入 250ml 容量瓶内(样 品中如含有较多的蛋白质、色素、胶体等可逐渐加入 20%醋酸铅溶液 10~15ml,至沉淀完全 为止。并加入 10~15ml10%磷酸二氢钠溶液,至不再产生沉淀为止)。加水至刻度,摇匀过 滤。 吸取滤液 50ml 于 100ml 容量瓶中,按上述铁氰化钾标定方法进行转化、中和及滴定(以 样液代替糖液,其余操作相同)。 按下述公式计算总糖含量: 式中 A:相当于 5ml 铁氰化钾溶液的转化糖的重量(g); V:滴定试样液消耗体积(ml)。 四、注意事项 ⒈ 当滴定到达终点时,过量的转化糖将指示剂次甲基蓝还原为无色的隐色体。这种隐色体 容易受空气中的氧所氧化,很快又变为次甲基蓝而显色。 ⒉ 整个加温过程应在低温电炉上操作,这样重现性好、准确、误差小。滴定要迅速,否则

滴定终点不明显
滴定终点不明显

实验三、蜂蜜中果糖含量的测定 一、原理 果糖是具有酮基的还原糖(酮糖)。测定时可用直接滴定法测定样品中总的还原糖含量, 然后用碘量法测定样品中醛糖的含量,总的还原糖含量减去醛糖的含量即是果糖的含量。 二 、蜂蜜中总还原糖含量的测定(直接滴定法) ⒈ 原理 将一定量的硫酸铜液(菲林试剂甲)和碱性酒石酸钾钠液(菲林试剂乙)等量混合,硫 酸铜液与氢氧化钠作用,生成兰色氢氧化铜沉淀,氢氧化铜立即与酒石酸钾钠作用,生成可 溶性酒石酸钾钠铜络合物。在加热条件下(煮沸),以次甲基蓝作指示剂,用处理好的样品 液滴定,样品液中还原糖与酒石酸钾钠铜反应,生成红色的氧化亚铜沉淀,达到终点时,稍 过量的还原糖把次甲基蓝还原,溶液由蓝色变为无色,即为终点。根据样液消耗量可计算还 原糖含量,反应过程如下: CuSO4+2NaOH=2Cu(OH)2↓ ⒉ 试 剂 ⑴ 菲林试剂甲:称取硫酸铜 34.63g,加蒸馏水溶解后,置于 500ml 容量瓶中,加水稀释至 刻度,混匀。 ⑵ 菲林试剂乙:称取酒石酸钾钠 173g 及氢氧化钠 50g,加蒸馏水溶解后置于 500ml 容量瓶 中,加水稀释至刻度,混匀,过滤后使用。 ⑶ 标准还原糖液(2mg/ml):称取纯蔗糖 9.5g,溶于 50ml 水中,加 6mol/L 盐酸 5ml,在 20~25℃室温下静置 5d(或煮沸 15min),使蔗糖转化,冷却后移入 1000ml 容量瓶中,加 水稀释至刻度,再从稀释了的糖液中吸取 100ml 放入 500ml 容量瓶中,加 1%酚酞 2~3 滴, 以 6mol/L 氢氧化钠溶液中和后加水稀释至刻度,即为转化糖溶液。此液 1ml 含转化糖 2mg。 ⑷ 1%次甲基蓝溶液。 ⒊ 操作步骤 ⑴ 菲林试剂的标定。准确吸取配好的菲林试剂甲、乙各 5ml 混于三角瓶中,加次甲基蓝指 示剂 2 滴,加热至沸,由滴定管中滴入糖液,至蓝色完全褪尽,溶液呈清亮为止,根据滴定 所用转化糖的体积校正菲林试剂 10ml 相当的转化糖的克数。 ⑵ 称样品 10g ,小心转入 100ml 容量瓶中,蒸馏水定容,吸 10ml 样品液放入 250ml 烧杯 中,加水 50ml,加 2.5ml 浓盐酸(12mol/L)在沸水中煮 40min,取出冷却,此时样品中的 蔗糖水解成还原糖,然后加 1 滴 1%的酚酞,加 6mol/L 氢氧化钠中和至微红色,转移至 100ml 容量瓶中,定容,摇匀。准确取菲林试剂甲、乙各 5ml,放入三角瓶中,加次甲基蓝指示剂 2 滴,加热至沸,用样品溶液进行滴定,直至样品转化液将菲林试剂滴定至沸腾的泡沫为清 亮,同时有红棕色沉淀出现为终点。记录样品液的体积,再重复一次。 ⒋ 计算 还原糖的含量(%)= 式中 A:10ml 菲林试剂所相当的还原糖的质量(g); V:滴定时所用样品液的体积(ml); m:所称样品的质量(g)。 ⒌ 注意事项 因次甲基蓝在碱性溶液中被过量的还原糖还原成无色,在常温下又极易被大气中的氧氧 化成蓝色,影响终点的确定,故滴定时瓶中须保持沸腾状态,同时滴定时要快速,尽可能在
实验三、蜂蜜中果糖含量的测定 一、原理 果糖是具有酮基的还原糖(酮糖)。测定时可用直接滴定法测定样品中总的还原糖含量, 然后用碘量法测定样品中醛糖的含量,总的还原糖含量减去醛糖的含量即是果糖的含量。 二 、蜂蜜中总还原糖含量的测定(直接滴定法) ⒈ 原理 将一定量的硫酸铜液(菲林试剂甲)和碱性酒石酸钾钠液(菲林试剂乙)等量混合,硫 酸铜液与氢氧化钠作用,生成兰色氢氧化铜沉淀,氢氧化铜立即与酒石酸钾钠作用,生成可 溶性酒石酸钾钠铜络合物。在加热条件下(煮沸),以次甲基蓝作指示剂,用处理好的样品 液滴定,样品液中还原糖与酒石酸钾钠铜反应,生成红色的氧化亚铜沉淀,达到终点时,稍 过量的还原糖把次甲基蓝还原,溶液由蓝色变为无色,即为终点。根据样液消耗量可计算还 原糖含量,反应过程如下: CuSO4+2NaOH=2Cu(OH)2↓ ⒉ 试 剂 ⑴ 菲林试剂甲:称取硫酸铜 34.63g,加蒸馏水溶解后,置于 500ml 容量瓶中,加水稀释至 刻度,混匀。 ⑵ 菲林试剂乙:称取酒石酸钾钠 173g 及氢氧化钠 50g,加蒸馏水溶解后置于 500ml 容量瓶 中,加水稀释至刻度,混匀,过滤后使用。 ⑶ 标准还原糖液(2mg/ml):称取纯蔗糖 9.5g,溶于 50ml 水中,加 6mol/L 盐酸 5ml,在 20~25℃室温下静置 5d(或煮沸 15min),使蔗糖转化,冷却后移入 1000ml 容量瓶中,加 水稀释至刻度,再从稀释了的糖液中吸取 100ml 放入 500ml 容量瓶中,加 1%酚酞 2~3 滴, 以 6mol/L 氢氧化钠溶液中和后加水稀释至刻度,即为转化糖溶液。此液 1ml 含转化糖 2mg。 ⑷ 1%次甲基蓝溶液。 ⒊ 操作步骤 ⑴ 菲林试剂的标定。准确吸取配好的菲林试剂甲、乙各 5ml 混于三角瓶中,加次甲基蓝指 示剂 2 滴,加热至沸,由滴定管中滴入糖液,至蓝色完全褪尽,溶液呈清亮为止,根据滴定 所用转化糖的体积校正菲林试剂 10ml 相当的转化糖的克数。 ⑵ 称样品 10g ,小心转入 100ml 容量瓶中,蒸馏水定容,吸 10ml 样品液放入 250ml 烧杯 中,加水 50ml,加 2.5ml 浓盐酸(12mol/L)在沸水中煮 40min,取出冷却,此时样品中的 蔗糖水解成还原糖,然后加 1 滴 1%的酚酞,加 6mol/L 氢氧化钠中和至微红色,转移至 100ml 容量瓶中,定容,摇匀。准确取菲林试剂甲、乙各 5ml,放入三角瓶中,加次甲基蓝指示剂 2 滴,加热至沸,用样品溶液进行滴定,直至样品转化液将菲林试剂滴定至沸腾的泡沫为清 亮,同时有红棕色沉淀出现为终点。记录样品液的体积,再重复一次。 ⒋ 计算 还原糖的含量(%)= 式中 A:10ml 菲林试剂所相当的还原糖的质量(g); V:滴定时所用样品液的体积(ml); m:所称样品的质量(g)。 ⒌ 注意事项 因次甲基蓝在碱性溶液中被过量的还原糖还原成无色,在常温下又极易被大气中的氧氧 化成蓝色,影响终点的确定,故滴定时瓶中须保持沸腾状态,同时滴定时要快速,尽可能在