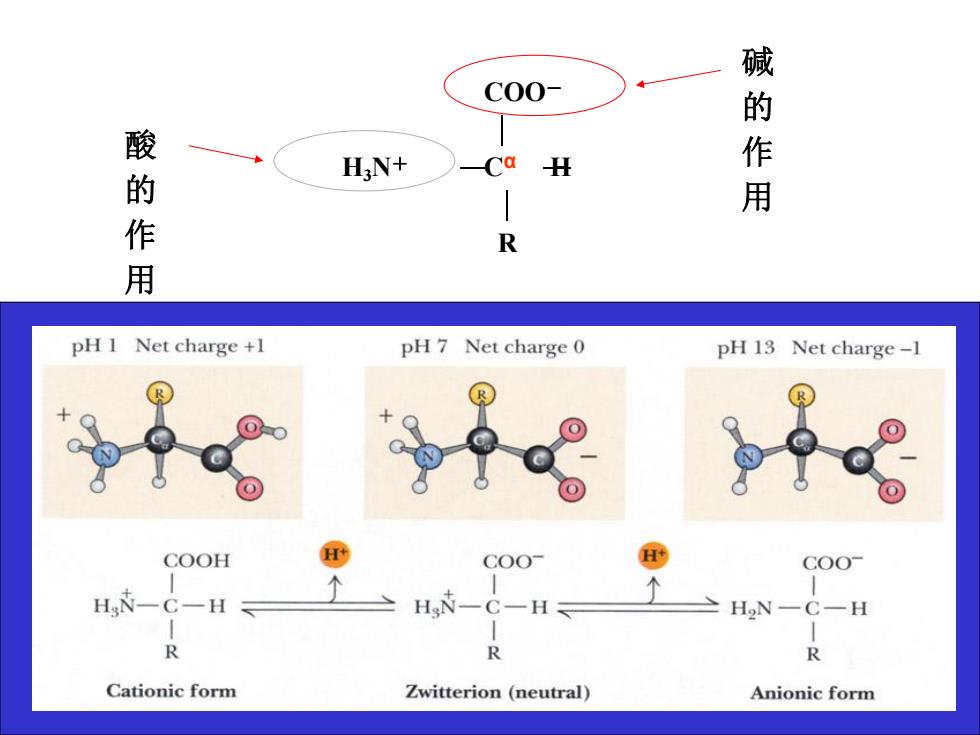
C00- 酸 H:N+ H 作 的 用 作 R 用 pH 1 Net charge +1 pH 7 Net charge 0 pH 13 Net charge-1 (R COOH COO COO 个 个 HN-C-H HN-C一H H2N-C-H R 1 Cationic form Zwitterion (neutral) Anionic form
11 COO- Cα H R H3N+ 碱的作用 酸的作用

甘氨酸的滴定(解离)曲线 Gly+ Glyo Gly- COOH COO COO HsN+- CH HsN+- CH2 H2N-CH2 14 12 10 D人 PH 8 6 Isoelectric point 4 PK 0 1.0 1.0 Equivalents of H+ Equivalents of OH ·分步解离:K [A][H+] [A-][H+] K2= [A+] [AO] KI= [Ht] pK=pH K2= [H+] pK2=H
12 甘氨酸的滴定(解离)曲线 • 分步解离: K1= [A 0][H +] [A +] [A -][H +] K2 = [A 0] K1= [H +] pK1= pH K2= [H +] pK2= pH

Handerson-Hasselbalch公式 pH=pKa+lg([A-]/[HA])=pKa+lg([碱]/[酸]) ·可计算出在任一pH条件下一种氨基酸的各种离子的比例。 ·氨基酸的带电状况与溶液的pH值有关。 ·表:氨基酸的酸碱化学133页 pK:基团一半解离时的pH。 [质子受体] pH pKa 1g [质子供体] 13
13 Handerson-Hasselbalch公式 pH = pKa + lg( [A -]/ [HA] )= pKa + lg( [碱]/[酸] ) • 可计算出在任一pH条件下一种氨基酸的各种离子的比例。 • 氨基酸的带电状况与溶液的pH值有关。 • 表:氨基酸的酸碱化学 133页 • pK:基团一半解离时的pH。 pH = pKa + lg [质子供体] [质子受体]
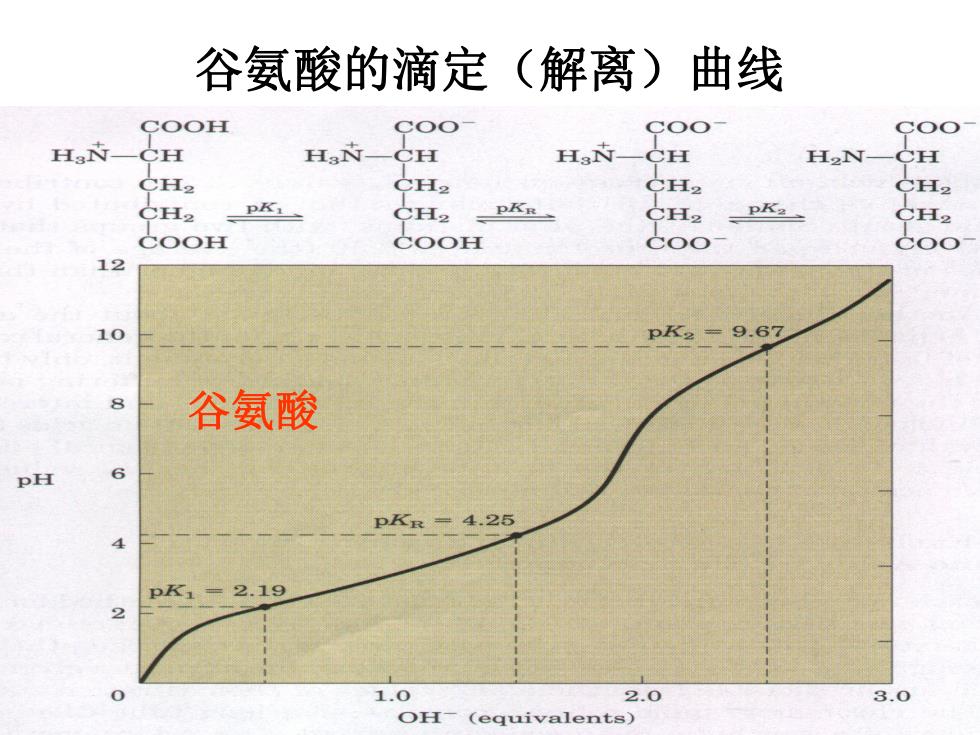
谷氨酸的滴定(解离) 曲线 COOH ●0O ●OO Ha古 CH Ha古 CH HsN- CH H2N CH CH2 CH2 CH2 CH2 CH2 CH2 COOH COOH 12 10 pK2=9.67 8 谷氨酸 PH 6 pKR=4.25 4 pK1=2.19 11 1 0 1.0 2.0 3.0 OH (equivalents)
14 谷氨酸的滴定(解离)曲线 谷氨酸
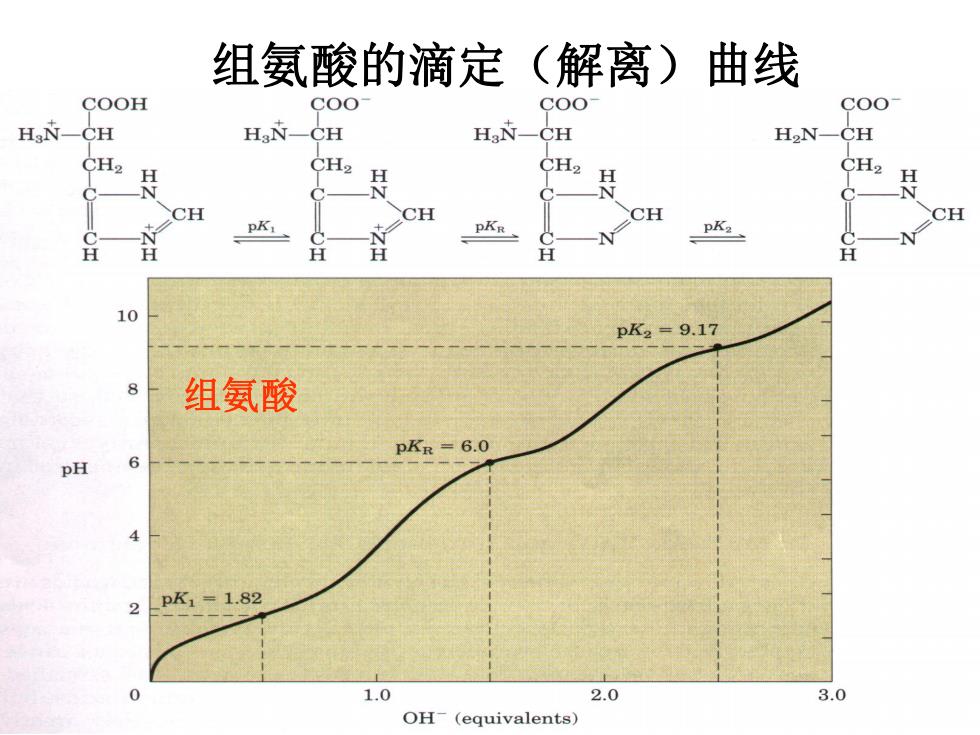
组氨酸的滴定 (解离)曲线 COOH COO COO COO HgN-CH HsN -CH HaN-CH H2N-CH CH2 CH2 CH2 H CH2 H CH CH CH H H 10 pK2=9.17 8 组氨酸 PKR=6.0 pH 4 pK1=1.82 0 1.0 2.0 3.0 OH(equivalents)
15 组氨酸的滴定(解离)曲线 组氨酸