
蛋白质(protein) 是生物体的基本组成成分之一,也是生物体中含量最丰富的 生物大分子(biomacromolecule) 蛋白质分布广泛,几乎所有的器官组织都含有蛋白质. 各自有特殊的结构与功能,承担着完成生物体内各种生理 功能的任务,如:酶、抗体、凝血因子、多肽激素、转运 蛋白、收缩蛋白、基因调控蛋白等。 蛋白质是生命活动的物质基础,没有蛋白质就没有生命活 动。 生物化学与分子生物学教研室
生物化学与分子生物学教研室 蛋白质(protein) 是生物体的基本组成成分之一,也是生物体中含量最丰富的 生物大分子(biomacromolecule) 蛋白质分布广泛,几乎所有的器官组织都含有蛋白质. 各自有特殊的结构与功能,承担着完成生物体内各种生理 功能的任务,如:酶、抗体、凝血因子、多肽激素、转运 蛋白、收缩蛋白、基因调控蛋白等。 蛋白质是生命活动的物质基础,没有蛋白质就没有生命活 动

第一节蛋白质的分子组成 元素组成包括碳、氢、氧、氮、硫,及其他 金属元素。 各种蛋白质含氮量很接近,平均为16%。 1克样品含氮克数×6.25 =1克样品中的蛋白质含量 生物化学与分子生物学教研室
生物化学与分子生物学教研室 第一节 蛋白质的分子组成 元素组成包括碳、氢、氧、氮、硫,及其他 金属元素。 各种蛋白质含氮量很接近,平均为16%。 1克样品含氮克数×6.25 =1克样品中的蛋白质含量

一、 氨基酸(amino acid,aa) 组成蛋白质的基本单位。人体蛋白质仅由20 种氨基酸构成。 proton H Side chain R COOH caboxyl a-carbon atom NH2 Amino group 生物化学与分子生物学教研室
生物化学与分子生物学教研室 一、氨基酸(amino acid,aa) 组成蛋白质的基本单位。人体蛋白质仅由20 种氨基酸构成。 caboxyl Amino group proton Side chain α-carbon atom C H COOH NH2 R
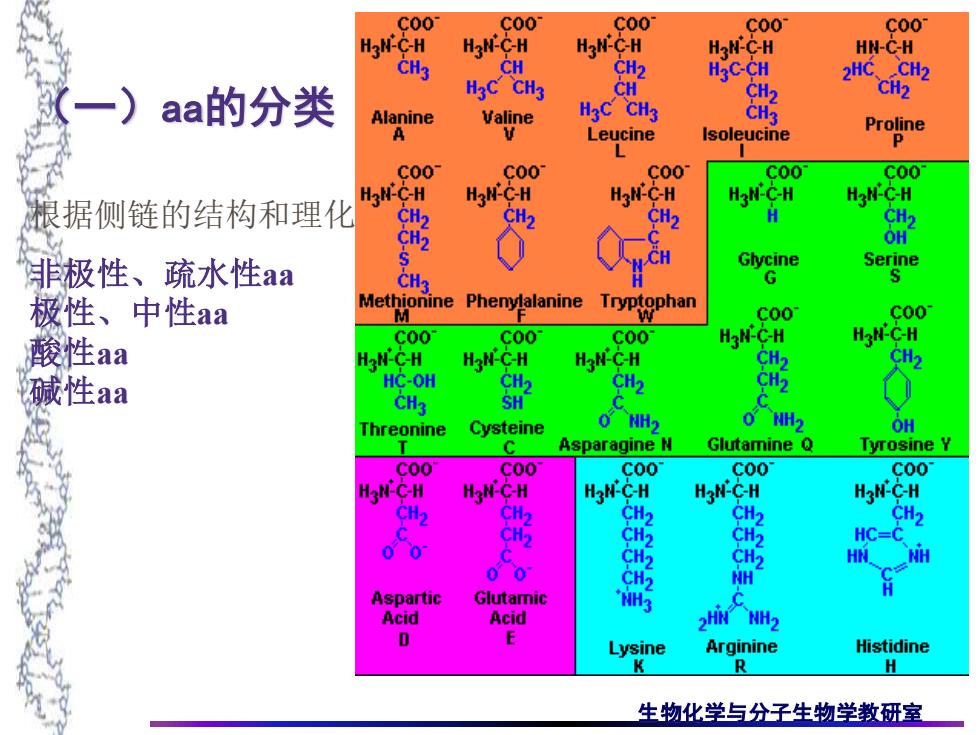
00 C00 C00 C00 C00 HgN-C- C-H H3N-C-H HN-C CH3 H2 H3C-CH 2HC CH2 一)aa的分类 HaC CH3 C CH2 Alanine Valine CH3 CH3 Proline A Leucine Isoleucine p L C00 00 C00 C00 C00 HaN-C-H HgN-C-H H3N-C-H H3N-C-H 根据侧链的结构和理化 H CH2 2 OH 非极性、疏水性aa CH Ghycine Serine CH3 G 极性、中性aa Methionine Phenylalanine Tryptophan W C00 C00 酸性aa C00 C00 C00 H3N-C- H3N-C-H HgNC-H H3N-C-H H3N-C-H CH2 CH2 碱性aa HC-OH CH2 CH2 CH3 0 Threonine Cysteine NH2 OH Asparagine N Glutamine Q Tyrosine c00 C00 001 C00 H3N-C-H H3N-C CH CH2 CH2 HC=C CH2 HN NH NH NH3 H Acid 2 Lysine Arginine Histidine K R H 生物化学与分子生物学教研室
生物化学与分子生物学教研室 (一)aa的分类 根据侧链的结构和理化性质分成四类: 非极性、疏水性aa 极性、中性aa 酸性aa 碱性aa

(二)氨基酸的理化性质 1、两性电离及等电点 R R R +OH OH CH-NH,* CH-NH" CH-NH2 COOH -H+ C00 +H C00 pH<pI pH=pI pH>pI 净电荷为正 净电荷=0 净电荷为负 当溶液在某一定H值时,氨基酸分子上所带正负电 荷相等,成为两性离子,在电场中既不向阳极也不向阴极 移动,此时溶液的pH值即为该氨基酸的等电点(isoelectric point,pl。 生物化学与分子生物学教研室
生物化学与分子生物学教研室 pH = pI 净电荷=0 pH< pI 净电荷为正 pH > pI 净电荷为负 CH R COOH NH3 + CH R COO CH NH2 R COO NH3 + + H+ + OH- + H+ + OH- 当溶液在某一定pH值时,氨基酸分子上所带正负电 荷相等,成为两性离子,在电场中既不向阳极也不向阴极 移动,此时溶液的pH值即为该氨基酸的等电点(isoelectric point,pI)。 (二)氨基酸的理化性质 1、两性电离及等电点