
第十章 含氮含磷有机化合物 教学目标: 1.胺的结构和性质。对于胺的碱性及氮原子上的未共用电子对的亲核性应作详细介绍。 例,各类胺的碱性强弱比较及其原因,烃基化、酰基化反应的应用等。 2.酰胺的结构对于了解蛋白质结构有重要作用应该详细讲解。此外,通过酰胺与溴的氢 氧化钠反应的讲授,使学生认识到分子重排是有机反应的一个重要类型。 3.芳香重氮盐的讲解,可着重于生成重氮盐的条件及其在合成上的应用。季铵碱热分解 的霍夫曼规则是杏讲授山教师自己决定。 教学重点、难点: 胺的结构和化学性质。重氮盐在有机合成上的应用 教学方法、手段:讲授、CAI课件辅助教学。 本章学时:5学时

教学内容: 第九章含氮和含磷有机化合物 分子中含有C一N键的化合物称为含氮有机化合物。含氨有机化合物的种类很多。例如 前面学习过的硝基苯,酰胺,苯肼等,甚全于氨基酸、蛋白质和含氮的杂环化合物等都属于 含氮有机化合物。 含磷有机化合物广泛存在于尘物体内。它们有的是维持尘命和生物体遗传不可缺少的物 质。在农业上,许多含磷有机化合物用作杀虫剂、杀菌剂和植物生长调节剂等,已成为一类 极为重要的农药。 第一节胺 胺类化合物可以看作是氨的烃类衍生物,广泛存在于自然界中。胺类化合物和生命活动 有密切的关系,许多激素、抗生素、尘物碱及所有的蛋白质、核酸都是胺的复杂衍生物。 一,胺的分类和命名 1.胺的分类 根据氮原子上所连烃基的数目,可把胺分为伯胺(一级胺)、仲胺(二级胺)、叔胺(二 级胺)、季铵盐(四级铵盐)和季铵碱(四级铵碱)。例: RNH2 R2NH RN RNX RANOH 伯胺 仲胺 叔胺 季铵盐 季铵碱 需要注意的是伯、仲、叔胺的分类方法与学过的伯、仲、叔卤代烃和伯、仲、叔醇的分 类方法是不同的。例: CH; CHs CH3 H3C一C-CH3 H:C-C-CHg HC-C-CHa Cl OH NH, 叔卤代烃 叔醇 伯胶 根据分子中烃基的结构,可把胺分为脂肪胺和芳香胺。例: NH2 CH,CH,NH, CH:CH2NH2 脂肪胺 NH NHCH2CH3 NH 芳香胶 根据分子中氨基的数目,可把胺分为一元胺、二元胺和多元胺等。例如: NH NH2 NH HNCH,CH2NH2 一儿胺 二元胺 多元胺 2.胺的命名

结构简单的胺可以根据烃基的名称命名,即在烃基的名称后加上“胺”字。若氮原子上 所连烃基相同,用二或二表明烃基的数日:若氮原子上所连烃基不同,则按基团的次序规则 山小到大写出其名称,“基”宁一般可省略。例: CH:NH2 CH:NHCH3 (CH3)2NCH2 CH3 甲胺 二甲胺 二甲基乙基胺 H2NCH2CH2NH2 H2NCH2CH2CH2CH2CH2CH2NH2 H2NCH2CH2 CH2 CH2 NH2 1.2-乙二胺 1.6-已二胺 1.4-」广二胺(腐胶) 芳香胺的命名,一般把芳香胺定为母体,其它烃基为取代基。命名时应标出烃基的位置, 接在氮上的烃基用“N某基”来表示。例: HC. CH,CH3 NH2 NHCH. CH3 对甲基苯胺 N甲基苯胺 N-甲基N-乙基对氯苯胶 复杂的胺则以烃为母体,氨基作为取代基来命名。例1: H C-CH CH,CHCH CH,CH,CH-CH-N(CH) CH2 NH2 CH CH 2甲基-4-氨基戊烷 3甲基-2(N,N甲氨基)戊烷 季铵盐或季铵碱可以看作铵的衍生物来命名。例如: (CH3)4N'CI [(CH3)3N CH2 CH3 ]OH 氯化四甲铵 氢氧化二甲基乙基铵 二.胺的物理性质 常温下,低级和中级脂肪胺为无色气体或液体,高级脂肪胺为固体,芳香胺为高沸点 的液体或固体。低级胺具有氨的气味或鱼腥味,高级胺没有气味,芳香胺有特殊气味,并有 较大的毒性。 山于胺是极性化合物,除叔胺外,其它胺分子间可通过氢键缔合,因此胺的熔点和沸 点比分子量相近的非极性化合物高。但山于氮的电负性比氧小,所以胺形成的氢键弱于醇或 羧酸形成的氢键,因而胺的熔点和沸点比分子量相近的醇和羧酸低。 伯、仲、叔胺都能与水形成氢键,所以低级脂肪胺可溶于水。随着烃基在分子中的比 例增大,溶解度迅速下降,所以中级胺、高级胺及芳香胺微溶或难溶于水。胺大都可溶于 有机溶剂。 三.胺的化学性质 氨基是胺类化合物的官能团,氨基中的氮原子为不等性p杂化,其中一个杂化轨道上 有一对未共用电子对,其余二个杂化轨道上各有一个电子。这样,氮原子可以和共它三个原 子分别形成二个0键,胺分子的构型是二三角锥形,与氨的构型相似

HR) H(R") H(R) (A)脂肪胶 (B)芳香胺 脂肪胺和芳香胺的结构 与氨相似,氨基中的氮原子上含有一对未共用电子对,有与其它原子共享这对电子的倾 向,所以胺具有碱性和亲核性。在芳香胺中,山于未共用电子对与苯环π键发生部分重叠, 使N原子的sp3轨道的未成键电子对的p轨道性质增加,N原子山sp杂化趋向于p2杂化。 因此,这对未共用电子对与芳环的π电子可以形成Ⅱ共轭体系,使芳香胺的碱性和亲核 性都有明显的减弱。另外,芳香胺中的这种厂π共轭体系使芳环的电子云密度增大,因此 芳香胺在芳环上容易发生亲电取代反应。 1.碱性 氨基的未共用电子对能接受质子,因此胺显碱性。按的碱性强弱用离解常数Kb或其负 对数DKb表示,Kb愈大或DKb愈小,碱性愈强。胺可以和大多数酸反应生成盐。 RNH2+H2O-RNH3+OH RNH2+HCI RNHCI 在脂肪胺中,山于烷基的+【效应,使氨基上的电子云密度增加,接受质子的能力增强, 所以脂肪胺的碱性大于氨。在芳香胺中,山于氨基的未共用电子对与芳环的大π键形成厂 T共轭体系,使氨基上的电子密度降低,接受质子的能力械弱,所以它的碱性比氨弱。取代 苯胺的碱性强弱取决于取代基的性质,取代基为供电子基团时,使碱性增强:取代基为吸电 子基团时,使减性城弱。 胺的碱性强弱除与烃基的诱导效应和共轭效应有关外,还受到水的溶剂化效应,空间 位阻效应等因素的影响。胺分子中,氮上连接的氢愈多,溶剂化程度愈大,铵正离子就愈稳 定,胺的碱性也愈强:氮上取代的烃基愈多,空间位阻愈大,使质子个易与氮原子接近,胺 的碱性也就愈弱。 综合以上各种效应的作用结果,胺类化合物的碱性强弱次序一般为: 脂肪族仲胺>脂肪族伯胺〉脂肪族叔胺〉氨〉芳香族伯胶〉芳香族仲胺〉芳香族叔胺 山于胺是弱碱,与酸生成的铵盐遇强碱会释放出原来的胺。 RN H:CI+NaOH RNH2 +NaCl+H2O 可以利用这一性质进行胺的分离、提纯。1将不溶于水的胺溶于稀酸形成盐,经分离后, 再用强碱将胺山铵盐中释放出来。 2.烷基化反应 卤代烃可以与氨作用生成胺,胺作为亲核试剂又可以继续与卤代烃发生亲核取代反应, 结果得到仲胺、叔胺,直至生成季铵盐。 NH;+RX -RNH2+HX RNH2+RX RNH+HX RNH+RX RN+HX
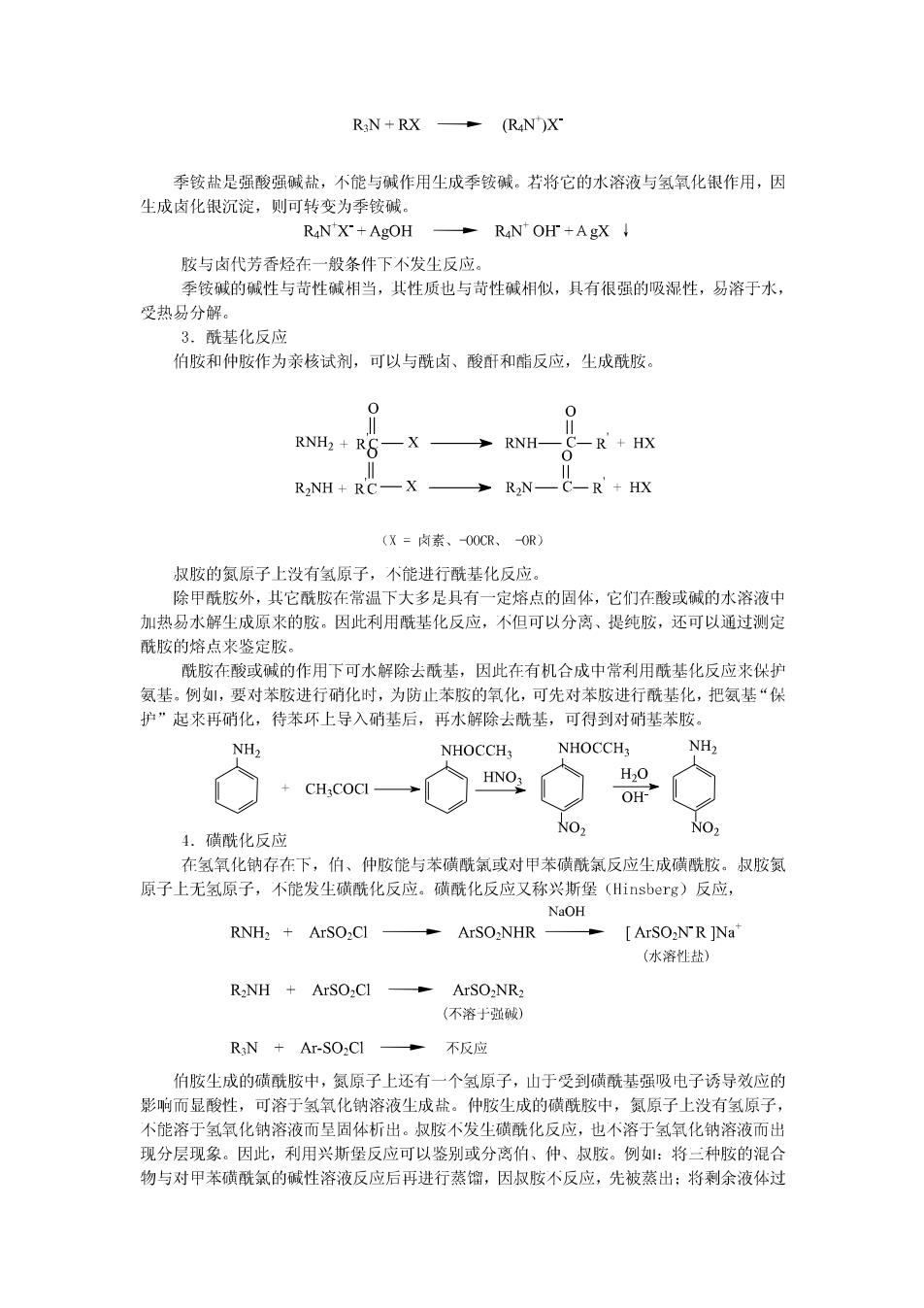
RiN+RX (R4N)X 季铵盐是强酸强碱盐,不能与碱作用生成季铵减。若将它的水溶夜与氢氧化银作用,因 尘成卤化银沉淀,则可转变为季铵碱。 RANX+AgOH R4NOH+AgX↓ 胺与卤代芳香烃在一般条件下不发生反应。 季铵碱的碱性与苛性碱相当,其性质也与苛性碱相似,具有很强的吸湿性,易溶于水, 受热易分解。 3.酰基化反应 伯胺和仲胺作为亲核试剂,可以与酰卤、酸酐和酯反应,生成酰胺。 0 0 RNH,+RS一X RNH- C-R+HX RNH+RC—X多RN—C-R'+HX (X=卤素、O0CR、OR) 叔胺的氮原子上没有氢原子,不能进行酰基化反应。 除甲酰胺外,其它酰胺在常温下大多是具有一定熔点的固体,它们在酸或碱的水溶液中 加热易水解生成原来的胺。因此利用酰基化反应,不但可以分离、提纯胺,还可以通过测定 酰胺的熔点来鉴定胺。 酰胺在酸或碱的作用下可水解除去酰基,因此在有机合成中常利用酰基化反应来保护 氨基。例,要对苯胺进行硝化时,为防止苯胺的氧化,可先对苯胺进行酰基化,把氨基“保 护”起来再硝化,待苯环上导入硝基后,再水解除去酰基,可得到对硝基苯胺。 NH2 NHOCCH NHOCCH NH2 HNO H2O CHCOCI OH- NO NO2 4.磺酰化反应 在氢氧化钠存在下,伯、仲胺能与苯磺酰氯或对甲苯磺酰氣反应生成磺酰胺。叔胺氮 原子上无氢原子,不能发生磺酰化反应。磺酰化反应又称兴斯堡(Hinsberg)反应, NaOH RNH2+ArSO2Cl ArSO-NHR ArSO2NR ]Na (水溶性盐) RNH ArSO,CI ArSO-NR2 (不溶于强碱) R3N Ar-SO2CI 。不反应 伯胺尘成的磺酰胺中,氮原子上还有一个氢原子,山于受到磺酰基强吸电子诱导效应的 影响而显酸性,可溶于氢氧化钠溶液生成盐。仲胺生成的磺酰胺中,氮原子上没有氢原子, 不能溶于氢氧化钠溶液而呈固体析出。叔胺不发生磺酰化反应,也不溶于氢氧化钠溶液而出 现分层现象。因此,利用兴斯堡反应可以鉴别或分离伯、仲、叔胺。例:将三种胺的混合 物与对甲苯磺酰氯的碱性溶液反应后再进行蒸馏,因叔胺不反应,先被蒸出:将剩余液体过