
Chapter 5 Redox titration (Oxidimetry) Lecture 1
1 Chapter 5 Redox titration (Oxidimetry) Lecture 1

第五章 氧化还原滴定法 Redox titration 一、 氧化还原反应平衡Redox equilibrium 二、氧化还原反应进行的程度Reaction completeness 三、氧化还原反应的速率与影响因素 Rate of reaction and influencing factors 四、氧化还原滴定指示剂Redox indicators 五、氧化还原滴定原理Oxidimetric principle 六、氧化还原滴定前的预处理Pretreatment 七、常用的氧化还原滴定法Common used titration 2
2 第五章 氧化还原滴定法 Redox titration 一、氧化还原反应平衡 Redox equilibrium 二、氧化还原反应进行的程度 Reaction completeness 三、氧化还原反应的速率与影响因素 Rate of reaction and influencing factors 四、氧化还原滴定指示剂 Redox indicators 五、氧化还原滴定原理 Oxidimetric principle 六、氧化还原滴定前的预处理 Pretreatment 七、常用的氧化还原滴定法 Common used titration

A brief introduction 1、氧化还原滴定: 以氧化还原反应为基础的滴定分析方法 2、实质:电子转移 3、特点:)机理复杂、多步反应 2)有的程度虽高但速度缓慢 3)有的伴有副反应而无明确计量关系 4、分类:碘量法、高锰酸钾法、重铬酸钾法、 亚硝酸钠法、溴量法、铈量法 5、应用:广泛,直接或间接测定无机物、有机物
3 A brief introduction 1、氧化还原滴定: 以氧化还原反应为基础的滴定分析方法 2、实质:电子转移 3、特点:1)机理复杂、多步反应 2)有的程度虽高但速度缓慢 3)有的伴有副反应而无明确计量关系 4、分类:碘量法、高锰酸钾法、重铬酸钾法、 亚硝酸钠法、溴量法、铈量法 5、应用:广泛,直接或间接测定无机物、有机物

氧化还原反应平衡 Redox equilibrium 氧化还原反应一电子的转移 Ox1 Red2 Red1+Ox2 由电对电位FOx/Red的高低判断反应方向 4
4 一、 氧化还原反应平衡 Redox equilibrium 氧化还原反应—电子的转移 Ox1 + Red2 = Red1 + Ox2 由电对电位 EOx/ Red 的高低判断反应方向
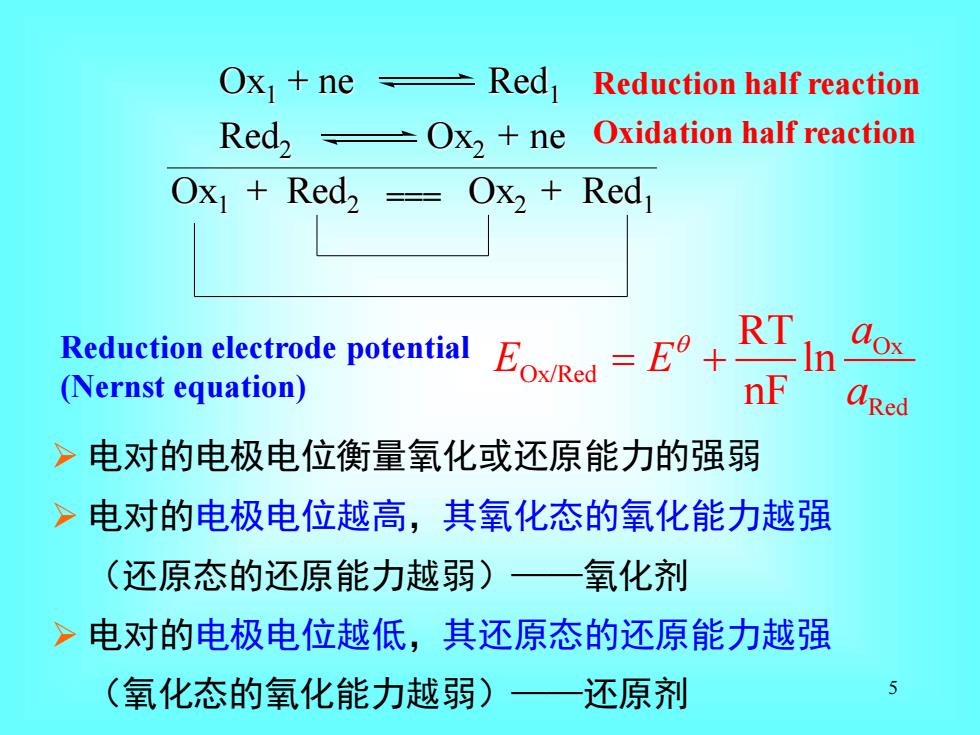
Ox1+ne±Red1 Reduction half reaction Red,Ox2 ne Oxidation half reaction Ox Red2 -Ox2 Red Redction trode potential E RT (Nernst equation) nF aRed >电对的电极电位衡量氧化或还原能力的强弱 >电对的电极电位越高,其氧化态的氧化能力越强 (还原态的还原能力越弱) 氧化剂 >电对的电极电位越低,其还原态的还原能力越强 (氧化态的氧化能力越弱)》 还原剂
5 ➢ 电对的电极电位衡量氧化或还原能力的强弱 ➢ 电对的电极电位越高,其氧化态的氧化能力越强 (还原态的还原能力越弱)——氧化剂 ➢ 电对的电极电位越低,其还原态的还原能力越强 (氧化态的氧化能力越弱)——还原剂 Ox1 + ne Red1 Red2 Ox2 + ne Ox1 + Red2 Ox2 + Red1 Oxidation half reaction Reduction half reaction Ox Ox/Red Red RT ln nF a E E a = + Reduction electrode potential (Nernst equation) ===