
第三章酸碱滴定 第五节酸碱滴定指示剂
第三章 酸碱滴定 第五节 酸碱滴定指示剂

一、指示剂的作用原理 Chromogenic mechanism of acid-base indicators 酸碱滴定过程-体系无颜色变化 确定滴定终点-依靠指示剂的颜色变化 酸碱指示剂-有机弱酸或有机弱碱 共轭酸碱对-结构不同,颜色不同 酸式结构酸色、碱式结构碱色) 理论变色点-体系pH值等于pKa (结构转变,各占50%)
2 一、指示剂的作用原理 Chromogenic mechanism of acid-base indicators 酸碱滴定过程 - 体系无颜色变化 确定滴定终点 - 依靠指示剂的颜色变化 酸碱指示剂 - 有机弱酸或有机弱碱 共轭酸碱对 - 结构不同,颜色不同 (酸式结构酸色、碱式结构碱色) 理论变色点 - 体系pH值等于pKa (结构转变,各占50%)

二、指示剂的pH变色范围 The pH range for color change of indicators Hn在溶液中的离解平衡为: HIn H+In- (酸式色) (碱式色) K。= [H*][n] pH pK,+log [In [HIn] [HIn] [n-/Hn≥10 碱色 pH≥pK,+l n]/Hn]≤0.1 酸色 pH≤pK。-1 0.1≤n/Hn]≤10 混合色,肉眼难分辨 变色范围:pH=pKa士1 3
3 二、指示剂的pH变色范围 The pH range for color change of indicators HIn在溶液中的离解平衡为: HIn = H+ ﹢ In- (酸式色) (碱式色) [In- ]/[HIn] ≥10 碱色 [In- ]/[HIn] ≤ 0.1 酸色 0.1≤[In- ]/[HIn] ≤ 10 混合色,肉眼难分辨 变色范围:pH=pKa±1

酸型和碱型具有不同的颜色 The acidic state and base state of indicator have different colors 甲基橙Methyl Orange(MO) (H3C)2N- N=N〈 S03 pKa=3.4 (H3C)2N= N-N S03 红3.1-4.0(橙) -4.4黄
4 甲基橙 Methyl Orange (MO) 红3.1- 4.0(橙)- 4.4黄 酸型和碱型具有不同的颜色 The acidic state and base state of indicator have different colors N N SO3 - N N (H3C)2N H SO3 - (H3C)2N H pKa=3.4 OH - +
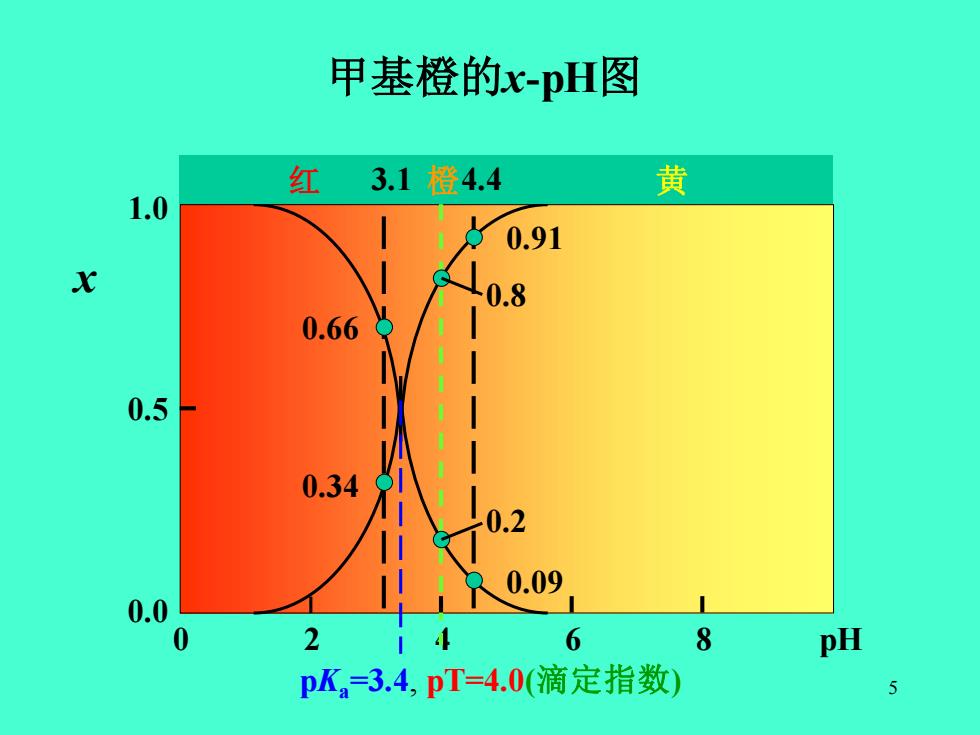
甲基橙的x-pH图 红 3.1橙4.4 黄 1.0 0.91 X 0.66 0.5 0.34 0.09 0.0 0 2 6 8 pH pK。=3.4,pT=4.0(滴定指数) 5
5 甲基橙的x-pH图 0 2 4 6 8 pH pKa=3.4, pT=4.0(滴定指数) 红 3.1 4.4 橙 黄 0.66 0.34 0.91 0.09 0.8 0.2 1.0 0.5 0.0 x