
吸电了基团的数目增加,鞍性增踫 CH3COOH C1CH2COOH C12CHCOOH C13CCOOH pKa 4.76 2.86 1.26 0.64 收电了基团距离羧基越近,酸性越出 CH3CH2 CH2 COOH CH2CH2CH2 COOH CH3 CH CH2 COOH CH3 CH2 CHCOOH C1 pKa 4.82 4.52 4.06 2.86 当烃基上连有给电子基团时,山于给电子效应使羧基中羟基氧原子上的电子云密度升 高,O一H键的极性减弱,因而较难电离出H,其酸性减弱。总之,基团的给电子能力越 强,羧酸的酸性就愈弱。 给电了基团的数目增加,酸性减网 HCOOH CH;COOH CHCH2COOH (CH3)3C COOH pKa 3.77 4.76 4.88 5.05 二元羧酸中,山于羧基是吸电子基团,两个羧基相互影响使一级电离常数比一元饱和羧 酸大,这种影响随着两个羧基距离的增大而减弱。二元羧酸中,草酸的酸性最强。 不饱和脂肪羧酸和芳香羧酸的酸性,除受到基团的诱导效应影响外,往往还受到共轭效 应的影响。一般来说,不饱和脂肪羧酸的酸性略强于相应的饱和脂肪羧酸。当芳香环上有基 团产尘吸电子效应时,酸性增强,产尘给电子效应时,酸性减弱,例: COOH COOH COOH COOH N02 OCH3 pKa 3.40 3.97 4.20 4.47 2.羧酸衍生物的生成 羧基中羟基被其它原子或基团取代的产物称为羧酸衍生物。如果羟基分别被卤素(一 X)、酰氧基(OCOR)、烷氧基(一OR)、氨基(一NH2)取代,则分别生成酰卤、酸酐、 酯、酰胺,这些都是羧酸的重要衍尘物。 (1)酰卤的生成羧酸与三卤化磷、五卤化磷或亚硫酰氯等反应,羧基中的羟基可被卤 素取代尘成酰卤。 R-C-OH+PC13△→R-C-C1+H,P0 0 OPC15RC-CI+POC+C1
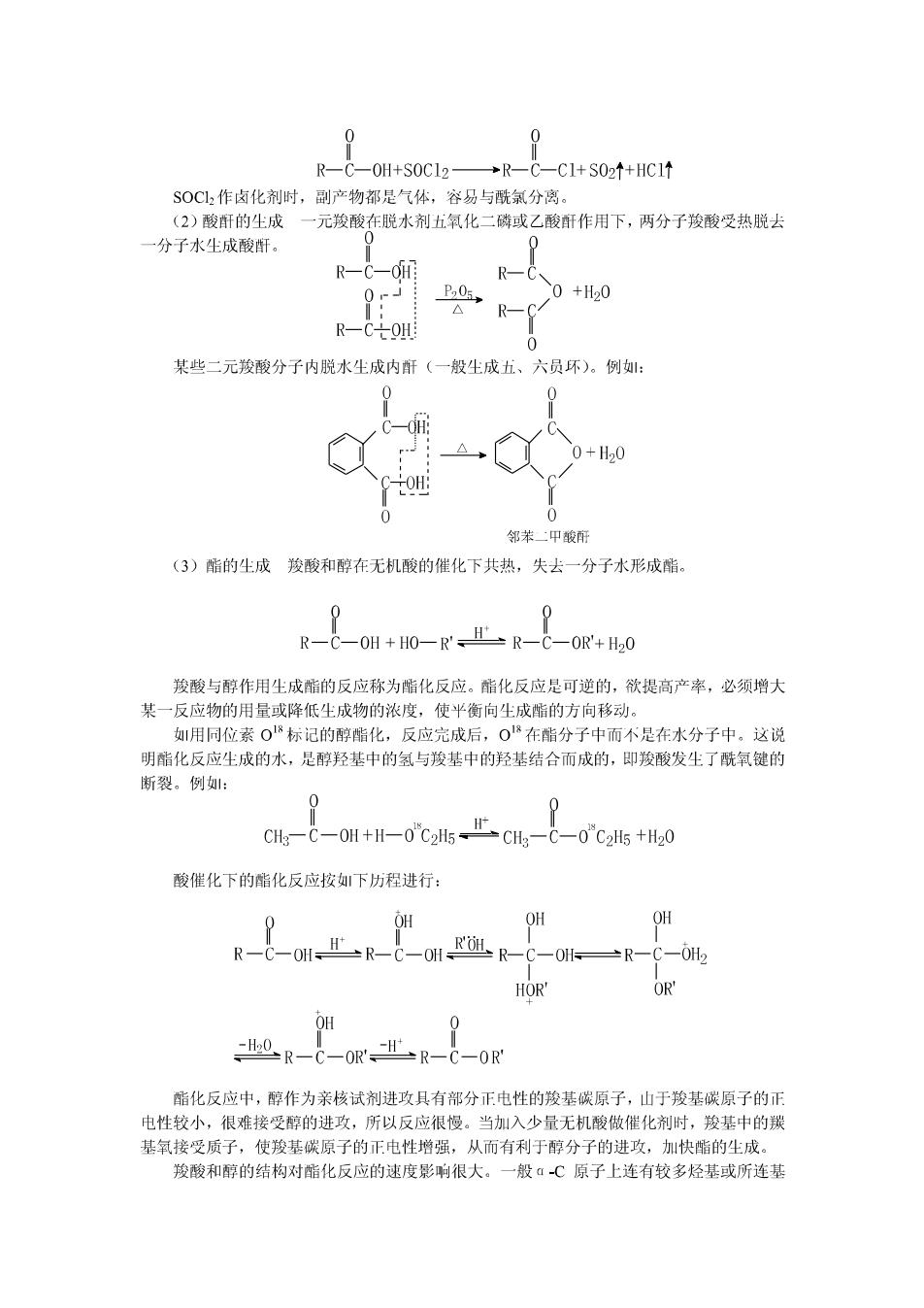
R-C-0H+S0C12→R-C-C1+S02↑+HC1t SOC2作卤化剂时,副产物都是气体,容易与酰氯分离。 (2)酸酐的生成一元羧酸在脱水剂五氧化二磷或乙酸酐作用下,两分子羧酸受热脱去 一分子水生成酸酐。 0 0 P05, 0+H20 △ R- R-COH 某些二元羧酸分子内脱水生成内酐(一般生成五、六员环)。例如: 0 -0H 0+H20 -OH 0 邻苯二甲酸所 (3)酯的生成羧酸和醇在无机酸的催化下共热,失去一分子水形成酯。 羧酸与醇作用生成脂的反应称为脂化反应。酯化反应是可逆的,欲提高产率,必须增大 某一反应物的用量或降低生成物的浓度,使平衡向生成脂的方向移动。 用同位素O18标记的醇酯化,反应完成后,O18在酯分子中而不是在水分子中。这说 明酯化反应生成的水,是醇羟基中的氢与羧基中的羟基结合而成的,即羧酸发生了酰氧键的 断裂。例: 0 CH-C-OH+H-0Cs CHt-C-0"C2ls +H20 酸催化下的酯化反应按如下历程进行: OH OH OH R--0m-上R-R-C-一R-- HOR' OR' OH -ILO-R-C-ORR-C-0R 酯化反应中,醇作为亲核试剂进攻具有部分正电性的羧基碳原子,山于骏基碳原子的正 电性较小,很难接受醇的进攻,所以反应很慢。当加入少量无机酸做催化剂时,羧基中的羰 基氧接受质子,使羧基碳原子的正电性增强,从而有利于醇分子的进攻,加快脂的生成。 羧酸和醇的结构对酯化反应的速度影响很大。一般α-C原子上连有较多烃基或所连基