
含氨有机化合物的化学性质摘要 §1硝基化合物 一、概述 硝基化合物山于具有较强的极性,因此硝基化合物的熔点、沸点比相应的卤代烃高,多 为高沸点的液体或固体。多硝基化合物具有爆炸性。液念的硝基化合物是许多有机化合物的 优良溶剂,但硝基化合物有毒,它的蒸气能透过皮肤使人中毒,因此应尽量避免使用硝基化 合物做溶剂。 二、还原反应 硝基容易被还原,尤其是直接连在芳环上的硝基,还原产物随还原介质的不同而有所不 同。硝基苯在酸性条件下,可用铁等金属还原为芳香族伯胺。 Fe+HCI NH §2胺 一、概述 与氨相似,氨基中的氮原子上含有一对未共用电子对,有与其它原子共享这对电子的倾 向,所以胺具有碱性和亲核性。在芳香胺中,山于未共用电子对与苯环π键发生部分重叠, 使N原子的sp轨道的未成键电子对的p轨道性质增加,N原子山p杂化趋向于sp杂化。 因此,这对未共用电子对与芳环的T电子可以形成广π共轭体系,使芳香胺的碱性和亲核 性都有明显的减弱。另外,芳香胺中的这种口π共轭体系使芳环的电子云密度增大,因此 芳香胺在芳环上容易发生亲电取代反应。 二、烷基化反应 卤代烃可以与氨作用生成胺,胺作为亲核试剂又可以继续与卤代烃发生亲核取代反应, 结果得到仲胺、叔胺,直全生成季铵盐。 NH+RX RNH,+HX RNH2+RX- RNH+HX RNH+RX RN+HX R3N+RX (R4N)X 季铵盐是强酸强碱盐,不能与碱作用尘成季铵碱。若将它的水溶液与氢氧化银作用,因 生成卤化银沉淀,则可转变为季铵碱。 RANX+AgOH RNOH+AgX↓ 胺与卤代芳香烃在一般条件下不发生反应。 三、酰基化反应 伯胺和仲胺作为亲核试剂,可以与酰卤、酸酐和酯反应,生成酰胺

0 0 RNH2+RC—X RNH—C-R'+HX 0 0 R2NH+RC—X R2N—C-R+HX (X=肉素、O0CR、OR) 叔胺的氮原子上没有氢原子,不能进行酰基化反应。 除甲酰胺外,其它酰胺在常温下大多是具有一定熔点的固体,它们在酸或碱的水溶液中 加热易水解生成原来的胺。因此利用酰基化反应,不但可以分离、提纯胺,还可以通过测定 酰胺的熔点来鉴定胺。 酰胺在酸或碱的作用下可水解除去酰基,因此在有机合成中常利用酰基化反应来保护 氨基。例如,要对苯胺进行硝化时,为防止苯胺的氧化,可先对苯胺进行酰基化,把氨基“保 护”起来再硝化,待苯环上导入硝基后,再水解除去酰基,可得到对硝基苯胺。 NH2 NHOCCH3 NHOCCH NH2 HNO. H2O CHCOCI OH- NO2 四、磺酰化反应 在氢氧化钠存在下,伯、仲胺能与苯磺酰氯或对甲苯磺酰氯反应生成磺酰胺。叔胺氮 原子上无氢原子,不能发生磺酰化反应。磺酰化反应又称兴斯堡(Hinsberg).反应, NaOH RNH2 ArSO2Cl ArSO2NHR- [ArSO2N R INa' (水溶性盐) R2NH ArSO2C1 (不溶于逆碱) RiN Ar-SO,Cl 。不反应 伯胺生成的磺酰胺中,氮原子上还有一个氢原子,山于受到磺酰基强吸电子诱导效应的 影响而显酸性,可溶于氢氧化钠溶液生成盐。仲胺生成的磺酰胺中,氮原子上没有氢原子, 不能溶于氢氧化钠溶液而呈固体析出。叔胺不发生磺酰化反应,也不溶于氢氧化钠溶液而出 现分层现象。因此,利用兴斯堡反应可以鉴别或分离伯、仲、叔胺。例如:将三种胺的混合 物与对甲苯磺酰氯的碱性溶液反应后再进行蒸馏,因叔胺个反应,先被蒸出:将剩余液体过 滤,固体为仲胺的磺酰胺,加酸水解后可得到仲胺:滤液酸化后,水解得到伯胺。 五、与亚硝酸反应 不同的胺与亚硝酸反应,产物各不相同。山于亚硝酸不稳定,在反应中实际使用的是亚 硝酸钠与盐酸的混合物。 NaNO2+HC1 HNO2 NaCl 脂肪族伯胺与亚硝酸反应,尘成醇、烯烃、卤代烃等混合物,在合成上没有价值。但 放出的氮气是定量的,可用于氨基的定量分析。 RNH2 NaNO2+HCl- 醇、烯、卤代烃等混合物+↑
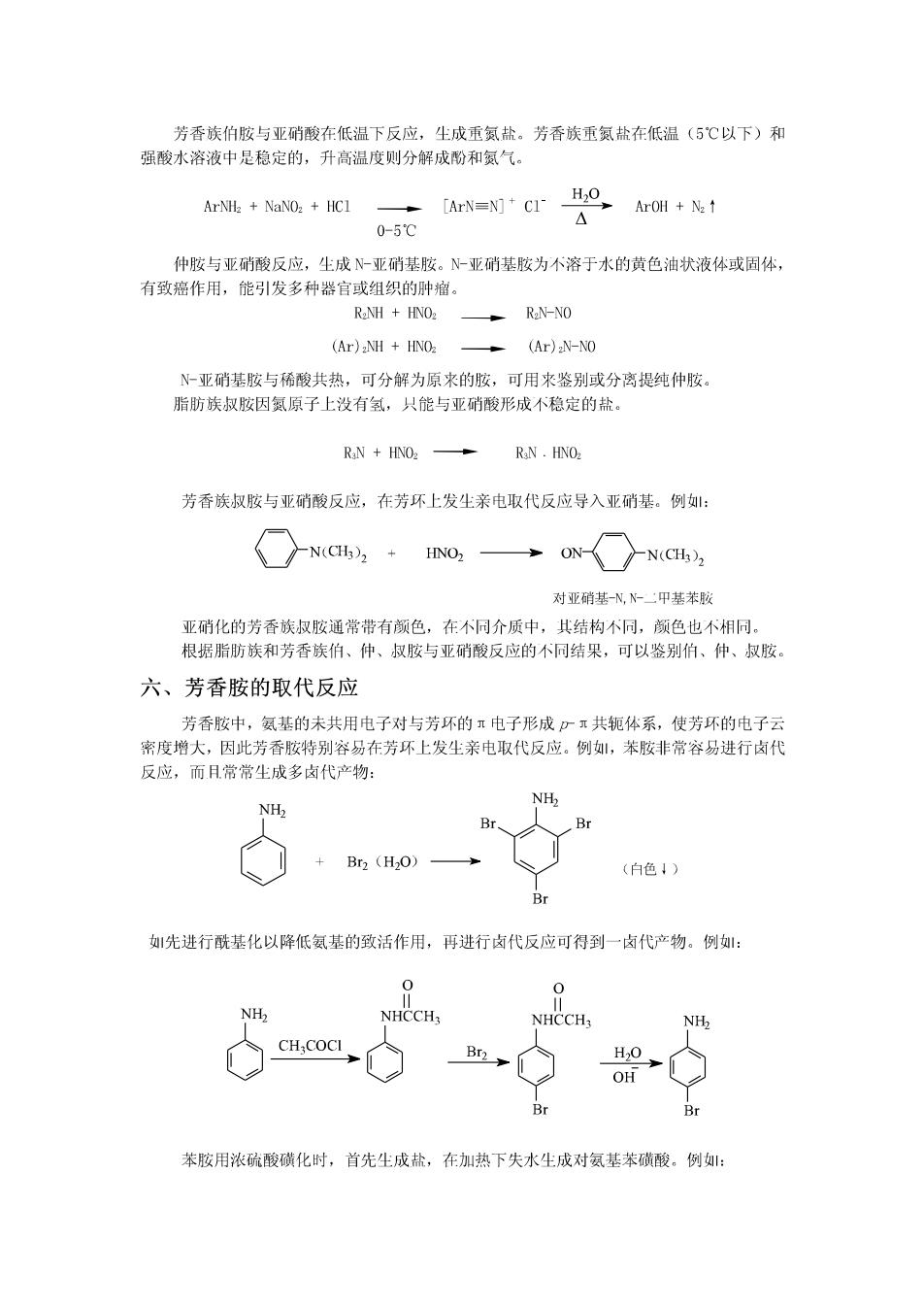
芳香族伯胺与亚硝酸在低温下反应,生成重氮盐。芳香族重氨盐在低温(5℃以下)和 强酸水溶液中是稳定的,升高温度则分解成酚和氨气。 ArNH2 NaNO2+HC1 [ArN=N]CI-H2o ArOH+N2↑ 0-5℃ 仲胺与亚硝酸反应,生成N-亚硝基胺。N-亚硝基胺为不溶于水的黄色油状液体或固体, 有致癌作用,能引发多种器官或组织的肿瘤。 R2NH HNO2 R2N-NO (Ar)2NH HNO2 (Ar)2N-NO N-亚硝基胺与稀酸共热,可分解为原来的胺,可用来鉴别或分离提纯仲胺。 脂肪族叔按因氮原子上没有氢,只能与亚硝酸形成不稳定的盐。 RaN HNO2 RaN HNOz 芳香族叔胺与亚硝酸反应,在芳环上发生亲电取代反应导入亚硝基。例: N(CH3),HNO2 ON N(CH3) 对亚硝基-N,N甲基苯胺 亚硝化的芳香族叔胺通常带有颜色,在不同介质中,其结构不同,颜色也不相同。 根据脂肪族和芳香族伯、仲、叔胺与亚硝酸反应的不同结果,可以鉴别伯、仲、叔胺。 六、芳香胺的取代反应 芳香胺中,氨基的未共用电子对与芳环的π电子形成少π共轭体系,使芳环的电子云 密度增大,因此芳香胺特别容易在芳环上发生亲电取代反应。例,苯胺非常容易进行卤代 反应,而且常常尘成多卤代产物: NHz NH> Br Br2(H2O) (白色1) Br 先进行酰基化以降低氨基的致活作用,再进行卤代反应可得到一卤代产物。例: 0 O NH2 NHCCH3 NHCCH3 NH2 CH:COCI Br H,O OH Br 苯胺用浓硫酸磺化时,首先生成盐,在加热下失水生成对氨基苯磺酸。例:
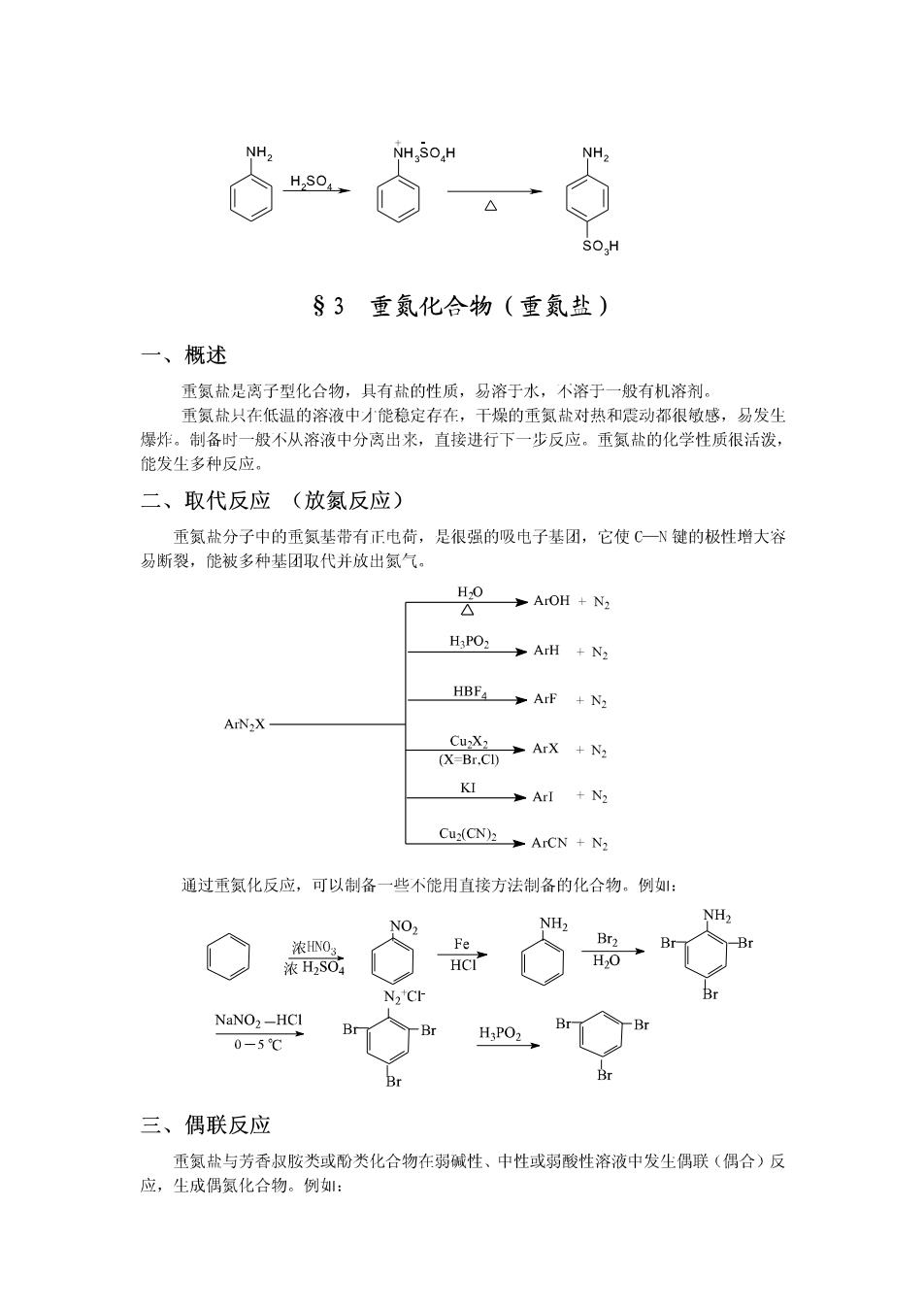
NH2 NH SOH Hs04, SO H §3重氨化合物(重氨盐) 一、概述 重氮盐是离子型化合物,具有盐的性质,易溶于水,不溶于一般有机溶剂。 重氮盐只在低温的溶液中才能稳定存在,干燥的重氮盐对热和震动都很敏感,易发生 爆炸。制备时一般不从溶液中分离出来,直接进行下一步反应。重氮盐的化学性质很活泼, 能发生多种反应。 二、取代反应(放氮反应) 重氮盐分子中的重氮基带有正电荷,是很强的吸电子基团,它使C一N键的极性增大容 易断裂,能被多种基团取代并放出氮气。 H2O △ ArOH N2 HPO> >ArH +N2 HBF4>ArF +N2 ArN2X CuX2 (X-Br.Cl) 多ArX+2 KI ArI N2 Cu(CN2→ArCN+N, 通过重氮化反应,可以制备一些不能用直接方法制备的化合物。例: NH2 NH2 NO? 浓HNO3 Fe Br2 Br 浓H2SO HCI H2O NaNO2-HCI Br Br H:PO2 0-5℃ 三、偶联反应 重氮盐与芳香叔胺类或酚类化合物在弱碱性、中性或弱酸性溶液中发生偶联(偶合)反 应,生成偶氮化合物。例:
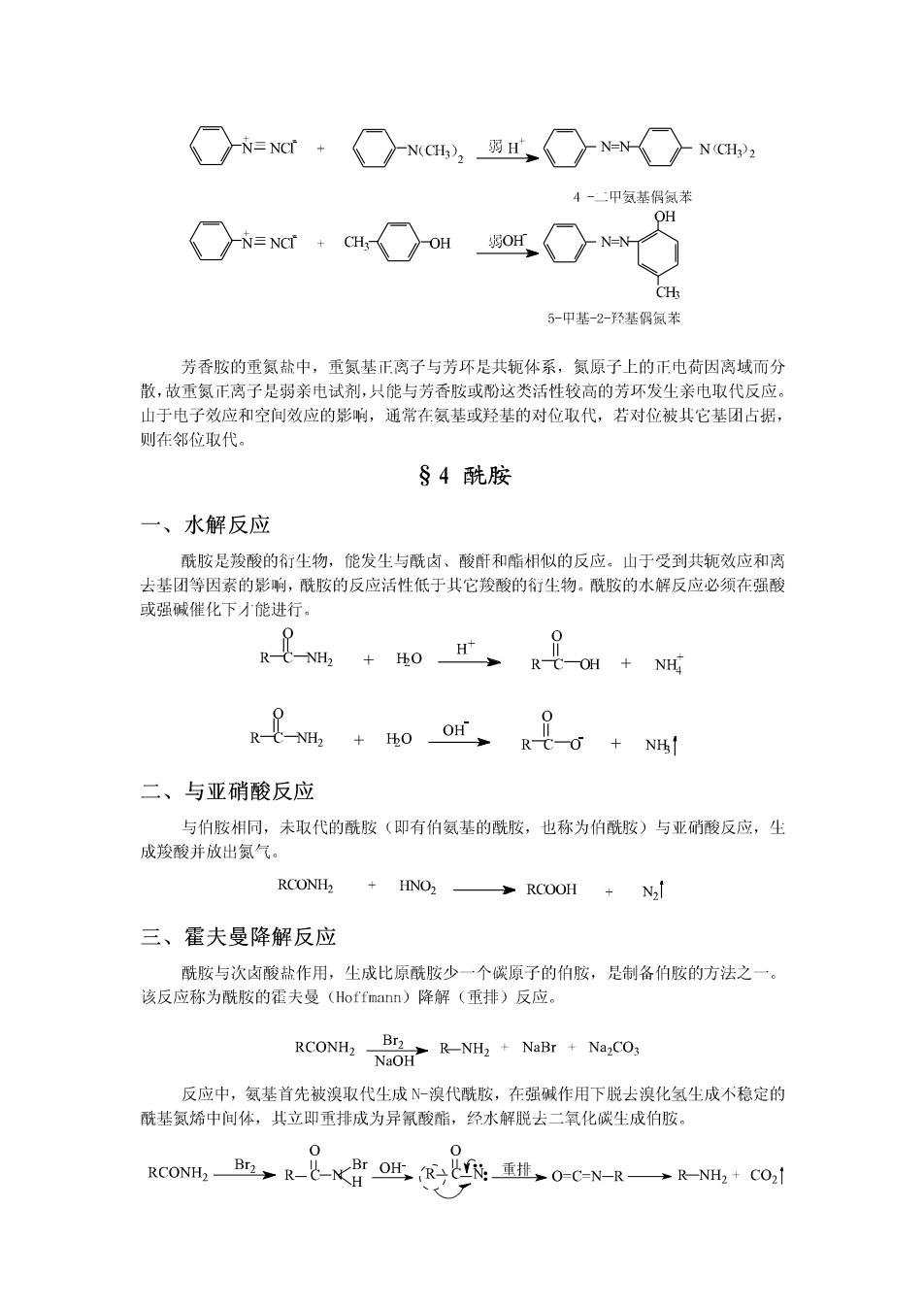
N=NCT+ N(CH2弱 N(CH?2 4-:甲氨基偶氮苯 OH N≡Ncr+CH OH 弱OH H 5-甲基-2-径基偶氮苯 芳香胺的重氮盐中,重氮基正离子与芳环是共轭体系,氮原子上的正电荷因离域而分 散,故重氨正离子是弱亲电试剂,只能与芳香胺或酚这类活性较高的芳环发生亲电取代反应。 山于电子效应和空间效应的影响,通常在氨基或羟基的对位取代,若对位被共它基团占据, 则在邻位取代。 §4酰胺 一、水解反应 酰胺是羧酸的衍生物,能发尘与酰卤、酸断和脂相似的反应。山于受到共轭效应和离 去基团等因素的影响,酰胺的反应活性低于其它羧酸的衍尘物。酰胺的水解反应必须在强酸 或强碱催化下才能进行。 t+o R-C-OH NH +40or、R 二、与亚硝酸反应 与伯胺相同,未取代的酰胺(即有伯氨基的酰胺,也称为伯酰胺)与亚硝酸反应,尘 成羧酸并放出氮气。 RCONH, 多RCOOH+ N2l 三、霍夫曼降解反应 酰胺与次卤酸盐作用,生成比原酰胺少一个碳原子的伯胺,是制备伯胺的方法之一。 该反应称为酰胺的霍夫曼(Hoffmann)降解(重排)反应。 RCONH2 NO R-NH2 NaBr NazCO; 反应中,氨基首先被溴取代生成N-溴代酰胺,在强碱作用下脱去溴化氢生成不稳定的 酰基氮烯中间体,其立即重排成为异氰酸酯,经水解脱去二氧化碳生成伯胺。 0 RCONHa,B,R-北-OH,Ry袋:重挂0C=N-R一→RNH,+CO,1