
1.同离子效应 当沉淀达平衡后,若向溶液中加入组成沉淀的构晶离 子试剂或溶液,使沉淀溶解度降低的现象称为同离子效应, 构晶离子:组成沉淀晶体的离子称为构晶离子 讨论:过量加入沉淀剂,可以增大构晶离子的浓度,降低沉淀 溶解度,减小沉淀溶解损失 √过多加入沉淀剂会增大盐效应或其他配位副反应,而使溶解 度增大 √沉淀剂用量: 一般一过量50%~100%为宜 非挥发性一过量20%~30% 16
1.同离子效应 当沉淀达平衡后,若向溶液中加入组成沉淀的构晶离 子试剂或溶液,使沉淀溶解度降低的现象称为同离子效应. 构晶离子:组成沉淀晶体的离子称为构晶离子. 讨论:过量加入沉淀剂,可以增大构晶离子的浓度,降低沉淀 溶解度,减小沉淀溶解损失 ✓ 过多加入沉淀剂会增大盐效应或其他配位副反应, 而使溶解 度增大 ✓ 沉淀剂用量:一般—— 过量50%~100%为宜 非挥发性 —— 过量20%~30% 16

例 用BaSO.重量法测定SO,2含量时,以BaCL,为沉淀剂, 计算加入过量0.1mol/LBa2+时,在200ml溶液中BaSO, 沉淀的溶解损失 解: 已知KsP(asa)=1.1×10-10 MBaso =233.4g mol Ba2+过量0.1mol/L与SO2反应的BaSO.沉淀溶解度为 S=[SO2]= Ks2_1.1×10-10 [Ba2+]0.1 =1.1×10-9mol/L →200ml溶液中BaSO,沉淀的溶解损失为 1.1×10-9×233.4×200=5.0×10-5mg<<0.2mg 溶解度减小了1万倍 17
例 解: 用BaSO4重量法测定SO4 2-含量时,以BaCl2为沉淀剂, 计算加入过量0.1mol/LBa2+时,在200ml溶液中BaSO4 沉淀的溶解损失 10 1.1 10 4 − 已知KSP(BaSO)= M g mol BaSO 233.4 / 4 = 2 2 4 4 10 2 9 4 2 0.1 / 1.1 10 [ ] 1.1 10 / [ ] 0.1 SP Ba mol L SO BaSO K S SO mol L Ba + − − − − + = = = = 过量 与 反应的 沉淀溶解度为 m g m g m l BaSO 1.1 10 233.4 200 5.0 10 0.2 200 9 5 4 = − − 溶液中 沉淀的溶解损失为 溶解度减小了1万倍 17

2.盐效应: 溶液中存在大量强电解质使沉淀溶解度增大的现象 讨论: MA(S)M叶+ An- 平衡时浓度S S K KP-=[M][A] YM*·YA 而T一定,K为定值 当存在大量强电解质时,ywy,→K个S个 注:沉淀溶解度很小时,常忽略盐效应 沉淀溶解度较大,且溶液离子强度很高时,要考虑盐效应 的影响 18
2. 盐效应: 溶液中存在大量强电解质使沉淀溶解度增大的现象 讨论: M A K S SP + − 当存在大量强电解质时, [ ] [ ] 0 + − = = + − M A K K M A SP SP 而T一定,KSP 0 为定值 注:沉淀溶解度很小时,常忽略盐效应 沉淀溶解度较大,且溶液离子强度很高时,要考虑盐效应 的影响 MA (s) M n+ + A n- 平衡时浓度 S S 18
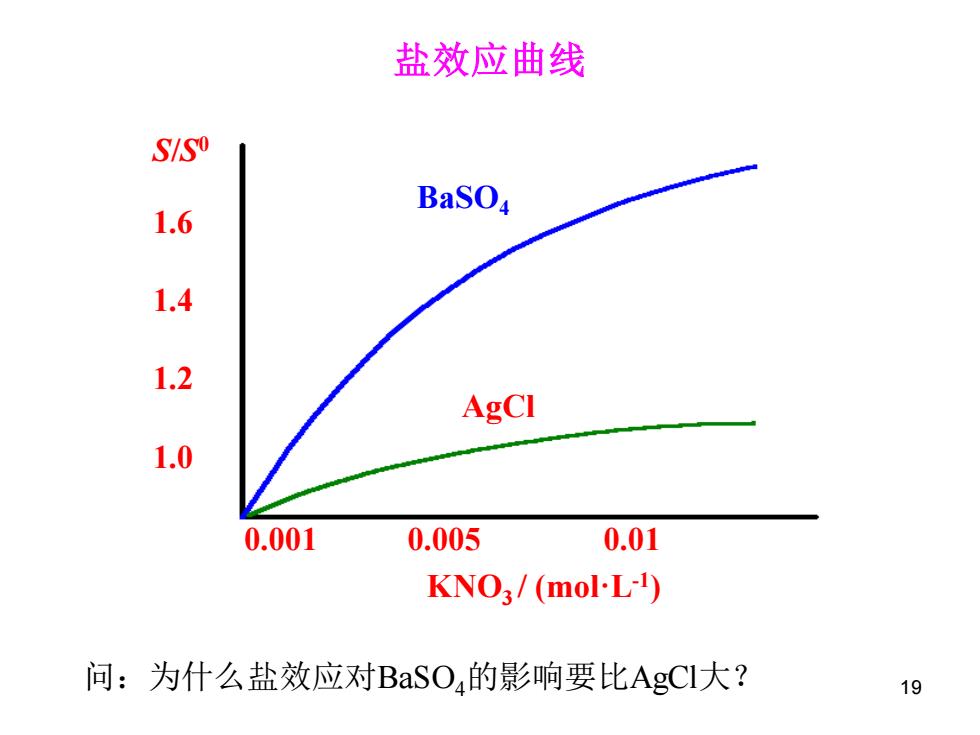
盐效应曲线 S/SO BaSO 1.6 1.4 1.2 AgCl 1.0 0.001 0.005 0.01 KNO3/(mol-L-1) 问:为什么盐效应对BaSO4的影响要比AgCI大? 19
盐效应曲线 S/S 0 1.6 1.4 1.2 1.0 0.001 0.005 0.01 KNO3 / (mol·L-1 ) BaSO4 AgCl 问:为什么盐效应对BaSO4的影响要比AgCl大? 19

例:计算BaS0,在0.08 mol/LMgCl2溶液中的溶解度 解: 己知P(BaS0,)=1.1×10-10 1-∑C7Cg×2+C。xr+C2+Cw2) 1 (0.08×22+0.016×12)=0.024mol/L 0 0 Ba2+:a=500S0:a=400,P385,附表4:I=0.025 Yw2≈0.56,Yo≈0.55 K 1.1×10-10 S= SP(BaSO =1.9×10-5mol/L YBa24·Yso V0.56×0.55 20
例: 计算BaSO4在0.08mol/LMgCl2溶液中的溶解度 解: 10 ( ) 1.1 10 4 − 已知KSP BaSO = 2 2 4 0 0 2 2 4 : 500 : 400, 385, 0.56, 0.55 Ba SO Ba a SO a P + − + − = = 附表4:I=0.025 4 2 2 4 0 10 1.1 10 5 1.9 10 / 0.56 0.55 SP BaSO Ba SO K S mol L + − − − = = = ( ) 2 2 2 4 2 2 2 2 2 2 2 1 1 ( 2 1 2 2 ) 2 2 1 (0.08 2 0.016 1 ) 0.24 / 2 i i Mg Cl Ba SO I C Z C C C C mol L = = + + + + − + − + = 20 0.024