
二、亲核取代反应历程: RXN0 R—Nu+X 反应物亲核试剂 产物离去基团 反应速率=碰撞几率 ×取向几率×能量几率 浓度+,几率+ 符合方向的 大于最低活化 T,几率 M+,几率 有效碰撞 能的有效碰撞 1.双分子亲核取代反应(S2一Substitution Nucleo- philic): A.反应机理:以CHBr的碱性水解为例: CH,Br+OH→CHOH+Br =kI CHBr [OH 1
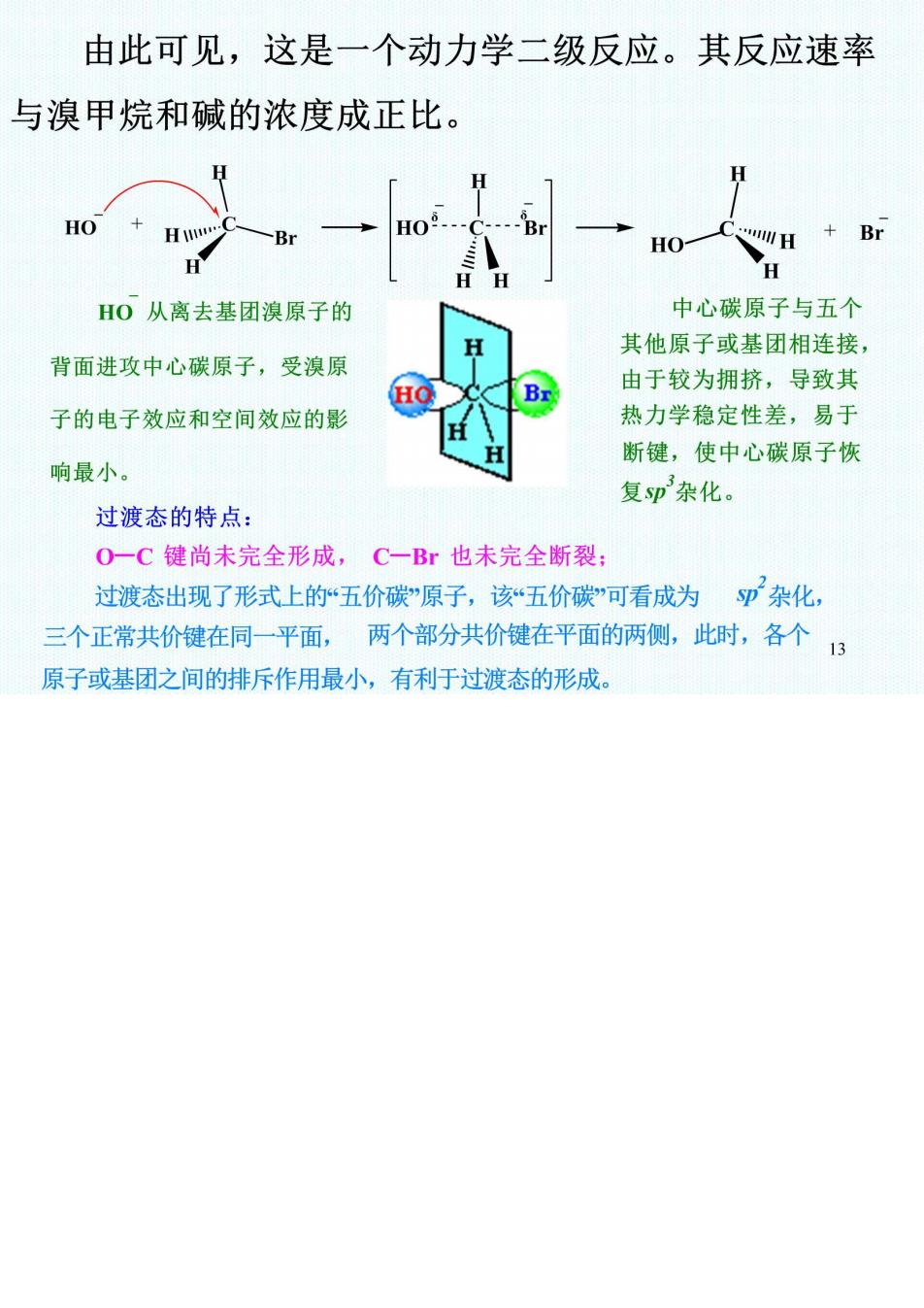
由此可见,这是一个动力学二级反应。其反应速率 与溴甲烷和碱的浓度成正比。 H HO HO H H HO从离去基团溴原子的 中心碳原子与五个 其他原子或基团相连接, 背面进攻中心碳原子,受溴原 HO 由于较为拥挤,导致其 子的电子效应和空间效应的影 热力学稳定性差,易于 断键,使中心碳原子恢 响最小。 复p杂化。 过渡态的特点: O一C键尚未完全形成,C一Br也未完全断裂: 过渡态出现了形式上的五价碳”原子,该“五价碳”可看成为p杂化, 三个正常共价键在同一平面,两个部分共价健在平面的两侧,此时,各个13 原子或基团之间的排斥作用最小,有利于过渡态的形成
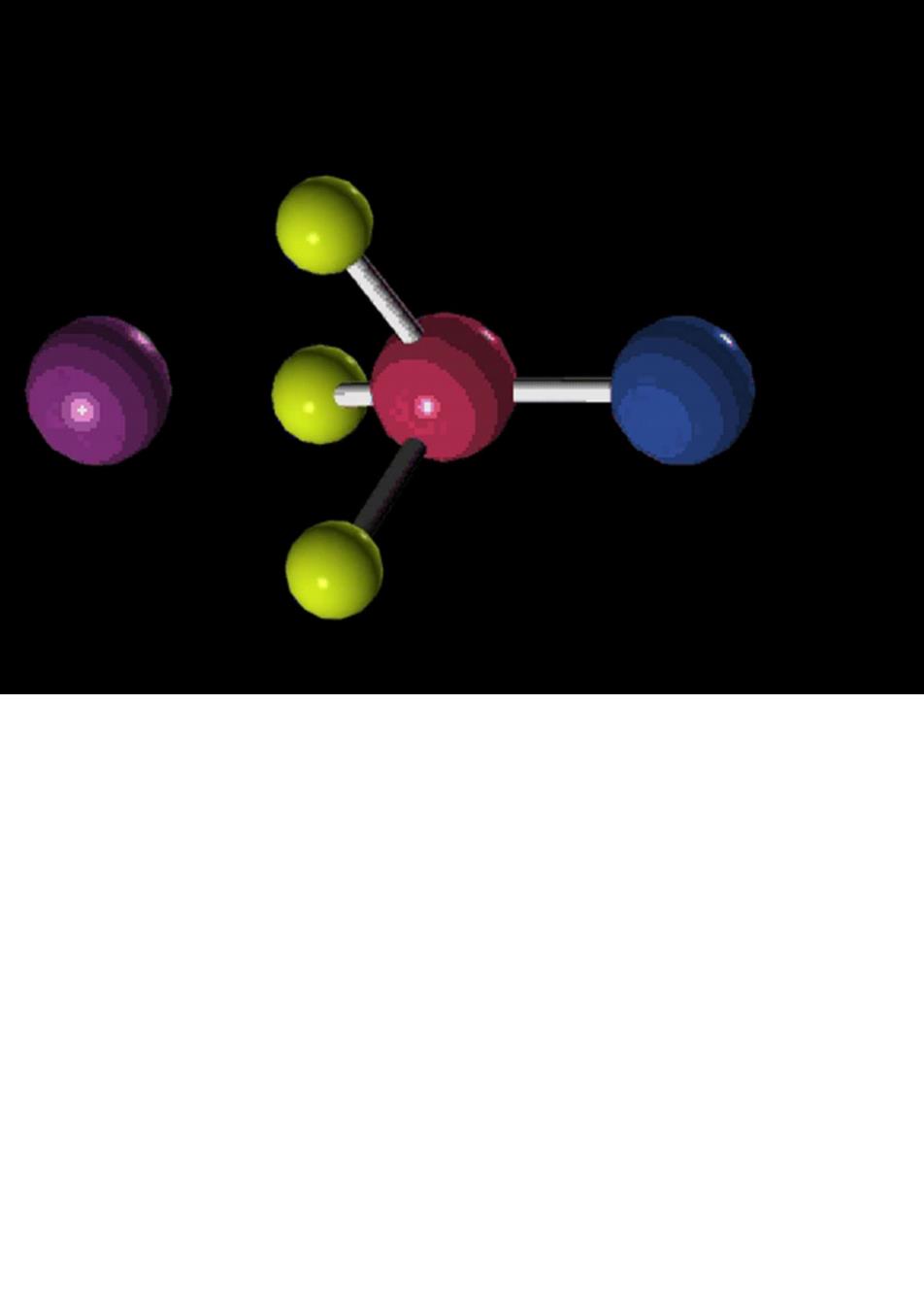
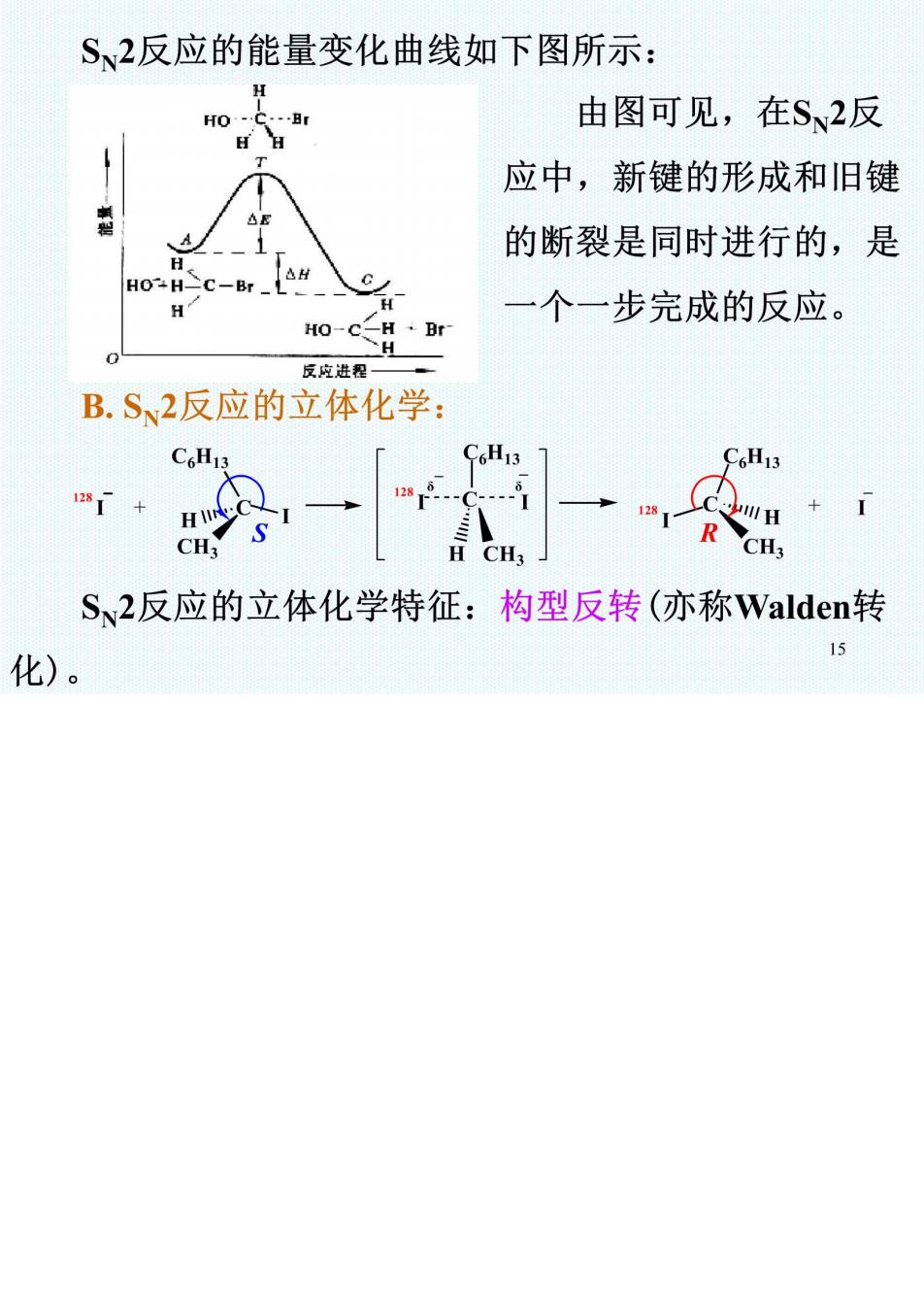
S、2反应的能量变化曲线如下图所示: HO- 由图可见,在S2反 应中,新键的形成和旧键 的断裂是同时进行的,是 一个一步完成的反应。 HO-CH Br 反吃进程 B.S2反应的立体化学: C6H13 6113 一一 CH CH Sw2反应的立体化学特征:构型反转(亦称Walden转 15 化)

2.单分子亲核取代反应(S、1): A.反应机理:以(CH)3CBr的碱性水解为例: (CH3)3C-Br OH -(CH3)C-OH Br =k[(CH3)3CBr 由此可见,这是一个动力学一级反应,其反应速率 只于叔丁基溴的浓度有关。 单分子亲核取代反应是分步进行的: 第一步:(CH,C-Br度I(CH,CBF1 →(CH3)3C+Br 过渡状态 中间体 第二步:(CHC+OH快【(CHC2-OH】 →(CH33C-OH 16