
(二)温度对反应速度的影响: 对大多数反应来说,升高溶液的温度 可提高反应速度。例如: 2M04+5C203+16H+—2Mm2++10002◆+8H20 (三)催化剂对反应速度的影响 催化剂是一种能改变反应速度而不影 响反应平衡的物质,虽然它参与反应历程, 但在反应前后,其形态和数量不变。催化剂 有正催化剂和负催化剂之分。 例如:Ce+氧化As,O3(-);MnO4与 C,0,2的反应(Mn2+、自动催化) 16
16 (二)温度对反应速度的影响: 对大多数反应来说,升高溶液的温度 可提高反应速度。例如: (三)催化剂对反应速度的影响 催化剂是一种能改变反应速度而不影 响反应平衡的物质,虽然它参与反应历程, 但在反应前后,其形态和数量不变。催化剂 有正催化剂和负催化剂之分。 例如:Ce4+氧化As2O3(I -);MnO4 -与 C2O4 2-的反应(Mn2+、自动催化)

催化剂的影响 催化剂的使用能显著改变反应的速度。催化剂的作用主要在 于改变反应历程,或降低原来反应的活化能。例: 2Mn0+5C,01+16H+ 7080C→2Mn2++10C02+8H20 慢 C2042 MnV⑩ Mn(III Mn(⑩)(C204)n3-2m Mn (II 快 快 Mn⑩+CO, 如果不外加Mn(山离子,而是利用反应生成的Mn(四离子对 反应进行催化,称作自动催化反应。自催化反应的特点是: 有一个诱导期开始反应慢,随着反应物的生成,反应加快
17 催化剂的影响 催化剂的使用能显著改变反应的速度。催化剂的作用主要在 于改变反应历程,或降低原来反应的活化能。例: 2MnO 5C O 1 6H 2Mn 1 0CO 2 8H 2 O 2 7 0~8 0 C 2 4 + 2 4 + ⎯⎯⎯⎯→ + + − − + + Mn (VII) Mn (III) 慢 Mn (III) (C2O4 )n(3-2n)+ C2O4 2- Mn(II) + CO2 Mn (II) 快 快 如果不外加Mn(II)离子,而是利用反应生成的Mn (II) 离子对 反应进行催化,称作自动催化反应。自催化反应的特点是: 有一个诱导期,开始反应慢,随着反应物的生成,反应加快
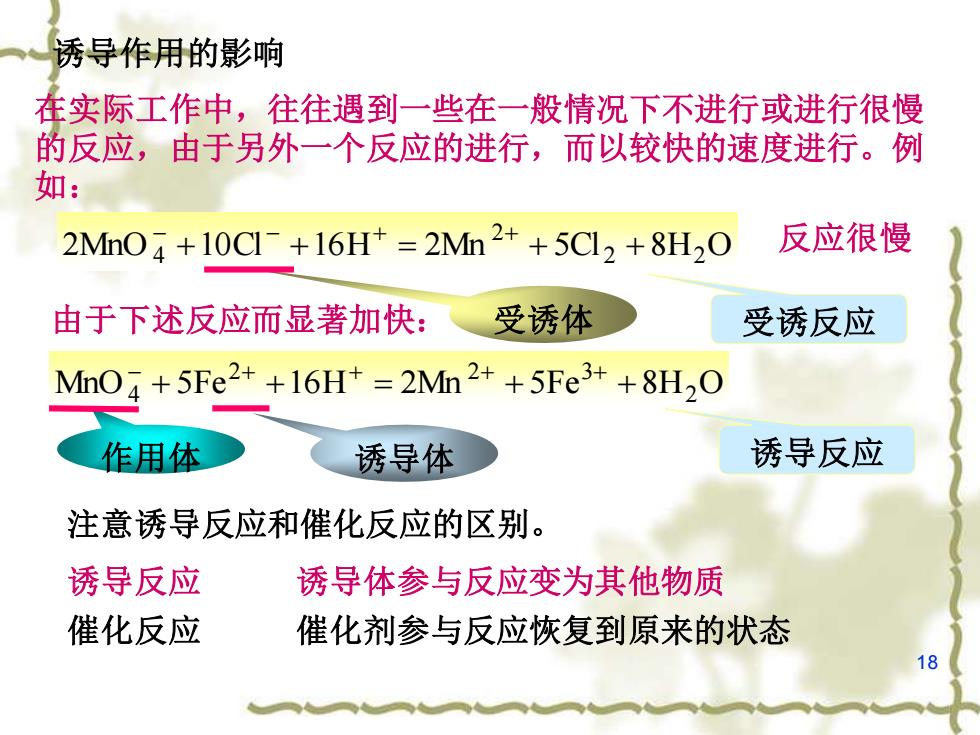
诱导作用的影响 在实际工作中,往往遇到一些在一般情况下不进行或进行很慢 的反应,由于另外一个反应的进行,而以较快的速度进行。例 如: 2Mn04+10C1+16H+=2Mn2++5C12+8H20 反应很慢 由于下述反应而显著加快:、 受诱体 受诱反应 MnO4+5Fe2++16H+=2Mn2++5Fe3++8H,0 作用体 诱导体 诱导反应 注意诱导反应和催化反应的区别。 诱导反应 诱导体参与反应变为其他物质 催化反应 催化剂参与反应恢复到原来的状态 18
18 诱导作用的影响 在实际工作中,往往遇到一些在一般情况下不进行或进行很慢 的反应,由于另外一个反应的进行,而以较快的速度进行。例 如: 2MnO 10Cl 16H 2Mn 5Cl 2 8H2 O 2 4 + + = + + − − + + 反应很慢 由于下述反应而显著加快: MnO 5Fe 16H 2Mn 5Fe 8H2 O 2 2 3 4 + + = + + − + + + + 受诱反应 作用体 诱导体 诱导反应 受诱体 注意诱导反应和催化反应的区别。 诱导反应 诱导体参与反应变为其他物质 催化反应 催化剂参与反应恢复到原来的状态

诱导作用 诱导反应的发生与氧化还原反应中间步骤产生的不稳定中 间价态离子或自由基等因素有关,例如: Mn04+5Fe2++16H+-2Mn2++5Fe3++8H20 生成Mn(VD,Mn(V),Mn(V),Mn(D等中间价态离子, 这些中间价态离子与氯离子作用而诱导以下反应 2Mn04+10CI+16H+=2Mn2++5CL2+8H20 19
19 诱导作用 诱导反应的发生与氧化还原反应中间步骤产生的不稳定中 间价态离子或自由基等因素有关,例如: 2MnO 10Cl 16H 2Mn 5Cl 2 8H2 O 2 4 + + = + + − − + + 生成 Mn (VI), Mn (V), Mn (IV), Mn (III) 等中间价态离子, 这些中间价态离子与氯离子作用而诱导以下反应 MnO 5Fe 16H 2Mn 5Fe 8H2 O 2 2 3 4 + + = + + − + + + +

7.2氧化还原滴定原理 7.2.1氧化还原指示剂 7.2.2氧化还原滴定曲线 7.2.3终点误差 20
20 7.2 氧化还原滴定原理 7.2.1氧化还原指示剂 7.2.2氧化还原滴定曲线 7.2.3终点误差