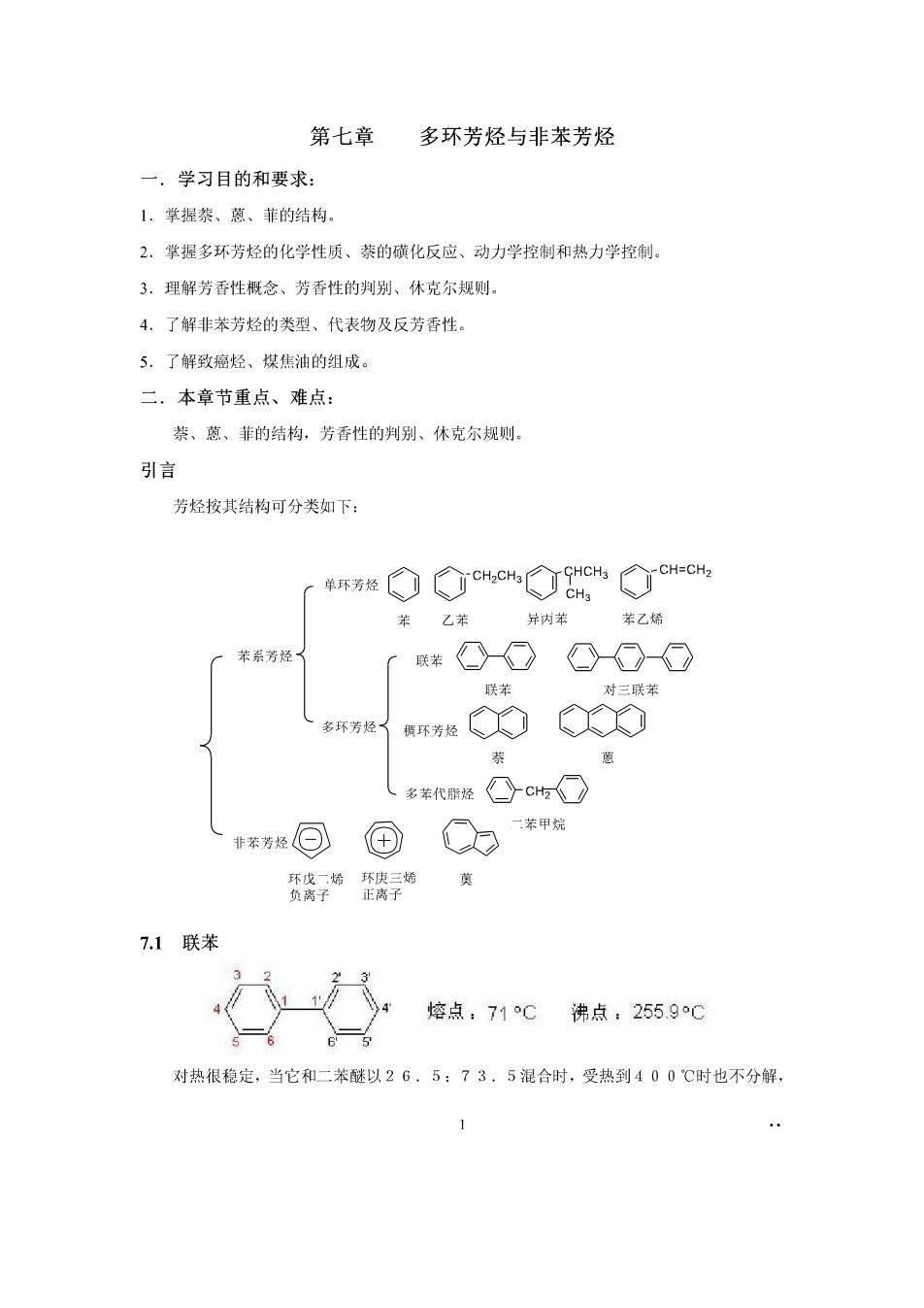
第七章多环芳烃与非苯芳烃 一,学习目的和要求: 1.掌握茶、蒽、菲的结构 2.掌握多环芳烃的化学性质、萘的碳化反应、动力学控制和热力学控制 3.理解芳香性概念、芳香性的判别、休克尔规则。 4.了解非苯芳烃的类型、代表物及反芳香性。 5.了解致癌烃、煤焦油的组成 二,本章节重点、难点: 萘、煎、菲的结构,芳香性的判别、休克尔规则。 引言 芳烃按其结构可分类如下: 「单环芳经①cc8ic今cHno 苯乙苯 异内苯 乙烯 苯系芳烃 联柴①①⊙-OO 联苯 对三联苯 多环芳经了 群OCO (多养代联经①cH○ 华回国Q力*甲 质终子“我导奶黄 7.1联苯 登 垮点,71℃沸点,2559C 对热很稳定,当它和二苯醚以26,5:73,5混合时,受热到400℃时也不分解
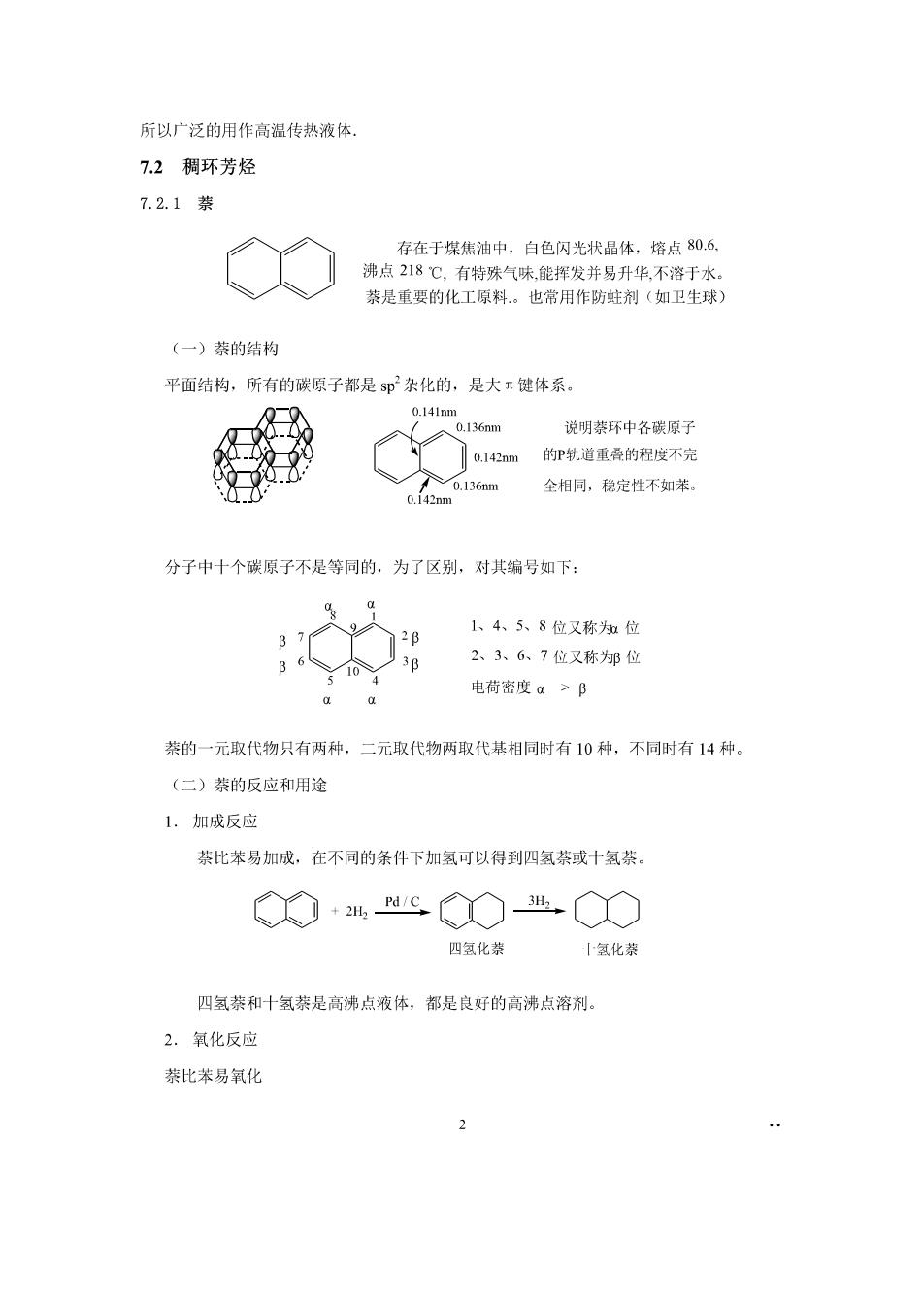
所以广泛的用作高温传热液体 7.2稠环芳烃 7.2.1装 存在于煤焦油中,白色闪光状晶体,熔点80.6, 沸点218℃,有特殊气味能挥发并易丹华,不溶于水 萘是重要的化工原料。也常用作防蛀剂(如卫生球 (一)萘的结构 平面结构,所有的碳原子都是5p杂化的,是大键体系。 0.l41nm136m 说明禁环中各碳原了 Q.142m的P轨道重叠的程度不完 全相同,稳定性不如米 分子中十个碳原子不是等同的,为了区别,对其编号如下: 1、4、5、8位又称知位 B 6 2、3、6、7位又称为邻位 aa 电荷密度a>B 茶的一元取代物只有两种,二元取代物两取代基相同时有10种,不同时有14种。 (二)萘的反应和用途 1.加成反应 萘比苯易加成,在不同的条件下加氢可以得到四氢萘或十氢萘。 ◇+HC◇出○ 四氢化恭 氢化恭 四氢萘和十氢萘是高沸点液体,都是良好的高沸点溶剂。 2.氧化反应 萘比苯易氧化
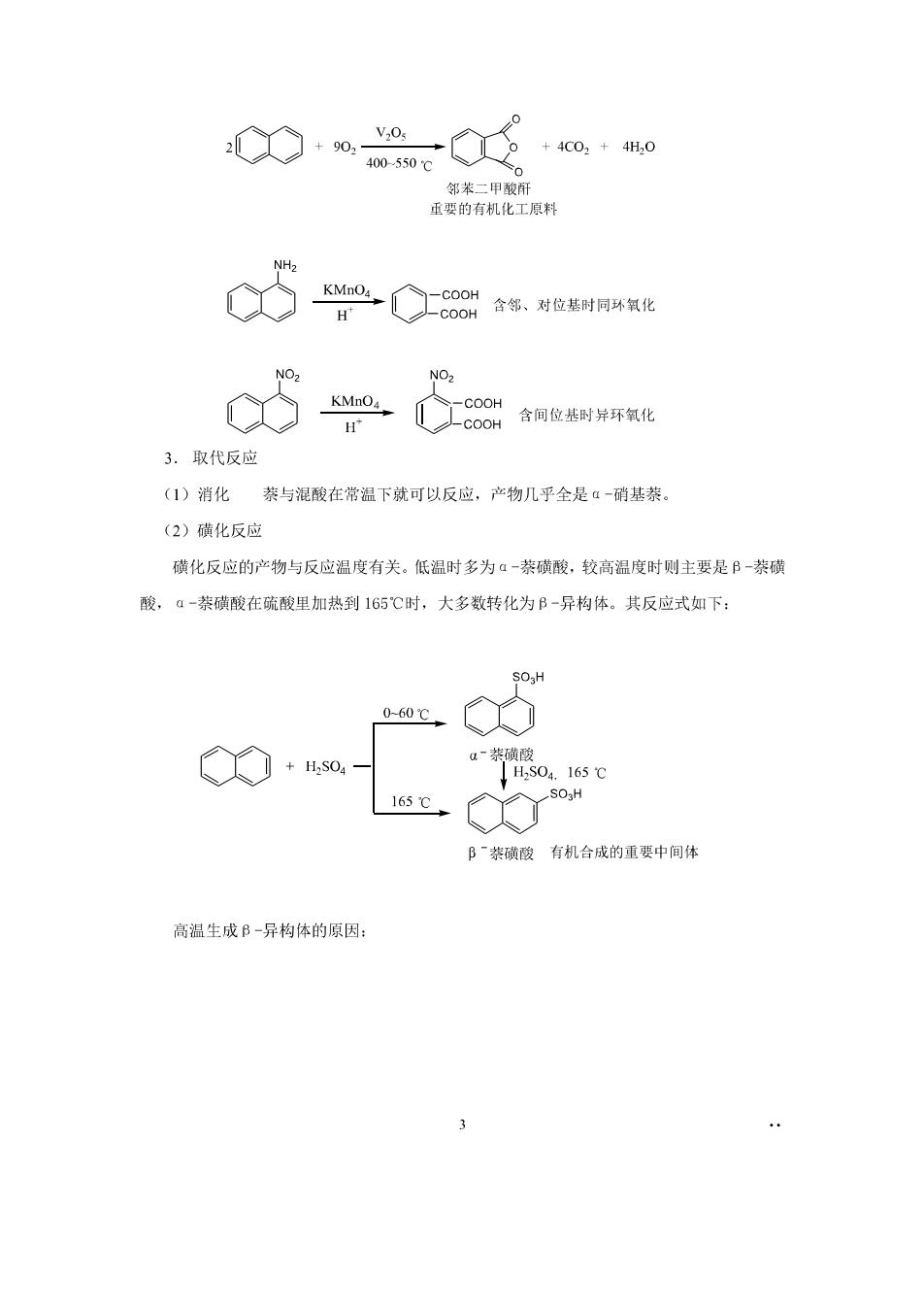
邻苯二甲酸肝 亚要的有机化工原料 c5m= 含间位基时异环氧化 3.取代反应 (1)消化与混酸在常温下就可以反应,产物几乎全是“-硝基 (2)磺化反应 磺化反应的产物与反应温度有关。低温时多为α一茶磺酸,较高温度时则主要是B-茶磷 酸,a-蒸磺酸在疏酸里加热到165℃时,大多数转化为B-异构体。其反应式如下: 0-60℃ +0,- 165℃ Bˉ类磺酸有机台成的重要中间体 高温生成B一异构体的原因: 3

S0H-位没稳定,被认为 是空间斥力的结果 斥力大 斥力小 速度控制产物 E大) 平视产物 为什么磺化反应随着温度不同生成的产物不一样呢?这里就有一个速度控制和平衡控 制的问题。 由于的的4-位比B-位活泼,在低温下,反应活性不是很强的时候,α位优先反应 生成α-萘碳酸,这种利用反应速度来控制主要产物的结果叫做速度控制.以前我们讨论苯 环的定位基效应大多是速度控制产物, 当温度升高,逆反应速度加快,产物由平衡控制:同时由于温度升高,对反应活化能 较高的B取代的反应速度也加快,加速了B取代产物的生成,当加热到160℃时,大部分☑ 异构体转变成B异构体,反应达到了平衡,所以,B萘磺酸是平衡控制产物. 两种竞争反应进程曲线图如下: +H,S0 B-茶磺酸 从曲线上我们看到,B茶磺酸比α茶磺酸更稳定,为什么呢? 8an α位活泼,反应快,但位阻大,不稳定,容易脱去:
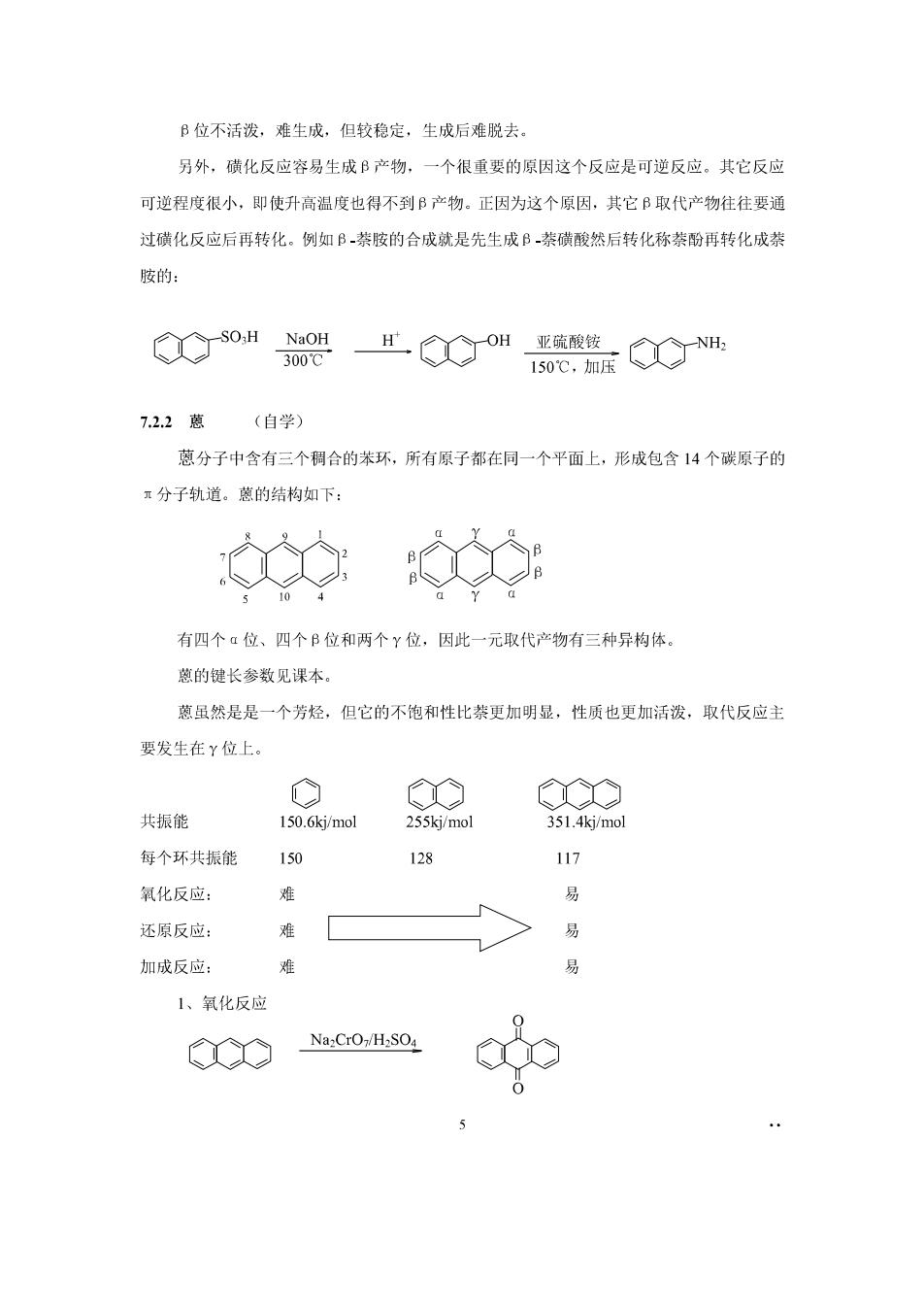
B位不活泼,难生成,但较稳定,生成后难脱去。 另外,磺化反应容易生成B产物,一个很重要的原因这个反应是可逆反应。其它反应 可逆程度很小,即使升高温度也得不到B产物。正因为这个原因,其它B取代产物往往要通 过磷化反应后再转化。例如B,茶胺的合成就是先生成B茶磺酸然后转化称萘酚再转化成茶 胺的: o州架O"0 7.22葱(自学) 蒽分子中含有三个稠合的苯环,所有原子都在同一个平面上,形成包含14个碳原子的 x分子轨道。的结构如下: 有四个a位、四个B位和两个Y位,因此一元取代产物有三种异构体 慈的键长参敌见课本, 慈虽然是是一个芳烃,但它的不饱和性比装更加明显,性质也更加活泼,取代反应主 要发生在Y位上 共振能 150.6kj/mol 255kj/mol 351.4kj/mol 每个环共振能 117 氧化反应: 难 易 还原反应: 易 加成反应: 1、氧化反应 C Na2CrO:/H:SO4