
第五章生物体内污染物质的运动过程及毒性 第四节污染物质的生物转化 教学目的与要求: 了解无机物污染物的微生物转化速率 掌握重金属污染物的微生物转化。 教学重点、难点: 化 教学方法:讲授法: 师生互动设计:提问:重金属污染物有哪些? 课堂练习、作业: 分别写出重金属汞、砷的微生物转化途径 本次课教学内容小结: 在学习这堂课之前,接触到重金属的微生物转化,这里又进一步学习,其目的是为了更深一层次 了解到重金属在土壤中是如何迁移转化的。这加深了同学们对知识结构的理解和掌握。 重金属元素的微生物转化 Hg(Mercury) (1)在环境中的形态:无机汞、有机汞 (2)毒性:有机汞>金属汞>无机汞 汞的生物甲基化 在好氧或厌氧条件下,水体底质中某些微生物能使二价无机汞盐转变为甲基汞和二甲基汞的过程 涉及的酶:甲基钴氨素(甲基维生素B12) 甲基钴复素: 汞的生物甲基化机理:
第五章 生物体内污染物质的运动过程及毒性 第四节 污染物质的生物转化 教学目的与要求: (1) 了解无机物污染物的微生物转化速率; (2) 掌握重金属污染物的微生物转化。 教学重点、难点: (1) 重金属污染物的微生物转化。 教学方法及师生互动设计: 教学方法:讲授法; 师生互动设计:提问:重金属污染物有哪些? 课堂练习、作业: 分别写出重金属汞、砷的微生物转化途径。 本次课教学内容小结: 在学习这堂课之前,接触到重金属的微生物转化,这里又进一步学习,其目的是为了更深一层次 了解到重金属在土壤中是如何迁移转化的。这加深了同学 们对知识结构的理解和掌握。 三、重金属元素的微生物转化 1、 Hg (Mercury) (1) 在环境中的形态:无机汞、有机汞 (2) 毒性:有机汞 > 金属汞 > 无机汞 汞的生物甲基化 在好氧或厌氧条件下,水体底质中某些微生物能使二价无机汞盐转变为甲基汞和二甲基汞的过程. 涉及的酶: 甲基钴氨素(甲基维生素B12) 甲基钴氨素: 汞的生物甲基化机理:
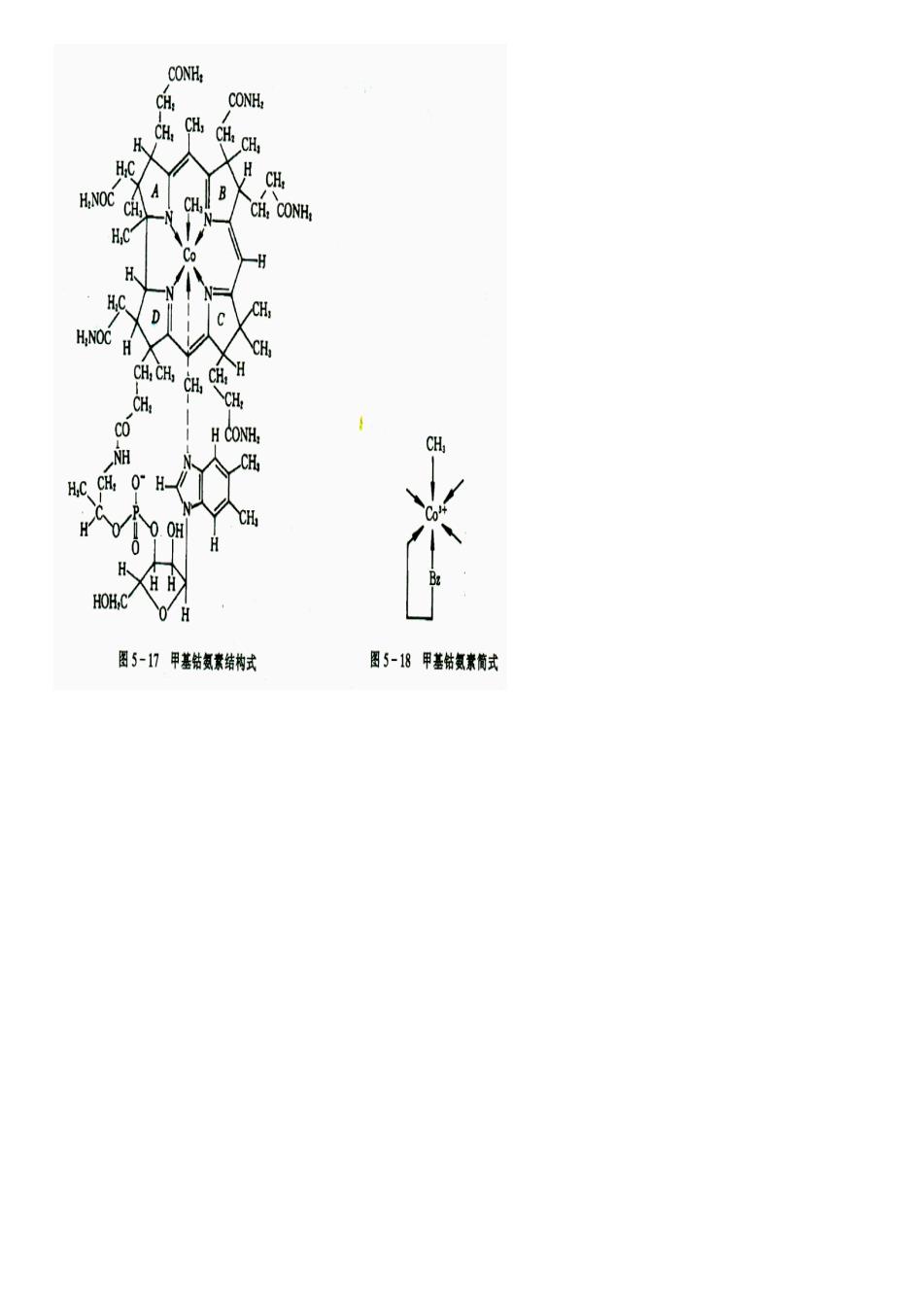
CONH HNOC CH CH.CONH. H.C 图5-7甲基给氮素结构式 图5-18甲基特氨素榄式
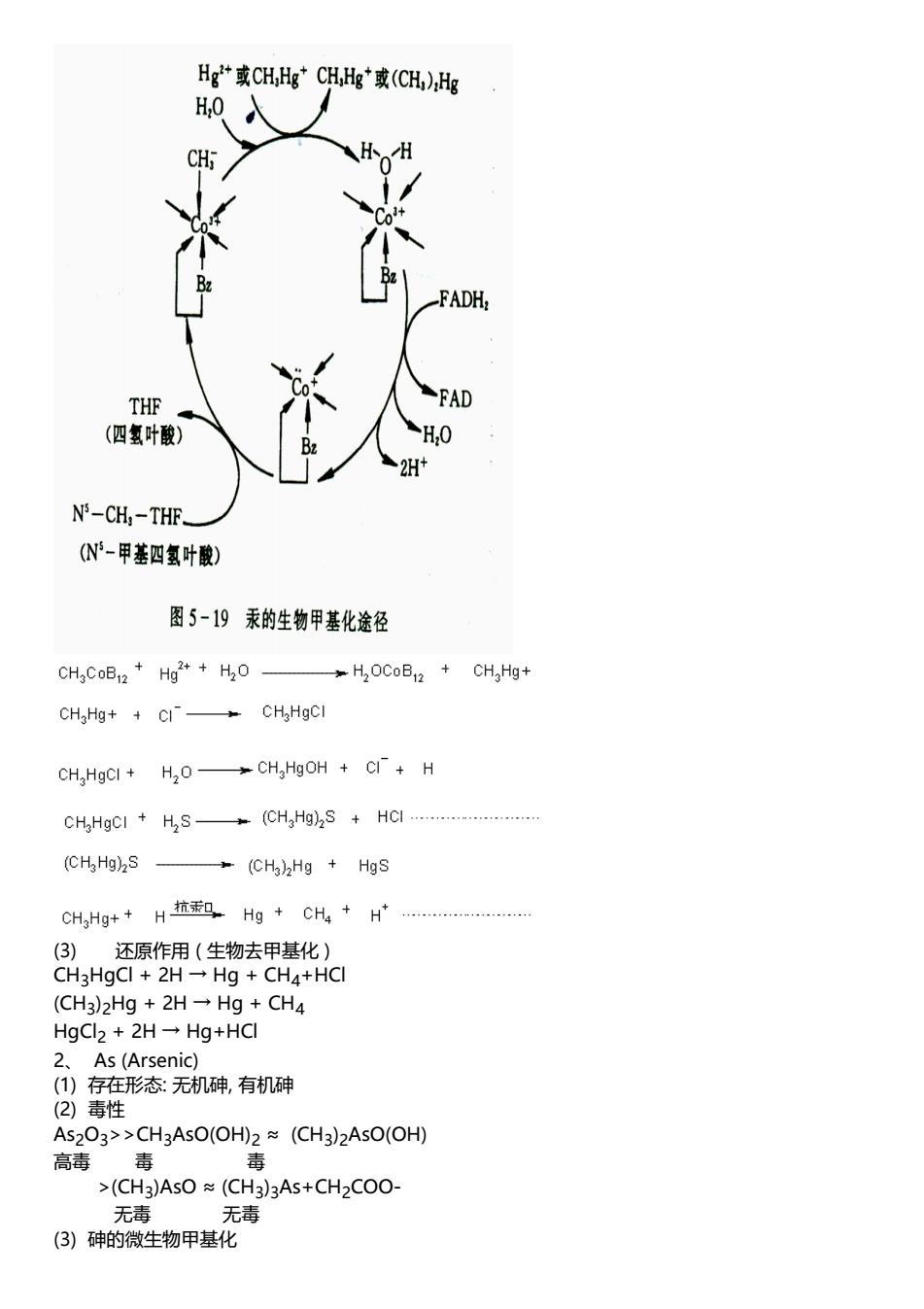
Hg*或CH,Hg"CH,,Hg或(CH)Hg H,0人 -FADH, FAD (四氢叶酸) ,0 2H+ N'-CH,-THF. (N-甲基四氢叶酸) 图5-19汞的生物甲基化途径 CHaCoB2 Hg2*H2O HOCoB:2 CH,Hg+ CHgHg+CI CHgHgCl CH HgCI H20 →CH,HgOH+C+H CHaHgCI HS(CHgHg)S HCI (CHHg)2S (CH)Hg HgS CH,Hg+H拉Hg+CH+H (3) 还原作用(生物去甲基化) CH3HgCl 2H-Hg CH4+HCI (CH3)2Hg+2H→Hg+CH4 HgCl2+2H一Hg+HCI 2、As(Arsenic) ()存在形态无机碑有机碑 (2)毒性 As203>>CH3AsO(OH)2(CH3)2AsO(OH) 高毒 香 >(CH3)AsO (CH3)3As+CH2COO- 无毒 无毒 (3)砷的微生物甲基化
(3) 还原作用 ( 生物去甲基化 ) CH3HɡCl + 2H → Hɡ + CH4+HCl (CH3 )2Hɡ + 2H → Hɡ + CH4 HɡCl2 + 2H → Hɡ+HCl 2、 As (Arsenic) (1) 存在形态: 无机砷, 有机砷 (2) 毒性 As2O3>>CH3AsO(OH)2 ≈ (CH3 )2AsO(OH) 高毒 毒 毒 >(CH3 )AsO ≈ (CH3 )3As+CH2COO- 无毒 无毒 (3) 砷的微生物甲基化

B4sQ254sg时CHAsCO励22 CHAO2时 (CHAsCO2CH)AdOCH)AsO 2CH)As (4)去甲基作用 三价与五价之间的转化: HAs02 CHaAsH 生物深百 CHa (OH) OH AR3 A50 CH2 (CH (CH)3AsO -0 1 3、硒(Selenium) 关键词: 人类所需,浓度范围,亚硒酸及其盐和酯 硒的甲基化(真菌)途径 H2SeO3 SeO(OH)- CH3SeOH (CH3)2SeO (CH3)2Se 4.铁(ron 亚铁杆菌催化: 4Fe(I)+4H++02=4Fe(四)+2H20+能量 酸性矿水的形成: 1、黄铁矿的氧化 2FeS2(S)+2H20+702=4H++4s042-+2Fe2+ 2、Fe2+氧化成Fe3+ 4Fe2++02+4H+=4Fe3++2H20 3、进一步氧化黄铁矿: FeS2(S)+14Fe3++8H20=15Fe2++2S042+16Ht 以上溶解FeS2的循环,生成大量H2SO4,形成酸性矿水。 酸性矿水的防治 CaC03(S+2H+=Ca2++H20+C02 四、污染物质的生物转化速率 生物转化速率有两个方面的内容:一是微生物体外的酶促反应速率,另一个是微生物本身对生物转 化速率的贡献。 1、酶促反应的速率 E+S =ES =E+P v=vmax[S]/(KM+[S]) (1) 米氏方程 (2) 影响酶促反应速率的因素 抑制剂 2、微生物反应的速率
(4) 去甲基作用 三价与五价之间的转化: 3、硒 (Selenium) 关键词: 人类所需,浓度范围,亚硒酸及其盐和酯 硒的甲基化(真菌)途径: H2SeO3 SeO(OH)- CH3SeOH (CH3 )2SeO (CH3 )2Se 4、铁 (Iron) 亚铁杆菌催化: 4Fe(Ⅱ)+4H+ +O2 =4Fe(Ⅲ)+2H2O+能量 酸性矿水的形成: 1、黄铁矿的氧化: 2FeS2 (S)+2H2O+7O2 =4H++4SO4 2-+2Fe 2+ 2、Fe 2+氧化成Fe 3+ : 4Fe 2+ +O2+4H+ =4Fe 3+ +2H2O 3、进一步氧化黄铁矿: FeS2 (S)+14 Fe 3+ +8H2O = 15Fe 2+ +2SO4 2- +16H+ 以上溶解FeS2的循环,生成大量H2SO4,形成酸性矿水。 酸性矿水的防治: CaCO3 (S)+2H+ =Ca 2+ +H2O+CO2 四、污染物质的生物转化速率 生物转化速率有两个方面的内容:一是微生物体外的酶促反应速率,另一个是微生物本身对生物转 化速率的贡献。 1、 酶促反应的速率 E + S = ES = E + P v=vmax[S]/(KM+[S]) (1) 米氏方程 (2) 影响酶促反应速率的因素 酸度 温度 抑制剂 2、 微生物反应的速率

(1)微生物反应的速率方程 (2) 影外响反映谏率的因寿 化学结构 链长规律:脂肪酸、脂族碳氢化合物和烷基苯等,在一定范围内碳链越长,降解越快,有机聚合物 随分子增大降解减慢。 链分支规律:烷基苯磺酸盐、烷基化合物(RnCH4-n)等有机物质中,烷基支链越多,分支程度越 大,降解也越慢的现象。 取代规律:羟基、羧基、氨基等取代基存在会加快降解,而硝基、磺酸基、氯基等取代基的存在则 使降解速度变慢 氯苯>二氯苯>三氯苯,随取代基增加,速率变慢;苯酚的一氯取代物中,邻、 对位的降解比间位的快。 微生物体内的酶 共代谢 2 环境条件: 温度 酸度 养分 溶解氧 共存物质等 第五节污染物的毒性 教学目的与要求 1) 了解污染物的毒性 (2) 了解毒物的联合作用: (3)掌握毒物的生物化学机制。 教学重点、难点: 毒物的生物化学机制 教学方法及师生互动设计 教学方法:讲授法; 师生互动设计:提问:有毒污染污染物质有哪些? 讨论:有毒污染物质对人体健康的危害有哪些? 课堂练习、作业 谈谈有毒污染物质对人体健康的危害作用。 本次课教学内容小结: 学习环境化学的目的,不只是为了清楚地了解周围的环境,更重要的要知道哪些污染物质对人体 是有害的, 应该如何消除 这就是本堂可所要学习的目的 毒物 毒物的概念 2 毒物的相对性 毒物的作用部位 刺激性 腐蚀性 室息性、致突变、致癌、致畸、致敏 毒物的毒性 1 影响毒性的因素 2 毒物的剂量 半数有效剂量 半数有效浓 三、毒物的联合作用 1、协同作用
(1) 微生物反应的速率方程 (2) 影响反映速率的因素 1、 化学结构 链长规律:脂肪酸、脂族碳氢化合物和烷基苯等,在一定范围内碳链越长,降解越快,有机聚合物 随分子增大降解减慢。 链分支规律:烷基苯磺酸盐、烷基化合物(RnCH4-n)等有机物质中,烷基支链越多,分支程度越 大,降解也越慢的现象。 取代规律:羟基、羧基、氨基等取代基存在会加快降解,而硝基、磺酸基、氯基等取代基的存在则 使降解速度变慢;一氯苯>二氯苯>三氯苯,随取代基增加,速率变慢;苯酚的一氯取代物中,邻、 对位的降解比间位的快。 微生物体内的酶 共代谢 2、环境条件: 温度 酸度 养分 溶解氧 共存物质等 第五节 污染物的毒性 教学目的与要求: (1) 了解污染物的毒性; (2) 了解毒物的联合作用; (3) 掌握毒物的生物化学机制。 教学重点、难点: 毒物的生物化学机制。 教学方法及师生互动设计: 教学方法:讲授法; 师生互动设计:提问:有毒污染污染物质有哪些? 讨论:有毒污染物质对人体健康的危害有哪些? 课堂练习、作业: 谈谈有毒污染物质对人体健康的危害作用。 本次课教学内容小结: 学习环境化学的目的,不只是为了清楚地了解周围的环境,更重要的要知道哪些污染物质对人体 是有害的,应该如何消除,这就是本堂可所要学习的目的。 一、毒物 1、 毒物的概念 2、 毒物的相对性 3、 毒物的作用部位 4、 刺激性、腐蚀性、窒息性、致突变、致癌、致畸、致敏 二、毒物的毒性 1、 影响毒性的因素 2、 毒物的剂量 半数有效剂量 半数有效浓度 三、毒物的联合作用 1、 协同作用