
有机化学教案 第三章】 第三章烯烃 一、学习目的和要求 1. 掌握烯烃的构造异构和命名 2.掌握烯烃的结构。 3.掌握烯烃结构的Z/E标记法和次序规侧。 4.掌握烯烃的来源和制法。 5。掌握烯烃的物理性质。 6,掌握烯烃的化学性质:催化氢化、亲电加成,马尔柯夫尼柯夫规则,硼氢化-氧化 反应、臭氧化反应。 7.了解烯烃的重要代表物:乙烯、丙烯和丁烯 二。本章节重点、难点 烯烃的分子结构、Π键的特点、。键与口键的区别、Z/E标定法、记住次序规则、碳正离 子的结构及其稳定性、亲电加成的反应历程和影响因素、乙烯的分子轨道、丙稀的游离基反 应、马氏与反马氏规则。 三.教学内容 烯烃是指分子中含有一个碳碳双键的开链不饱和烃,烯烃双键通过SP杂化轨道成键。 因此和烷烃相比,相同碳原子的烯烃比烷烃少两个碳原子,通式为C2n。 3.1烯烃的构造异构和命名 3.1.1烯烃的同分异构 烯烃的同分异构现象比烷烃的要复杂,除碳链异构外,还有由于双键的位置不同引起的 位置异构和双键两侧的基团在空间的位置不同引起的顺反异构,造异构(以四个碳的烯烃 为例): CH,-CH-CH-CH 1-丁烯 位置异构 CH-CH-CH-CH 2-丁烯 构造异构 CHs-C(CH)=CH 2-甲基丙烯 碳链异构

3.1.2烯烃的命名 (1)烯烃系统命名法 烯烃系统命名法,基本和烷烃的相似。其要点是: 1)选择含碳碳双键的最长碳链为主链,称为某烯 2)从最靠近双键的一端开始,将主链碳原子依次编号。 3)将双键的位置标明在烯烃名称的前面(只写出双键碳原子中位次较小的一个) 1)其它同烷烃的命名原则。 例如:C一C一C-C的名称是3-甲基-1-丁烯 CH. 烯烃去掉一个氢原子后剩下的一价基团就是烯基,常见的烯基有: CH2-CH- 乙烯基 CH.CH-CH- 丙烯基(1-丙烯基) CH:=CH-CH:- 烯丙基(2丙烯基) CH2-C- CH3 异丙烯基 3.2烯烃的结构 最简单的烯烃是乙烯,我们以乙烯为例来讨论烯烃双键的结构。 3.2.1双键的结构 乙烯与丙烯的共价键参数如下: 121.7 H 117( H 0.133nm >C-C<键能为61OKJ/mol,C-C键能为316XJ/mol,由键能看出碳碳双键的键 能不是碳碳单健的两倍,说明碳碳双键不是由两个碳碳单键构成的。事实证明碳碳双键是由 一个。键和一个云键构成的。现代物理方法证明:乙烯分之的所有原子在同一平面上。 2
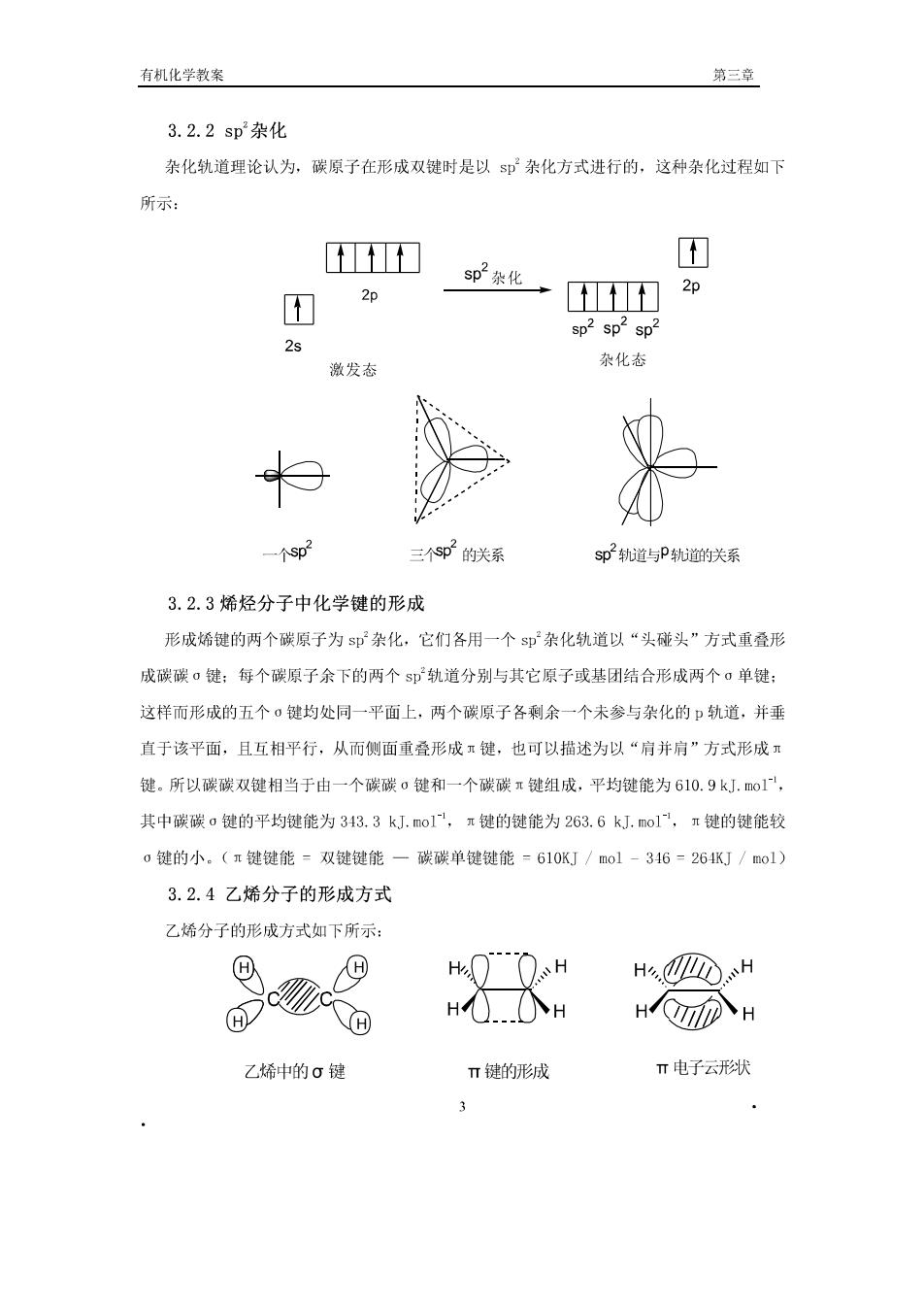
有机化学教案 第三章】 3.2.2sp杂化 杂化轨道理论认为,碳原子在形成双键时是以s即杂化方式进行的,这种杂化过程如下 所示 D T 团 2p p款化,] 2p sp2sp2 sp2 2s 激发态 杂化态 个sp2 三个02的关系 sp2轨道与P轨道的关系 3.2.3烯烃分子中化学键的形成 形成烯键的两个碳原子为即杂化,它们各用一个s即杂化轨道以“头碰头”方式重叠形 成碳碳。键:每个碳原子余下的两个$即轨道分别与其它原子或基团结合形成两个▣单键: 这样而形成的五个·键均处同一平面上,两个碳原子各剩余一个未参与杂化的口轨道,并垂 直于该平面,且互相平行,从而侧面重叠形成键,也可以捐述为以“肩并肩”方式形成 键。所以碳碳双键相当于由一个碳碳o键和一个碳碳π键组成,平均键能为610.9kJ.o1。 其中碳碳o键的平均键能为343.3kJ.o1,π键的键能为263.6k.mo1,π键的键能较 o键的小.(π键键能-双键键能一碳碳单键键能-610KJ/ol-346-26KJ/o1) 3.2.4乙烯分子的形成方式 乙烯分子的形成方式如下所示: HH Hi.OH HIOTIIDH 乙烯的σ键 T键的形成 π电子云形状 3

3.2.5π键的特点 与0键相比,1键与0键有明显区别,由此决定了烯烃的化学性质,1键的特点如下: (1)五键以“肩并肩”方式重叠,碳碳之间的连线还是不是轴对称,因此以双键相连的 两个原子之间不能再以碳碳之间连线为轴自由旋转,如果吸收一定的能量,克服p轨道的结 合力,才能围绕碳碳之间连线旋转,结果使π键破坏。 (2)π键由两个p轨道侧面承叠而成,重叠程度比一般0键小,键能小,不如0键牢固, 容易发生反应 (3)π键电子云不是集中在两个原子核之间,而是分布在上下两侧,原子核对严电子的 束缚力较小,因此电子有较大的流动性,在外界试剂电场的诱导下,电子云变形,导致π 键被破坏而发生化学反应。 ()键不能独立存在,只能与键共存 3.2.6顺反异构 由于双键不能自由旋转,而双键碳上所连接的四个原子或原子闭是处在同一平面的,当 双键的两个碳原子各连接两个不同的原子或原子团时,就能产生顺反异构体。 例如:H ne ese cn 顺丁烯) 立体异构体,构型异构 顺反异构体】 H 反丁婉 bp0.88( 这种由于组成双键的两个碳原子上连接的基团在空间的位置不同而形成的构型不同的 现象称为顺反异构相现象。 构成双键的任何一个碳原子上所连的两个基团要不同是产生顺反异构体的必要条件 如下图所示: 有派反异构的类型 无哌反异构的类型

有机化学教案 第三章】 顺反异构体的命名可在系统名称前加一“顺”或“反”字,例如: CHCH C-CH.C 顺2-戊烯 反3甲基3己烤 但顺反命名法有局限性,即在两个双键碳上所连接的两个基团彼此应有一个是相同的, 彼此无相同基团时,则无法命名其顺反, 例如 =CH.CH.CHcu。C=CCH3 为解决顺反命名法的局限性,IUPC规定,用Z、E命名法来标记顺反异构体的构型。 3.3E一2命名法 3.3.1次序规则 顺序规则的要点: (1)比较与双键碳原子直接连接的原子的原子序数,按大的在前、小的在后排列。 例如: I>Br CI S P F O N C D H -Br>-0H>-N2>-CH3>H (2)如果与双键碳原子直接连接的基团的第一个原子相同时,则要依次比较第二、第 三顺序原子的原子序数,米决定基团的大小顺序。 例如:CHCH〉CH-(因第一顺序原子均为C,故必须比较与碳相连基团的大小) 中与碳相连的是C(H、H、D CH,CH中与碳相连的是C(C、H、HD所以CH,CH-优先。 同理:(CH):C->CHCH(CH)CH>(CH):CHCH->CH.CH.CH.CH (3)当取代基为不饱和基团时,则把双键、三键原子看成是它与多个某原子相连。 例如: cH-相当于8g8- >0酯于火 3.3.2E-7命名法 Z、E命名法的具体内容是:一个化合物的构型是乙型还是E型,要由“次序规则”来决