
.依据物料平衡和电荷平衡写质子条件式 C mol/mL的NaHCO3的质子条件式 物料平衡式[Na]=C [H2C03]+[HC03]+[C032]=C(1) 电荷平衡式Na]+[H+]=[HCO3]+2[CO32] +[OH] (2) 将(1)式带入(2)式 质子条件式[H+]+[H2CO]=[CO32]+[OH1 ①6
26 C mol/mL的NaHCO3的质子条件式 物料平衡式 [Na+] = C [H2CO3 ] + [HCO3 -] + [CO3 2-]= C (1) 电荷平衡式 [Na+] + [H +] = [HCO3 -] +2 [CO3 2-] + [OH-] (2) 将(1)式带入(2)式 质子条件式 [H +] + [H2CO3 ] = [CO3 2-] + [OH-] 2.依据物料平衡和电荷平衡写质子条件式

§5.2酸碱平衡体系中各种型体的分布 酸碱溶液分布分数的计算 1、分布分数的定义: 酸碱以某一形式(型体)存在的平衡浓度 与其分析浓度的比值。又称分布系数。用δ: 表示。 心=某一型体] 27
27 §5.2 酸碱平衡体系中各种型体的分布 酸碱溶液分布分数的计算 1、分布分数的定义: 酸碱以某一形式(型体)存在的平衡浓度 与其分析浓度的比值。又称分布系数。用δi 表示。 c [某一型体] i

2、 δ的计算公式: (以一元弱酸为例) [HAc] [HAc] [H1 δHAC [HAc]+[Ac H]+K。 [Ac-] K [HAc]+[Ac [H"]+Ka ⊙iIAe+OA。=1 >某组分的分布系数,决定于该酸碱物质的性 质和溶液中H+的浓度,而与总浓度c无关。 28
28 c [HAc] HAc [HAc] [Ac ] [HAc] Ka [H ] [H ] c [Ac ] Ac [HAc] [Ac ] [Ac ] a a [H ] K K 2、 δi 的计算公式:(以一元弱酸为例) 1 HA Ac c Ø某组分的分布系数,决定于该酸碱物质的性 质和溶液中H+的浓度,而与总浓度c无关
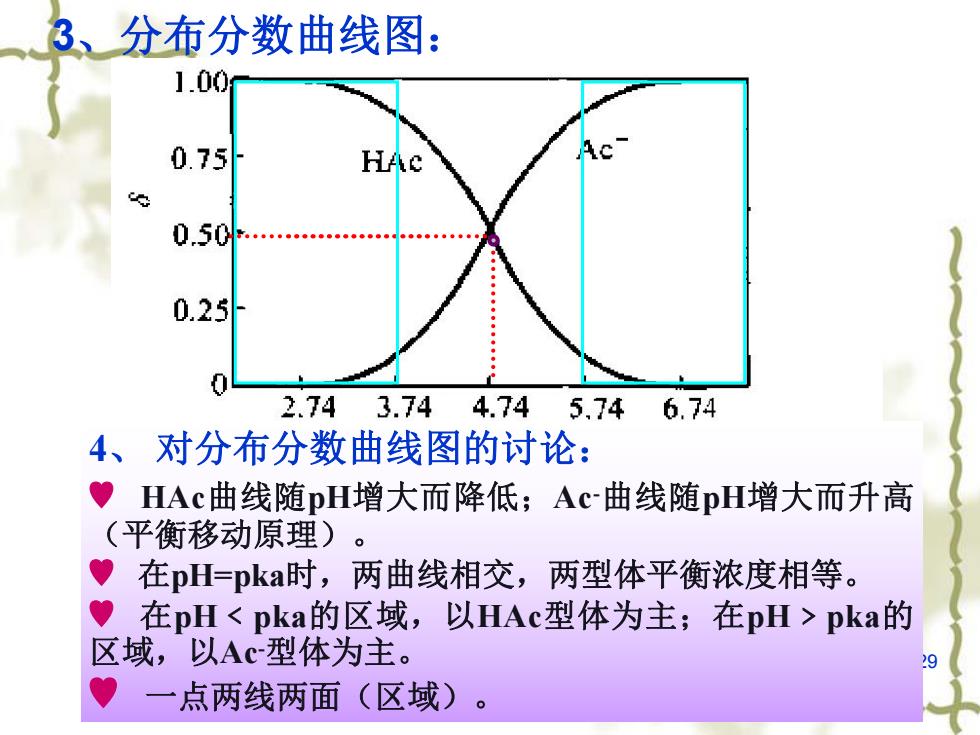
3、分布分数曲线图: 1.00 0.75 0.50. 0.25 2.74 3.74 4.74 5.74 6.74 4、对分布分数曲线图的讨论: HAc曲线随pH增大而降低; Ac曲线随pH增大而升高 (平衡移动原理)。 在pH=pka时,两曲线相交,两型体平衡浓度相等。 曾 在pH<pka的区域,以HAc型体为主;在pH>pka的 区域,以Ac型体为主。 一点两线两面(区域)
29 3、分布分数曲线图: 4、 对分布分数曲线图的讨论: ♥ HAc曲线随pH增大而降低;Ac -曲线随pH增大而升高 (平衡移动原理)。 ♥ 在pH=pka时,两曲线相交,两型体平衡浓度相等。 ♥ 在pH﹤pka的区域,以HAc型体为主;在pH﹥pka的 区域,以Ac -型体为主。 ♥ 一点两线两面(区域)

4对分布分数曲线图的讨论: 影响分布分数的因素有二:一是酸碱的本性Ka, 二是溶液的酸度pH。 ”对给定的弱酸碱,分布分数仅是溶液酸度的函数, 与总浓度无关。 平衡浓度的求算:pH→δ,→ δ与总浓度c无关,而]则与总浓度c有关 30
30 4、对分布分数曲线图的讨论: ♥ 影响分布分数的因素有二:一是酸碱的本性pKa, 二是溶液的酸度pH。 ♥ 对给定的弱酸碱,分布分数仅是溶液 的函数, 与总浓度无关。 ♥ 平衡浓度的求算:pH→ δi →[ ] δi与总浓度c无关,而[ ]则与总浓度c有关 c