
关于PBE的书写规则 1.零水准法 (质子参考水准) 零水准物质的选择 a.溶液中大量存在的 b.参与质子转移反应 ,质子条件式书写方法 等式左边一得质子后产物 等式右边一失质子后产物 根据质子得失相等原则列出质子条件式
21 1.零水准法(质子参考水准) Ø 零水准物质的选择 a.溶液中大量存在的 b.参与质子转移反应 Ø 质子条件式书写方法 等式左边——得质子后产物 等式右边——失质子后产物 根据质子得失相等原则列出质子条件式

HAc溶液PBE: (1)选择参考物质:选择H2O和HAc作为参考水准 (2)判断哪些物质得质子,哪些物质失质子 (3) 等式左边—得质子后产物 等式右边一失质子后产物 [H]总=[Ac]+[OH] [H']8=[H']He+[HIno Na2S溶液PBE: [OH]点=2[H2S]+[HS]+[H+] 22
22 HAc溶液 PBE : (1)选择参考物质:选择 H2O 和HAc作为参考水准 (2)判断哪些物质得质子,哪些物质失质子 (3)等式左边——得质子后产物 等式右边——失质子后产物 [ H+]总= [ Ac-] + [ OH-] [ ] 2[ ] [ ] [ ] 2 OH 总 H S HS H Na2S溶液 PBE : H H HAc H H2O [ ] [ ] [ ] 总

÷NaHCO3溶液 参考物质:HC03,H20 +H H H2C03← HCO3 C03 +H -H" H30 H2O OH 质子条件式: [HCO3]+[H+]=[CO32-]+[OH] ①3
23 v NaHCO3溶液 参考物质:HCO3 -,H2O HCO3 - H2O -H + -H + +H + +H + CO3 2- OH - H2CO3 H3O + 质子条件式: [H2CO3]+[H+]=[CO3 2-]+[OH-]
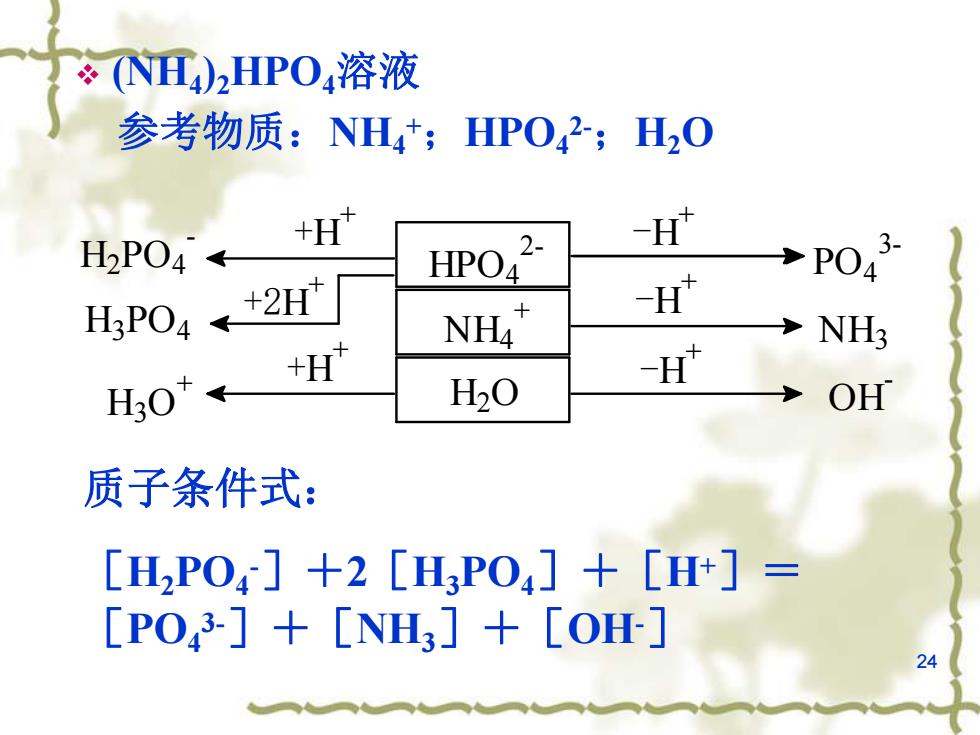
(NH)2HIPO4溶液 参考物质:NH4;HPO42;H2O H2P04← + 2- H HPO PO4 H3PO4 +2H NH4 H H30 +H H2O -H" OH 质子条件式: [H2PO4]+2[H3PO4]+[H+]= [PO43-]+[NHL3]+[OH] 24
24 v (NH4)2HPO4溶液 参考物质:NH4 +;HPO4 2-;H2O H2O -H + -H + +H + +H + OH - H3O + NH4 + NH3 -H + HPO4 2- PO4 3- H2PO4 - +2H + H3PO4 质子条件式: [H2PO4 -]+2[H3PO4]+[H+]= [PO4 3-]+[NH3]+[OH-]

PBE的意义: NH4)2HPO4溶液质子条件式: [H+]=[PO43-]+[NH3]+[OH] -[H2P04]-2[H3P04] 右边各项依次为HPO42-成为PO43放出的质子、 NH4+成为NH3放出的质子、水成为OH放出的 质子、HPO42-成为H2PO4消耗的质子、HPO4 2-成为H3PO4消耗的质子。 质子参考水准不出现在PBE中 25
25 右边各项依次为HPO4 2–成为PO4 3-放出的质子、 NH4 +成为NH3放出的质子、水成为OH-放出的 质子、HPO4 2–成为H2PO4 -消耗的质子 、 HPO4 2–成为H3PO4消耗的质子。 PBE的意义: (NH4)2HPO4溶液质子条件式: [H+]=[PO4 3-]+[NH3]+[OH-] -[H2PO4 -]-2[H3PO4] 质子参考水准不出现在PBE中