
石河子大学教案 课程名称:无机化学 药学 任课班级:2012中药(1-2)班 任课教师:乔秀文 化学化工学院化学系无机化学课程组 2012~2013学年第一学期 2012-08-24
石 河 子 大 学 教 案 课程名称: 无机化学 任课班级: 2012 (1-2)班 任课教师: 乔秀文 化学化工 学院 化学 系 无机化学课程组 2012~2013 学年第一学期 2012-08-24 药学 中药

姓名乔秀文职称教授总学时64 使用教材 《无机化学》张天蓝主编 1.让学生掌握元素周期律:初步掌握化学热力学、近 课 代物结构、化学平衡以及电化学基础等基本化学原理。 彩 2.培养学生运用上述原理掌握有关无机化学中元素的 教 单质及其化合物的基本知识,并具有对一般无机化学问题 学 进行理论分析和计算的能力,利用参考资料的能力。 目 3,教学中要重视讲授重要元素的单质及其化合物的性 的 质、结构和用途,为今后学习后续课程的新理论、新实验 技术打下必要的无机化学基础。 章次 章 名 学时 绪论 第4章 酸与碱 8 第3章 溶解与沉淀 第1章 原子结构 6 学 第2章 分子结构 9 时 第5章 氧化还原 第6章 配位化合物 6 不 第7章 s区元素 2 第8章 d区元素和ds区元素 8 配 第9章 p区元素 11
1 姓名 乔秀文 职称 教授 总学时 64 使用教材 《无机化学》 张天蓝 主编 课 程 教 学 目 的 1.让学生掌握元素周期律;初步掌握化学热力学、近 代物结构、化学平衡以及电化学基础等基本化学原理。 2.培养学生运用上述原理掌握有关无机化学中元素的 单质及其化合物的基本知识,并具有对一般无机化学问题 进行理论分析和计算的能力,利用参考资料的能力。 3.教学中要重视讲授重要元素的单质及其化合物的性 质、结构和用途,为今后学习后续课程的新理论、新实验 技术打下必要的无机化学基础。 学 时 分 配 章 次 章 名 学时 绪论 第 4 章 酸与碱 8 第 3 章 溶解与沉淀 6 第 1 章 原子结构 6 第 2 章 分子结构 9 第 5 章 氧化还原 8 第 6 章 配位化合物 6 第 7 章 s 区元素 2 第 8 章 d 区元素和 ds 区元素 8 第 9 章 p 区元素 11

年月日 1.使学生了解无机化学的发展及研究内容。 目的 2.了解化学和药学的关系。 3. 掌握无机化学的学习方法。 绪论 1、无机化学的内容及发展 2、化学与药学的关系。 教学 3、无机化学的学习方法 第2章溶液 第1节溶解 第2节溶液的组成标度 质量分数、摩尔分数、质量摩尔浓度、物质的量浓度、质量浓度 教学重 重点:各种常用溶液浓度的表示方法,尤其是物质的量浓度 点 以及有关计算 、难 点及教 学方法 作业思 考题(讨 论题)阅 读材料 1.本次课教学内容完成情况: 课」 ①顺利②较紧张③未完成④其他 2.学生课堂纪律:①良好②一般③较差: 3.教学内容深、广度:①合适②较合适③不合适 4.其它: 注:课后记包括学生课堂纪律、教学内容完成情况及教学体会等
2 年 月 日 教 学 目 的 1. 使学生了解无机化学的发展及研究内容。 2. 了解化学和药学的关系。 3. 掌握无机化学的学习方法。 教 学 内 容 绪 论 1、无机化学的内容及发展 2、化学与药学的关系。 3、无机化学的学习方法。 第 2 章 溶 液 第 1 节 溶解 第 2 节 溶液的组成标度 质量分数、摩尔分数、质量摩尔浓度、物质的量浓度、质量浓度 教学重 点 、难 点及教 学方法 重点:各种常用溶液浓度的表示方法,尤其是物质的量浓度 以及有关计算; 作业思 考题(讨 论题)阅 读材料 P 课 后 记 1. 本次课教学内容完成情况: ①顺利 ②较紧张 ③未完成 ④其他 2. 学生课堂纪律: ①良好 ②一般 ③较差: 3.教学内容深、广度:合适 较合适 不合适 4.其它: 注:课后记包括学生课堂纪律、教学内容完成情况及教学体会等
年月日 1、掌握弱电解质的电离平衡及稀释定律的概念和应用。 2、掌握酸碱质子理论及其应用 3、弱酸弱碱的电离平衡 酸和碱 第1节弱电解质的解离平衡 电离度,同离子效应,水的质子自递平衡 第2节酸碱理论 酸碱质子理论、酸碱质子理论酸碱的定义、强度。 布朗斯台德(怎.N.Bronsted)一洛里(T.M.Lowry)质子理论和路易斯酸碱 容 概念,则根据物质在反应过程中给出、接受质子或电子的性质,对物质 的酸碱性和酸碱反应的实质进行重新认识, 本章重点:应用化学平衡原理的基本概念,讨论弱电解质(弱酸、 教学重 弱碱)在水溶液中的电离平衡特点及缓冲溶液的概念,学习掌握酸碱厨 点 子理论的基本概念。 本章难点:是以酸碱质子理论的观点判断物质的酸碱性及其强度, 学方法 熟练掌握有关缓冲溶液的计算方法。 作业思 考题(讨 1.本次课教学内容完成情况: ①顺利:②较紧张: ③未完成:④其他: 课后记 2.学生课堂纪律:①良好②一般③较差: 3.教学内容深、广度:①合适②较合适③不合适 4.其它: 注:课后记包括学生课堂纪律、教学内容完成情况及教学体会等
3 年 月 日 教 学 目 的 1、掌握弱电解质的电离平衡及稀释定律的概念和应用。 2、掌握酸碱质子理论及其应用 3、弱酸弱碱的电离平衡 教 学 内 容 酸和碱 第1节 弱电解质的解离平衡 电离度,同离子效应,水的质子自递平衡 第 2 节 酸碱理论 酸碱质子理论、酸碱质子理论酸碱的定义、强度。 布朗斯台德(J.N.Bronsted)-洛里(T.M.Lowry)质子理论和路易斯酸碱 概念,则根据物质在反应过程中给出、接受质子或电子的性质,对物质 的酸碱性和酸碱反应的实质进行重新认识, 教学重 点 、难 点及教 学方法 本章重点:应用化学平衡原理的基本概念,讨论弱电解质(弱酸、 弱碱)在水溶液中的电离平衡特点及缓冲溶液的概念,学习掌握酸碱质 子理论的基本概念。 本章难点:是以酸碱质子理论的观点判断物质的酸碱性及其强度, 熟练掌握有关缓冲溶液的计算方法。 作业思 考题(讨 论题)阅 读材料 课 后 记 1. 本次课教学内容完成情况: ①顺利 : ②较紧张: ③未完成: ④其他: 2. 学生课堂纪律: ①良好 ②一般 ③较差: 3.教学内容深、广度:合适 较合适 不合适 4.其它: 注:课后记包括学生课堂纪律、教学内容完成情况及教学体会等
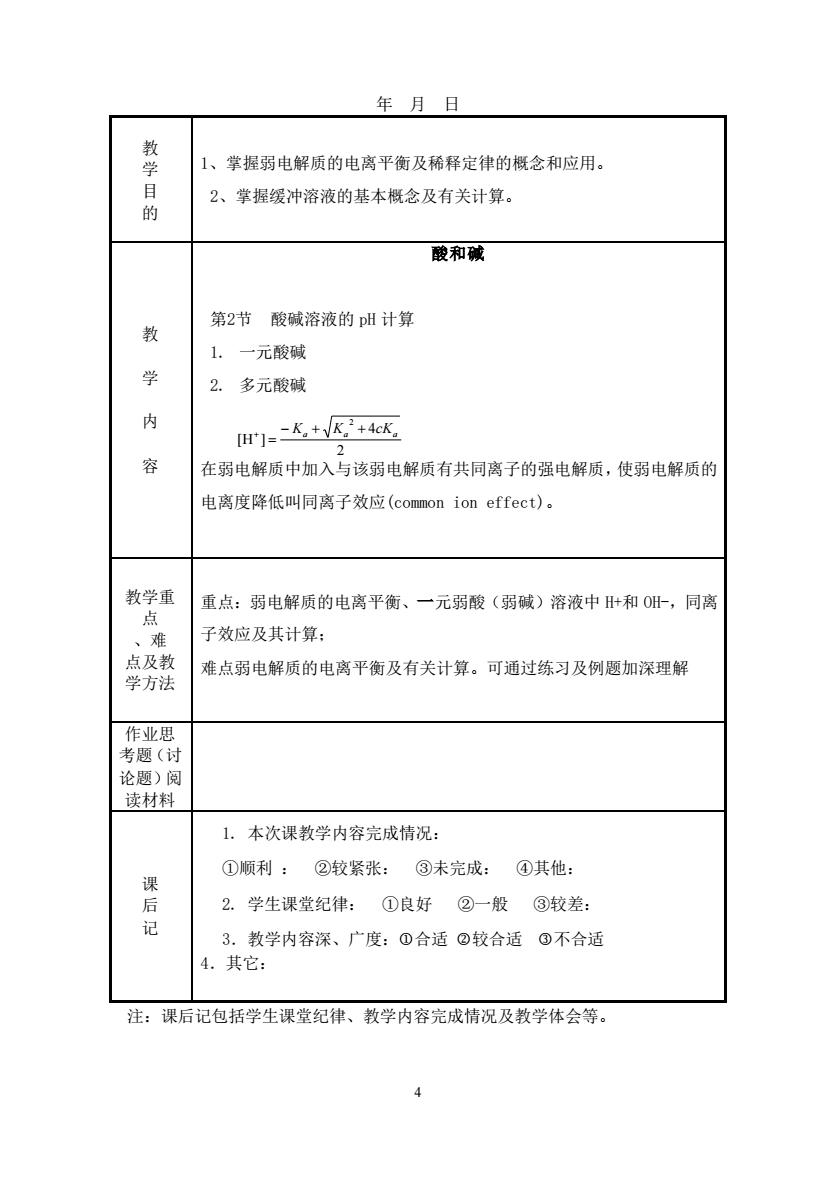
年月日 教学目 1、掌握弱电解质的电离平衡及稀释定律的概念和应用。 2、掌握缓冲溶液的基本概念及有关计算。 酸和碱 粉 第2节酸碱溶液的pH计算 1.一元酸碱 学 2.多元酸碱 $ 田]=大+K+4e述 在弱电解质中加入与该弱电解质有共同离子的强电解质,使弱电解质的 电离度降低叫同离子效应(common ion effect)。 教学重 重点:弱电解质的电离平衡、一元弱酸(弱碱)溶液中+和0H-,同离 点 子效应及其计算: 点及教 难点弱电解质的电离平衡及有关计算。可通过练习及例题加深理解 学方法 作业思 考题(讨 论愿)阅 读材料 1.本次课教学内容完成情况: ①顺利:②较紧张:③未完成:④其他: 2.学生课堂纪律:①良好②一般③较差: 3.教学内容深、广度:①合适⊙较合适⊙不合适 4.其它: 注:课后记包括学生课堂纪律、教学内容完成情况及教学体会等
4 年 月 日 教 学 目 的 1、掌握弱电解质的电离平衡及稀释定律的概念和应用。 2、掌握缓冲溶液的基本概念及有关计算。 教 学 内 容 酸和碱 第2节 酸碱溶液的 pH 计算 1. 一元酸碱 2. 多元酸碱 在弱电解质中加入与该弱电解质有共同离子的强电解质,使弱电解质的 电离度降低叫同离子效应(common ion effect)。 教学重 点 、难 点及教 学方法 重点:弱电解质的电离平衡、一元弱酸(弱碱)溶液中 H+和 OH-,同离 子效应及其计算; 难点弱电解质的电离平衡及有关计算。可通过练习及例题加深理解 作业思 考题(讨 论题)阅 读材料 课 后 记 1. 本次课教学内容完成情况: ①顺利 : ②较紧张: ③未完成: ④其他: 2. 学生课堂纪律: ①良好 ②一般 ③较差: 3.教学内容深、广度:合适 较合适 不合适 4.其它: 注:课后记包括学生课堂纪律、教学内容完成情况及教学体会等。 2 4 [H ] 2 a a a − K + K + cK = +