
第三章 酸碱滴定法的应用 滴定分析法 二、配位滴定法的应用 三、氧化还原滴定法的 应用 第四节 滴定分析法应用 四、沉淀滴定法的应用 下页 帽动 越回
第三章 滴定分析法 第四节 滴定分析法应用 一、酸碱滴定法的应用 二、配位滴定法的应用 三、氧化还原滴定法的 应用 四、沉淀滴定法的应用

、 酸碱滴定法的应用 1.混合碱的测定(双指示剂法) (动画) NaOH,Na2C03,NaHCO3,判断由哪两种组成(定性/定量 计算)。Na2CO3能否直接滴定,有几个突跃? H2CO3=H++HCO3 pKa=6.38 HC03=Ht+C032pKa2=10.25 V>V2:NaOH(V1-V),Na2CO3(V) V=V2:Na.CO Vi<V2 Na,CO3(V),NaHCO3(V2-V1) V=0:NaHCO =0:NaOH 上页 下页 返回
一、酸碱滴定法的应用 1.混合碱的测定(双指示剂法) NaOH ,Na2CO3 ,NaHCO3 , 判断由哪两种组成(定性/定量 计算)。Na2CO3能否直接滴定, 有几个突跃? H2CO3 = H+ + HCO3 - pKa1=6.38 HCO3 - = H+ + CO3 2- pKa2=10.25 V1>V2 : NaOH(V1 – V2 ) ,Na2CO3 (V2 ) V1=V2 : Na2CO3 V1<V2 : Na2CO3 (V1 ),NaHCO3 (V2 –V1 ) V1=0 : NaHCO3 V2=0 : NaOH (动画)
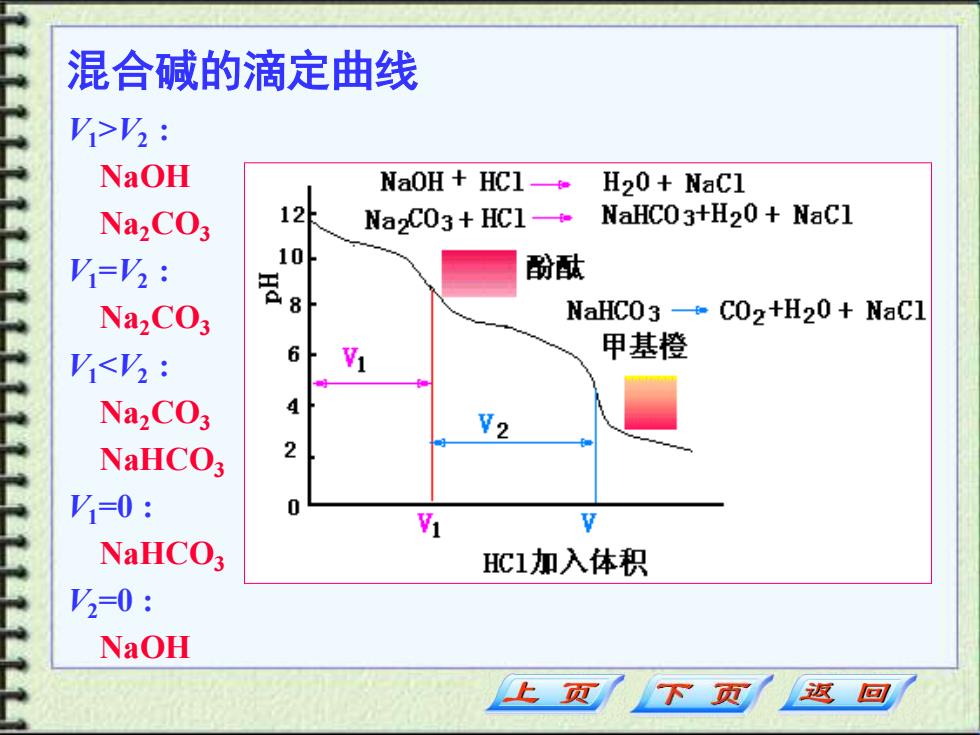
混合碱的滴定曲线 K>: NaOH NaOH+HC1- H20+NaCl NazCO3 12 Na2C03+HCl- NaHCO3+H20+NaCl V=V2: 10 酚酞 Na,CO3 NaHCO3-CO2+H20+NaCl <: 6 甲基橙 Na2CO3 4 NaHCO3 2 V=0: NaHCO; HC1加入体积 3=0: NaOH 上页 下页返回
混合碱的滴定曲线 V1>V2 : NaOH Na2CO3 V1=V2 : Na2CO3 V1<V2 : Na2CO3 NaHCO3 V1=0 : NaHCO3 V2=0 : NaOH

2.化合物中氮含量的测定 (1)蒸馏法 将铵盐试液置于蒸馏瓶中,加入过量浓NaOH溶液进行 蒸馏,用过量的H3BO3溶液吸收蒸发出的NH3: NH3+H3 BO3=NH++H2BO3 用HC1标准溶液滴定反应生物的HBO3, H++H2BO3=H3BO3 终点时的pH=5,选用甲基红作指示剂。 下页 返回
2.化合物中氮含量的测定 (1)蒸馏法 将铵盐试液置于蒸馏瓶中,加入过量浓NaOH溶液进行 蒸馏,用过量的H3BO3溶液吸收蒸发出的NH3: NH3+ H3BO3 = NH+ 4+ H2BO3 - 用HCl标准溶液滴定反应生物的H2BO3 -, H+ + H2BO3 - = H3BO3 终点时的pH=5,选用甲基红作指示剂

(2)甲醛法 反应式: 6HCHO+4NH=(CH2)6NH++3H++6H2O 利用NaOH标准溶液滴定反应生成的4个H+。 六次甲基四胺(CH2)6N4是一种极弱有机碱,应选用 酚酞作指示剂。 上页下页返回
(2)甲醛法 反应式: 6HCHO+4NH4 + =(CH2 )6N4H++3H + +6H2O 利用NaOH标准溶液滴定反应生成的4 个H+ 。 六次甲基四胺(CH2)6N4是一种极弱有机碱,应选用 酚酞作指示剂