
第四章 电解质溶液的基本 电化学分析法 性质 二、电导测量 三、电导分析法的应用 第六节 电导分析法 下页 螺助 热回
第六节 电导分析法 第四章 电化学分析法 一、 电解质溶液的基本 性质 二、 电导测量 三、 电导分析法的应用

电解质溶液的基本性质 1. 电解质溶液的基本性质 导电性质:离子导电; 1)1 电导(G、电导率(、摩尔电导率(Am) 电导:衡量电解质溶液导电能力的物理量,电阻的倒数。 G=1/R=K·A/I=K·KWA 单位:西门子S,1S=121 电导率:K=1/p=KWA·G 电阻率的倒数单位:S.ml 两电极板为单位面积,距离为单位长度时溶液的电导。 电导池常数:KwA=IA (A电极面积;1电极间距) 由标准KC1溶液的电导率(查表)确定电导率和电导池常数。 下页 返回
一、电解质溶液的基本性质 1. 电解质溶液的基本性质 导电性质:离子导电; (1) 电导(G) 、电导率() 、摩尔电导率(m) 电导:衡量电解质溶液导电能力的物理量,电阻的倒数。 G=1/R= A / l = K(l/A) 单位:西门子S,1S=1-1 电导率: =1 / =K(l/A) G 电阻率的倒数 单位:S m-1 两电极板为单位面积,距离为单位长度时溶液的电导。 电导池常数:K(l/A) =l / A (A电极面积; l 电极间距) 由标准KCl溶液的电导率(查表)确定电导率和电导池常数
80 摩尔电导率(Am) H2S04 % KOH 定义:距离为单位长度的两电极板间 40 KCl 含有单位物质的量的电解质的溶液的电导。 MgSO 单位:Sm2.mo1 乙酸 10 15 不同浓度、不同类型电解质导电能力 电导率与物质的量浓度的关系 的比较。 400 右图中出现极大值的原因: 1m KCI 300 电导率的大小与溶液中离子数日和 离子自由运动能力有关。两种因素相 NaOH 200 互制约。浓度大,相互作用力大。 100 AgNO3 无限稀释摩尔电导() CHCOOH 05 1.0 An =A -Avc c 摩尔电导率与浓度c的变化关系 页 返 回
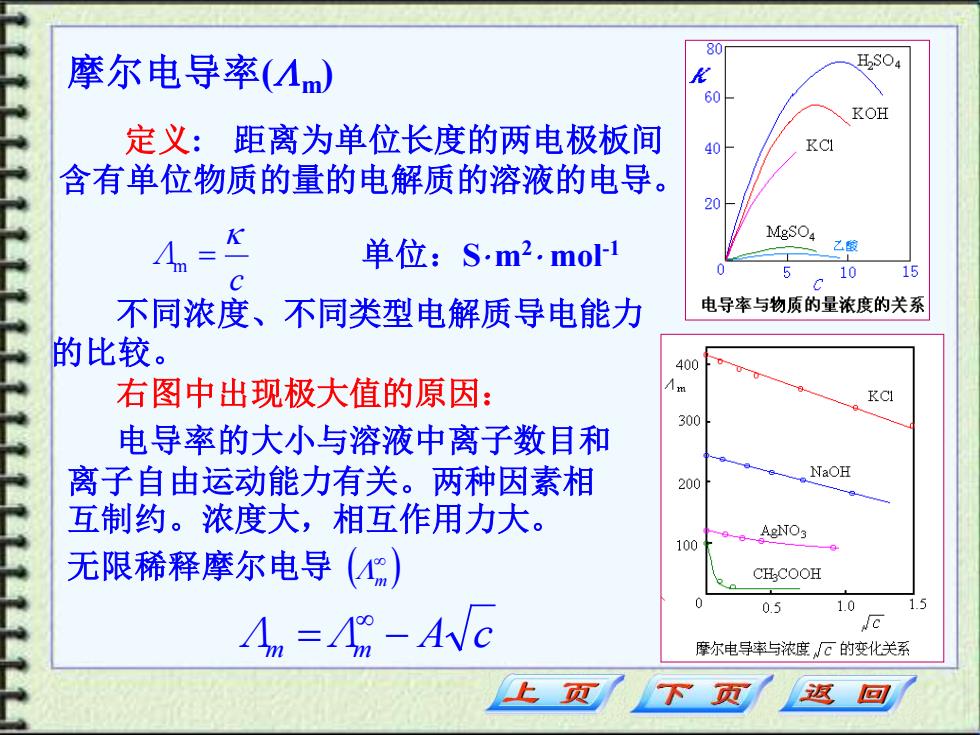
摩尔电导率( m) 定义: 距离为单位长度的两电极板间 含有单位物质的量的电解质的溶液的电导。 c Λ m = 单位:S m2 mol-1 不同浓度、不同类型电解质导电能力 的比较。 Λ Λ A c m = m − ( ) m 右图中出现极大值的原因: 电导率的大小与溶液中离子数目和 离子自由运动能力有关。两种因素相 互制约。浓度大,相互作用力大。 无限稀释摩尔电导
2.离子的电导与漂移速率 (1)离子的电迁移率 电解质 00 离子在外加电场中受溶 剂阻力和电场力,平衡时, KCI 0.014986 34.8×104 以恒定的速率运动。离子 LiCl 0.011503 的漂移速率U。 单位电场强度下离子的漂 KNO3 0.01450 34.9×104 移速率:离子的电迁移率uB LiNO: 0.01101 UB=UB/E KCI 0.014986 4.90×104 (2)离子独立运动定律 KNO3 0.01450 由右表数据可以得出 离子独立运动定律: LiCl 0.011503 4.90×104 4m=4,++△4m, LiNO; 0.01101 下页 返回
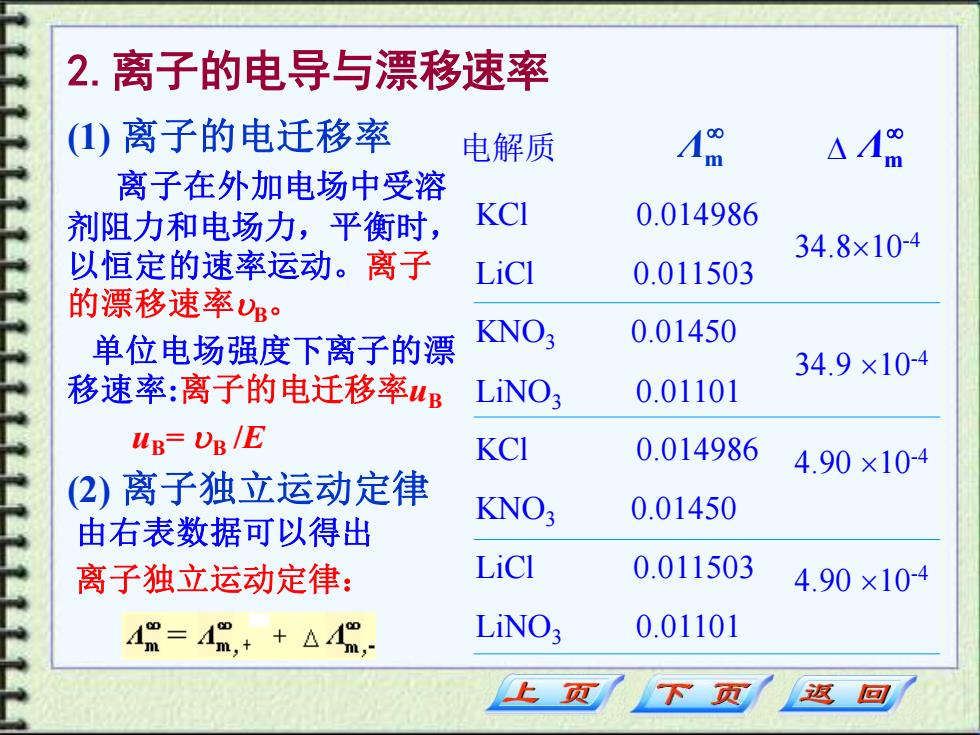
2.离子的电导与漂移速率 电解质 Λm KCl 0.014986 LiCl 0.011503 KNO3 0.01450 LiNO3 0.01101 KCl 0.014986 KNO3 0.01450 LiCl 0.011503 LiNO3 0.01101 Λm 34.810-4 34.9 10-4 4.90 10-4 4.90 10-4 (1) 离子的电迁移率 离子在外加电场中受溶 剂阻力和电场力,平衡时, 以恒定的速率运动。离子 的漂移速率B。 单位电场强度下离子的漂 移速率:离子的电迁移率uB uB= B /E (2) 离子独立运动定律 由右表数据可以得出 离子独立运动定律:
3)离子的电导 离子 溶液的总电导:G=∑cAm 4x104 K 73.52 弱电解质(乙酸)溶液的m Na+ 50.11 Am NaOAc)=A Na)+1(OAc-) L计 38.69 4m (HCI)=4%m(H+)+1%m(CI) H 349.82 Am (NaCl)=A%m (Na)+Am(CI) Ag" 61.92 m(H0Ac)片m(Ht)+m(0A) C 76.34 =A%m (NaOAc)+m(HCI)-A%m (NaCI) Br 78.4 H、L计、Na、K+在溶液中的 OH 198 运动速度大小顺序? 返 回
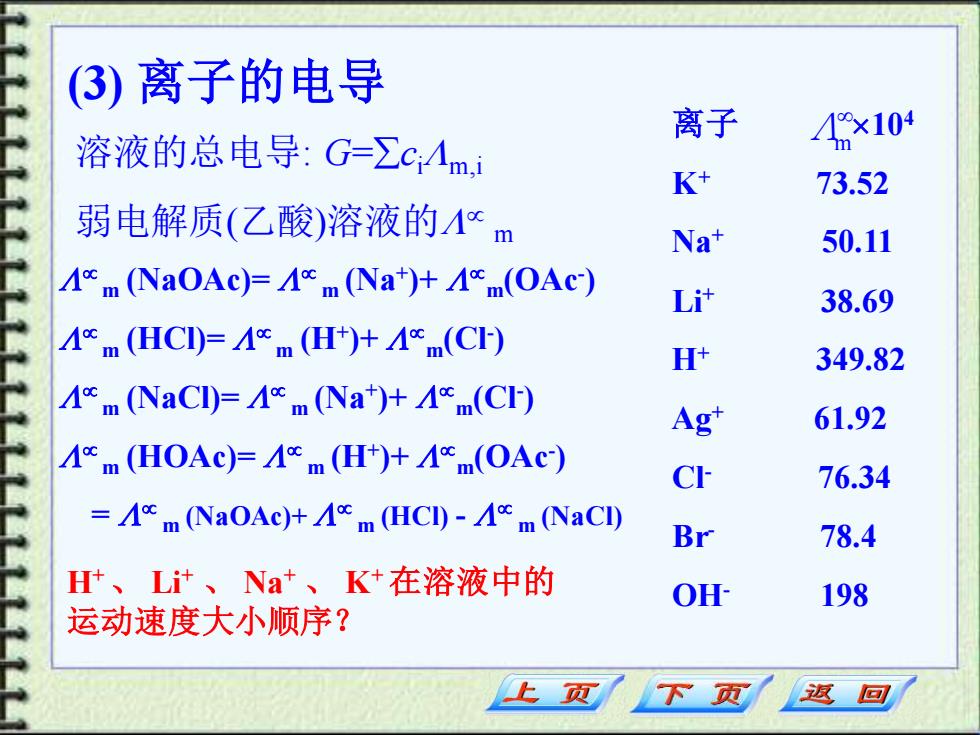
(3) 离子的电导 溶液的总电导: G=cim,i 弱电解质(乙酸)溶液的 m 离子 Λm 104 K+ 73.52 Na+ 50.11 Li+ 38.69 H+ 349.82 Ag+ 61.92 Cl- 76.34 Br- 78.4 OH- 198 H+ 、 Li+ 、 Na+ 、 K+ 在溶液中的 运动速度大小顺序? m (NaOAc)= m (Na+ )+ m(OAc- ) m (HCl)= m (H+ )+ m(Cl- ) m (NaCl)= m (Na+ )+ m(Cl- ) m (HOAc)= m (H+ )+ m(OAc- ) = m (NaOAc)+ m (HCl) - m (NaCl)