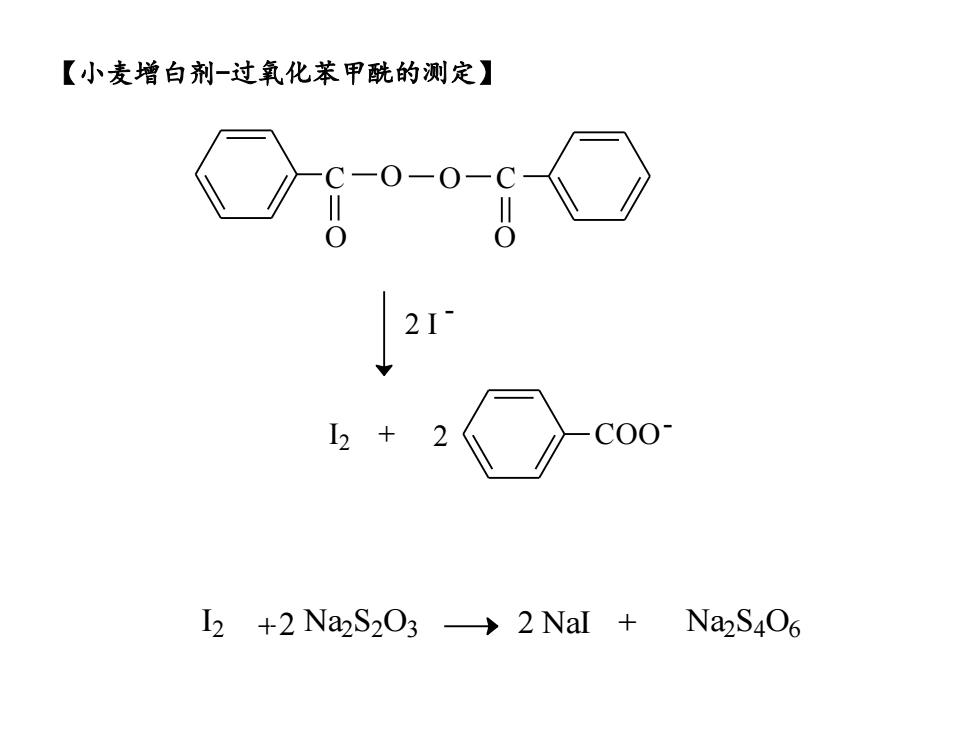
【小麦增白剂一过氧化苯甲酰的测定】 I2+2 C00 I2 +2 Na2S203>2 Nal Na2S406
【小麦增白剂-过氧化苯甲酰的测定】 C C O O O O I 2 + - 2 I COO- 2 I 2 + 2 Na2 S2O3 2 NaI + 2 Na2 S4O6

【方便面中氯化钠含量的测定】 NaCl+AgNO3→AgCl↓+NaNO3
【方便面中氯化钠含量的测定】 NaCl + AgNO3 → AgCl ↓ + NaNO3

一、滴定分析法概述 1、基本术语 NaOH HCI NaCI H2O 碱式滴定管 酸式滴定管 HCI HCI 滴定装置 NaOH
一、滴定分析法概述 1、基本术语 NaOH HCl NaOH + HCl = NaCl + H2O HCl NaOH

(1)标准溶液 (2)滴定 (3)化学计量点(比如上面的酸碱中和反应:pH=7.0) (4)滴定终点 (5)滴定终点误差 (6)指示剂(酚酞的变色点:pH=9.1,变色范围:8.2~10.0; (无色)(紫红) 甲基红的变色点:pH=5.1,变色范围:4.4~6.2;) (红色) (黄色)
(1)标准溶液 (2)滴定 (3)化学计量点(比如上面的酸碱中和反应:pH=7.0) (4)滴定终点 (5)滴定终点误差 (6)指示剂(酚酞的变色点:pH=9.1,变色范围:8.2 ~ 10.0; (无色) (紫红) 甲基红的变色点:pH=5.1,变色范围:4.4 ~ 6.2; ) (红色) (黄色)

2、滴定分析法对化学反应的要求 并不是所有的化学反应都适用于滴定分析法,适合滴定分析的反应 必须具备以下几个条件: (1)反应必须按一定的化学方程式进行,即,有确定的化学计量关 系,无副反应发生,而且反应必须完全,在达到滴定终点时,反应至少 达到99.99%以上。 (2)反应要快,对于速度较慢的反应可通过加热或加入催化剂的 方法来加快反应速率。 (3)必须有较简单可靠的方法确定滴定终,点,如用合适的指示剂或 其他物理方法
并不是所有的化学反应都适用于滴定分析法,适合滴定分析的反应 必须具备以下几个条件: 2、滴定分析法对化学反应的要求 (1)反应必须按一定的化学方程式进行,即,有确定的化学计量关 系,无副反应发生,而且反应必须完全,在达到滴定终点时,反应至少 达到 99.99% 以上。 (2)反应要快,对于速度较慢的反应可通过加热或加入催化剂的 方法来加快反应速率。 (3)必须有较简单可靠的方法确定滴定终点,如用合适的指示剂或 其他物理方法