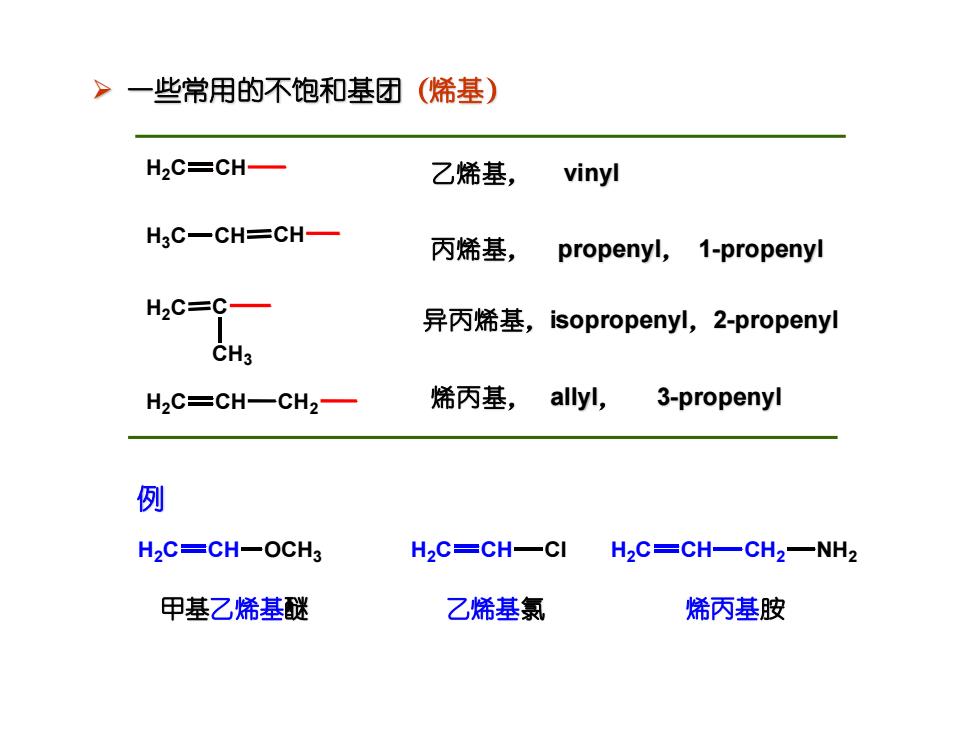
➢ 一些常用的不饱和基团(烯基) H2C CH H3C CH CH H2C C CH3 H2C CH CH2 乙烯基, vinyl 丙烯基, propenyl, 1-propenyl 异丙烯基,isopropenyl,2-propenyl 烯丙基, allyl, 3-propenyl 甲基乙烯基醚 乙烯基氯 烯丙基胺 H2C CH OCH3 H2C CH Cl H2C CH CH2 NH2 例
➢ 一些常用的不饱和基团(烯基) H2C CH H3C CH CH H2C C CH3 H2C CH CH2 乙烯基, vinyl 丙烯基, propenyl, 1-propenyl 异丙烯基,isopropenyl,2-propenyl 烯丙基, allyl, 3-propenyl 甲基乙烯基醚 乙烯基氯 烯丙基胺 H2C CH OCH3 H2C CH Cl H2C CH CH2 NH2 例

四、烯烃的化学性质 1. 双键的结构与性质分析 C C C C 键能: s 键 ~347 kJ / mol p 键 ~263 kJ / mol ➢p 键活性比 s 键大 ➢不饱和,可加成至饱和 p 电子结合较松散, 易参与反应。是电子 供体,有亲核性。 ➢与亲电试剂结合 ➢与氧化剂反应
四、烯烃的化学性质 1. 双键的结构与性质分析 C C C C 键能: s 键 ~347 kJ / mol p 键 ~263 kJ / mol ➢p 键活性比 s 键大 ➢不饱和,可加成至饱和 p 电子结合较松散, 易参与反应。是电子 供体,有亲核性。 ➢与亲电试剂结合 ➢与氧化剂反应

2. 烯烃加成的三种主要类型 ➢亲电加成 C C + A B C C A B 加 成 A B A + B + - A B A + B A B H2 ➢自由基加成 ➢催化加氢 (异裂) (均裂) 重点
2. 烯烃加成的三种主要类型 ➢亲电加成 C C + A B C C A B 加 成 A B A + B + - A B A + B A B H2 ➢自由基加成 ➢催化加氢 (异裂) (均裂) 重点
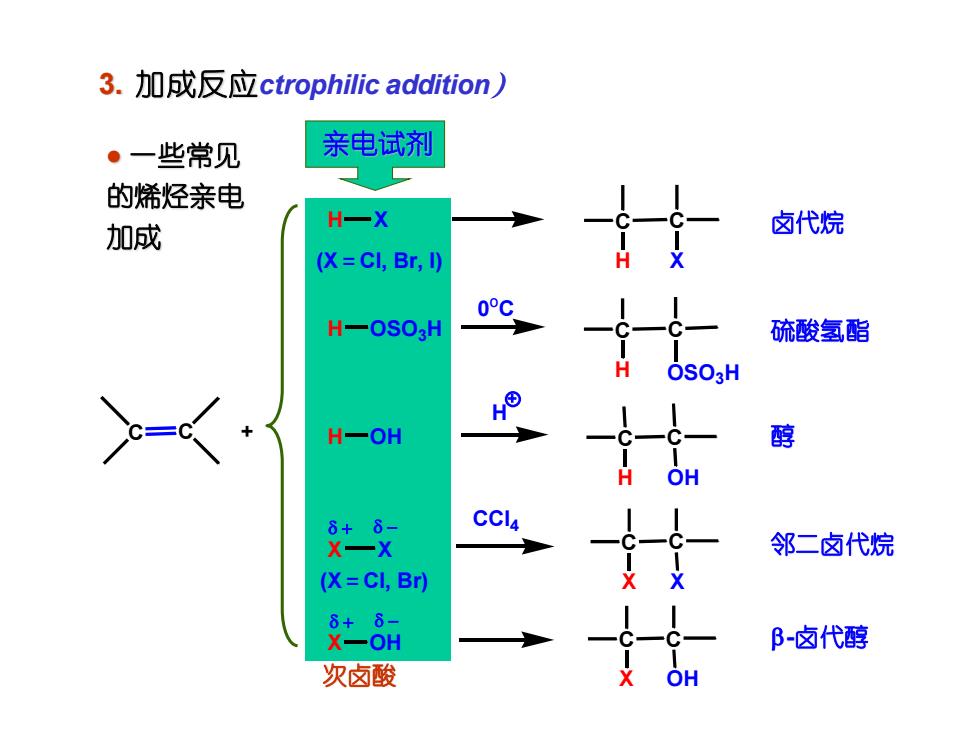
3. 加成反应ctrophilic addition) ⚫ 一些常见 的烯烃亲电 加成 C C + H X C C (X=Cl, Br, I) H X H OSO3H C C H OSO3H 0 oC H C C H OH X X C C (X=Cl, Br) X X CCl4 C C X OH H OH X OH + - + - 亲电试剂 卤代烷 硫酸氢酯 醇 邻二卤代烷 b-卤代醇 次卤酸
3. 加成反应ctrophilic addition) ⚫ 一些常见 的烯烃亲电 加成 C C + H X C C (X=Cl, Br, I) H X H OSO3H C C H OSO3H 0 oC H C C H OH X X C C (X=Cl, Br) X X CCl4 C C X OH H OH X OH + - + - 亲电试剂 卤代烷 硫酸氢酯 醇 邻二卤代烷 b-卤代醇 次卤酸
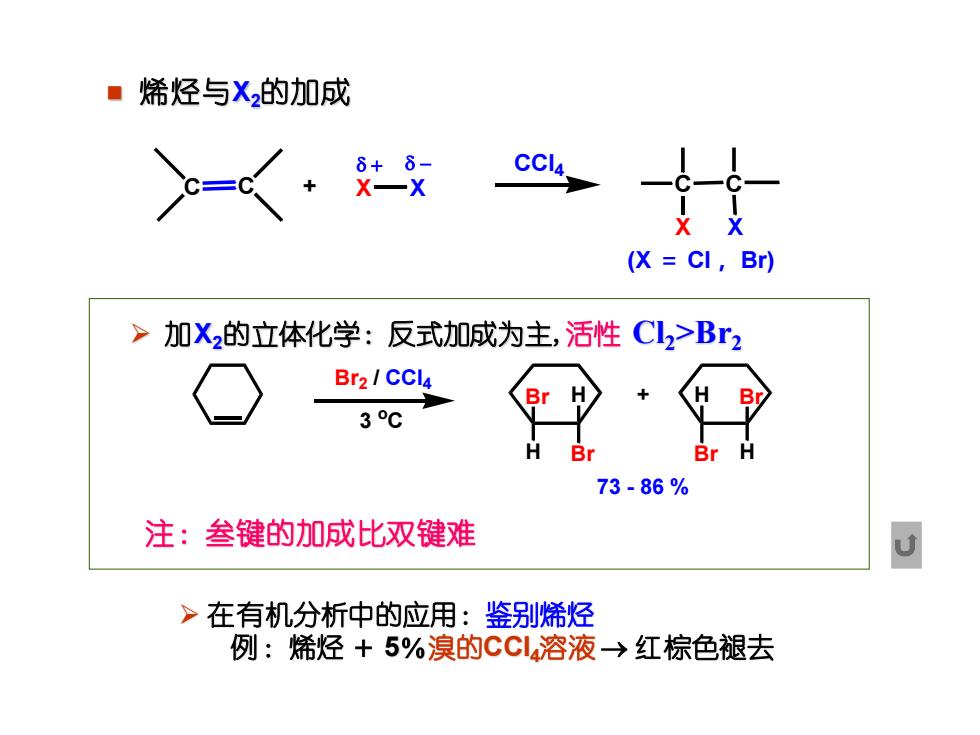
◼ 烯烃与X2的加成 ➢ 加X2的立体化学:反式加成为主,活性 Cl2>Br2 X X C C X X (X = Cl, Br) CCl4 + - C C + 3 oC Br2 / CCl4 Br H H Br Br H H Br + 73 - 86 % ➢ 在有机分析中的应用:鉴别烯烃 例:烯烃 + 5%溴的CCl4溶液 → 红棕色褪去 注:叁键的加成比双键难
◼ 烯烃与X2的加成 ➢ 加X2的立体化学:反式加成为主,活性 Cl2>Br2 X X C C X X (X = Cl, Br) CCl4 + - C C + 3 oC Br2 / CCl4 Br H H Br Br H H Br + 73 - 86 % ➢ 在有机分析中的应用:鉴别烯烃 例:烯烃 + 5%溴的CCl4溶液 → 红棕色褪去 注:叁键的加成比双键难