
■(3)系统命名法 1. 以含有羟基的最长碳链为主链,并以它为母体,其他官能团为取代基 2.羟基的编号尽可能的小。 3.羟基的编号相同时,第一个分叉处的编号尽可能的小。 4.优先级低的取代基编号尽可能的小。 书写:先写优先性小的官能团,醇的位置也要标号。 以上规则应用的前提:不含有其他比羟基优先级高的官能团! RCOOH>RCOOR>RCONHR>RCN>RCHO >RC-OR>ROH>RSH>RNH2>R-O-R>R2C=CR2 R-C=C-R>R-X>R-NO, 6
(3)系统命名法 1. 以含有羟基的最长碳链为主链,并以它为母体,其他官能团为取代基 2. 羟基的编号尽可能的小。 3. 羟基的编号相同时,第一个分叉处的编号尽可能的小。 4. 优先级低的取代基编号尽可能的小。 书写:先写优先性小的官能团,醇的位置也要标号。 以上规则应用的前提:不含有其他比羟基优先级高的官能团! RCOOH > RCOOR > RCONHR > RCN > RCHO > RC=OR > ROH > RSH > RNH2 > R-O-R > R2C=CR2 > R-C≡C-R > R-X > R-NO2 6
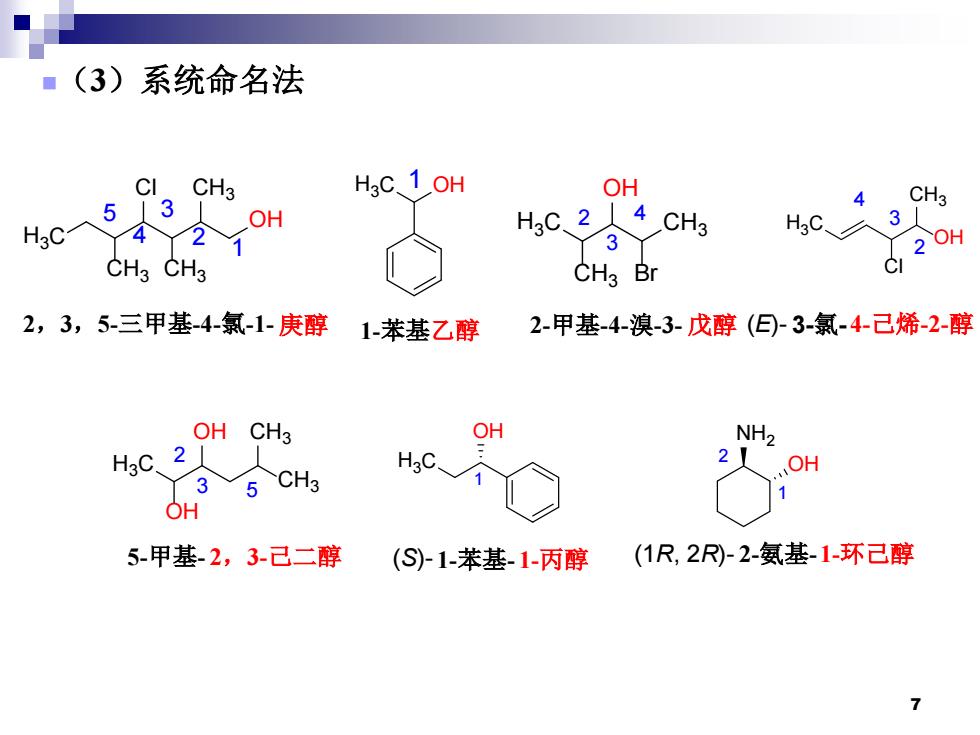
(3)系统命名法 CI CH3 H3C 1OH OH CH3 5 13 OH 3 HgC HC2人4CH3 3 2OH CH3 CH3 CH3 Br ci 2,3,5-三甲基-4-氯-1-庚醇 1-苯基乙醇 2-甲基-4-溴-3-戊醇(日-3-氯-4己烯-2-醇 OH CH3 OH NH2 HaC.2 3 5 CH3 H:C 2 OH OH 5-甲基-2,3-己二醇 (S)-1-苯基-1-丙醇 (1R,2R)-2-氨基-1环己醇
(3)系统命名法 H3C OH CH3 CH3 Cl CH3 H3C OH CH3 Cl H3C CH3 Br OH CH3 H3C OH H3C CH3 OH OH CH3 H3C OH OH NH2 2,3,5-三甲基-4-氯-1- 庚醇 1-苯基乙醇 2-甲基-4-溴-3- 戊醇 3-氯- 4-己烯-2-醇 5-甲基- 2,3-己二醇 1-苯基- 1-丙醇 (E)- (S)- (1R, 2R)- 2-氨基-1-环己醇 1 4 2 5 3 1 2 3 4 2 3 4 2 3 5 1 1 2 7
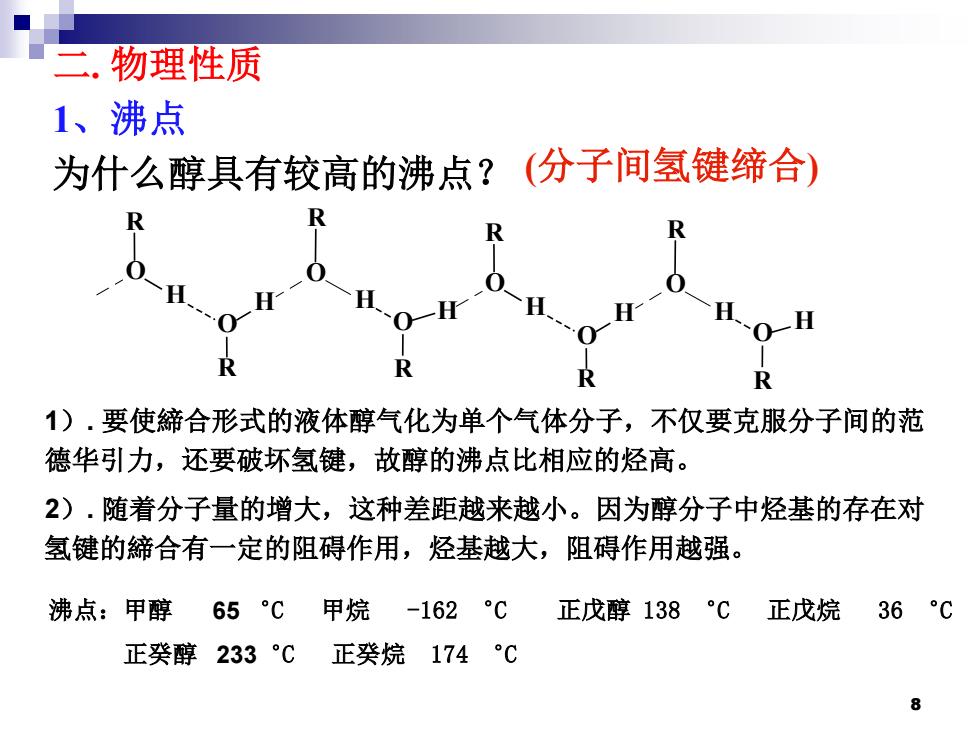
二,物理性质 1、沸点 为什么醇具有较高的沸点?(分子间氢键缔合) R 0 H 0-H R 1).要使締合形式的液体醇气化为单个气体分子,不仅要克服分子间的范 德华引力,还要破坏氢键,故醇的沸点比相应的烃高。 2).随着分子量的增大,这种差距越来越小。因为醇分子中烃基的存在对 氢键的締合有一定的阻碍作用,烃基越大,阻碍作用越强。 沸点:甲醇 65℃甲烷-162℃ 正戊醇138℃正戊烷 36 C 正癸醇233°℃正癸烷174°℃ 8
二. 物理性质 (分子间氢键缔合) 1、沸点 为什么醇具有较高的沸点? O H R H O R O R H O H R O H R H O R O R H O H R 1). 要使締合形式的液体醇气化为单个气体分子,不仅要克服分子间的范 德华引力,还要破坏氢键,故醇的沸点比相应的烃高。 2). 随着分子量的增大,这种差距越来越小。因为醇分子中烃基的存在对 氢键的締合有一定的阻碍作用,烃基越大,阻碍作用越强。 沸点:甲醇 65 ︒C 甲烷 -162 ︒C 正戊醇 138 ︒C 正戊烷 36 ︒C 正癸醇 233︒C 正癸烷 174 ︒C 8
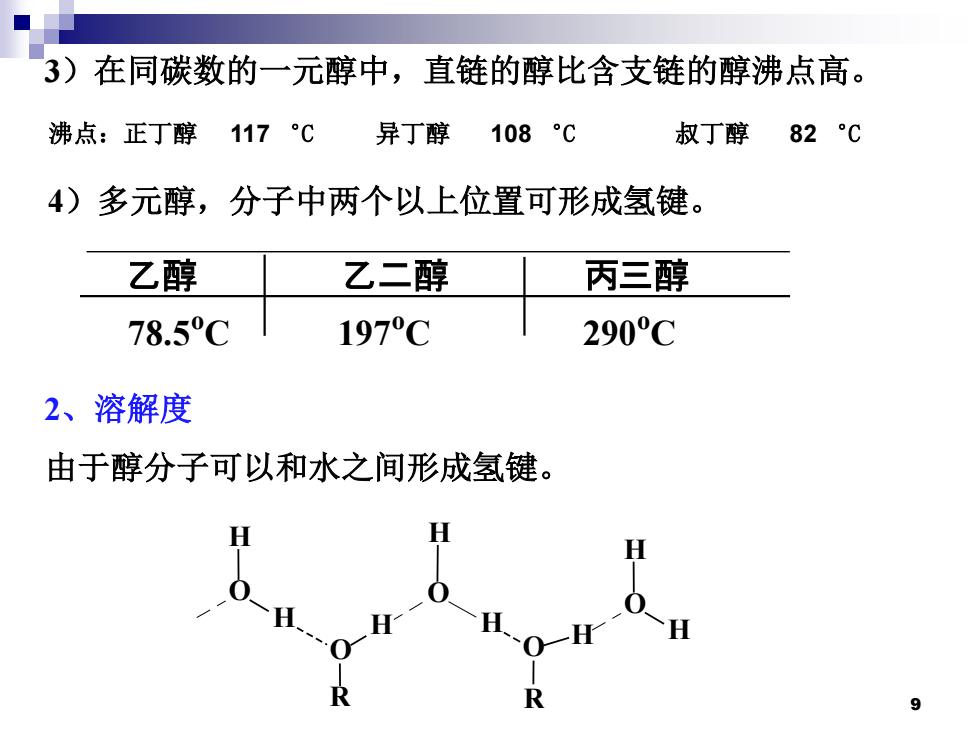
3)在同碳数的一元醇中,直链的醇比含支链的醇沸点高。 沸点:正丁醇117C 异丁醇 108C 叔丁醇 82°C 4)多元醇,分子中两个以上位置可形成氢键。 乙醇 乙二醇 丙三醇 78.5C 197C 290°C 2、溶解度 由于醇分子可以和水之间形成氢键。 R 9
3)在同碳数的一元醇中,直链的醇比含支链的醇沸点高。 4)多元醇,分子中两个以上位置可形成氢键。 乙醇 乙二醇 丙三醇 78.5o C 197o C 290o C 2、溶解度 由于醇分子可以和水之间形成氢键。 O H R H O H O H H O H R H O H 沸点:正丁醇 117 ︒C 异丁醇 108 ︒C 叔丁醇 82 ︒C 9

低级醇(3个碳以下的醇及叔丁醇)可以与水互溶。 随着分子量的增大,醇羟基与水形成氢键的能力减小, 溶解度随之降低,当烃基大到一定程度,高级醇就完 全不溶于水。 在强酸中的溶解度比在水中大。 水 浓HCI CH3CH2CH2CH2OH 8% 互溶 多元醇,分子中两个以上位置可形成氢键,故在水 中的溶解度很大,如乙二醇,甘油都可和水互溶
•低级醇(3个碳以下的醇及叔丁醇)可以与水互溶。 随着分子量的增大,醇羟基与水形成氢键的能力减小, 溶解度随之降低,当烃基大到一定程度,高级醇就完 全不溶于水。 •多元醇,分子中两个以上位置可形成氢键,故在水 中的溶解度很大,如乙二醇,甘油都可和水互溶。 •在强酸中的溶解度比在水中大。 CH3CH2CH2CH2OH 水 浓HCl 8% 互溶 10