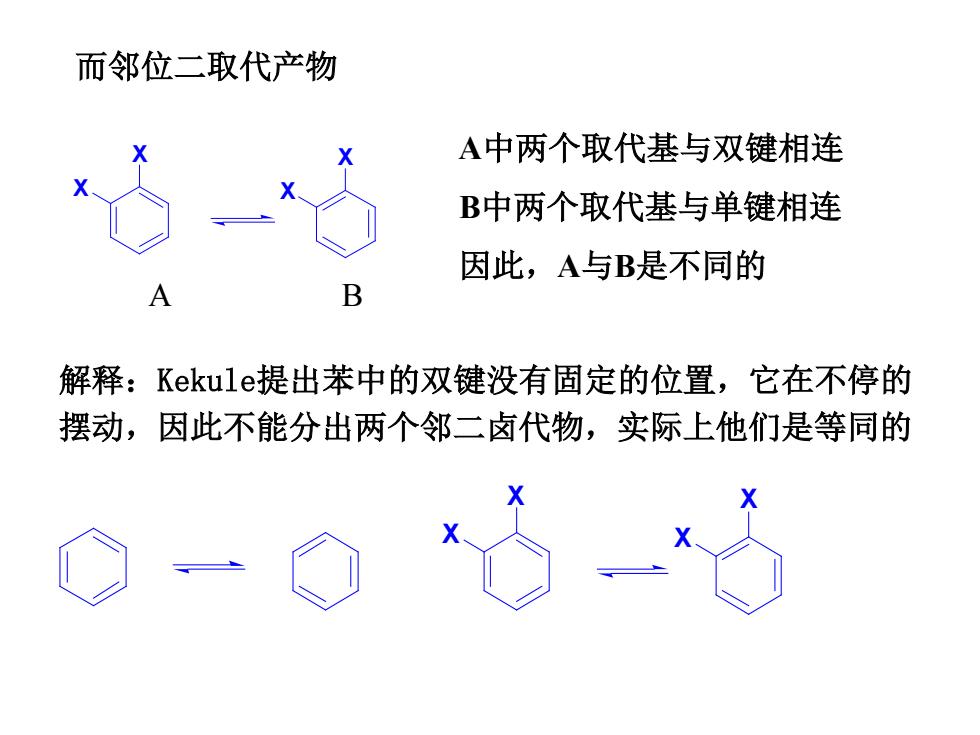
而邻位二取代产物 A中两个取代基与双键相连 B中两个取代基与单键相连 因此,A与B是不同的 B 解释:Kekule?提出苯中的双键没有固定的位置,它在不停的 摆动,因此不能分出两个邻二卤代物,实际上他们是等同的
而邻位二取代产物 A中两个取代基与双键相连 B中两个取代基与单键相连 因此,A与B是不同的 A B 解释:Kekule提出苯中的双键没有固定的位置,它在不停的 摆动,因此不能分出两个邻二卤代物,实际上他们是等同的 X X X X X X X X
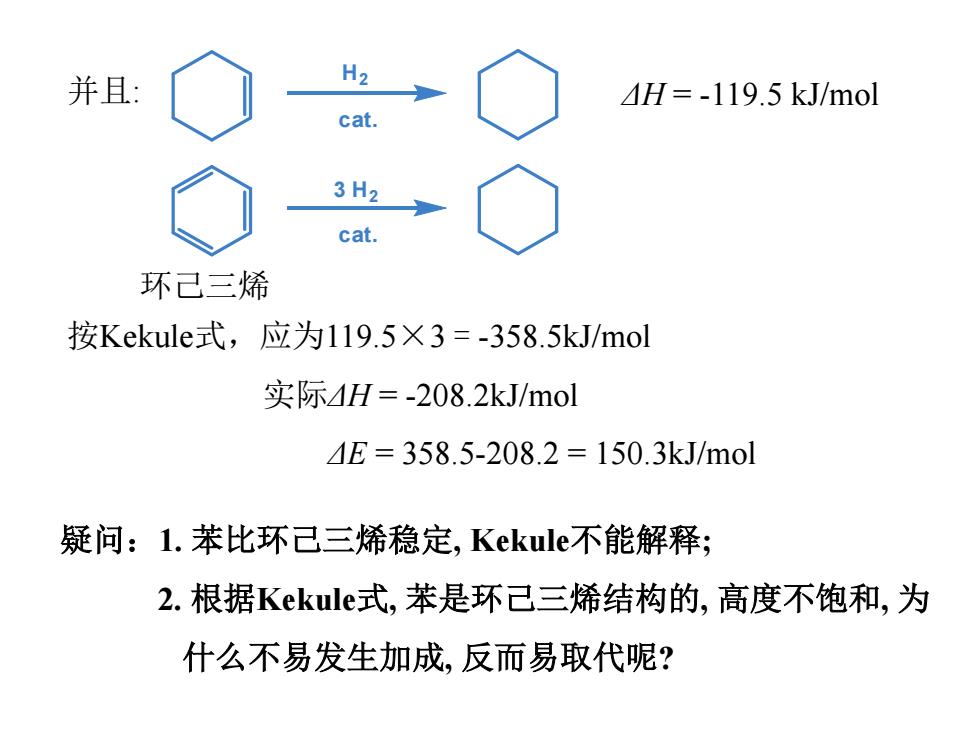
并且: H2 H=-119.5 kJ/mol cat. 3H2 cat. 环己三烯 按Kekule式,应为119.5×3=-358.5kJ/mol 实际4H=-208.2kJ/mol 4E=358.5-208.2=150.3kJ/mol 疑问:1.苯比环己三烯稳定,Kekule不能解释; 2.根据Kekule式,苯是环己三烯结构的,高度不饱和,为 什么不易发生加成,反而易取代呢?
并且: 按Kekule式,应为119.5×3 = -358.5kJ/mol 实际ΔH = -208.2kJ/mol ΔE = 358.5-208.2 = 150.3kJ/mol 疑问:1. 苯比环己三烯稳定, Kekule不能解释; 2. 根据Kekule式, 苯是环己三烯结构的, 高度不饱和, 为 什么不易发生加成, 反而易取代呢? cat. H2 3 H2 cat. ΔH = -119.5 kJ/mol 环己三烯
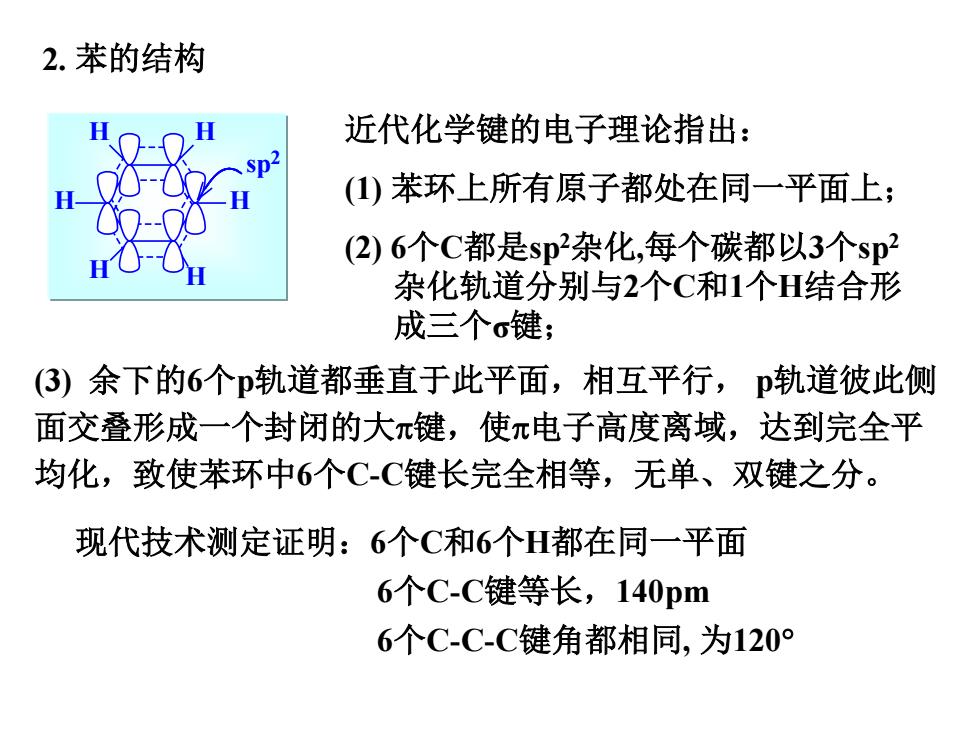
2.苯的结构 近代化学键的电子理论指出: ()苯环上所有原子都处在同一平面上; (2)6个C都是sp杂化,每个碳都以3个sp2 杂化轨道分别与2个C和1个H结合形 成三个σ键; (3)余下的6个p轨道都垂直于此平面,相互平行,p轨道彼此侧 面交叠形成一个封闭的大π键,使π电子高度离域,达到完全平 均化,致使苯环中6个C-C键长完全相等,无单、双键之分。 现代技术测定证明:6个C和6个H都在同一平面 6个C-C键等长,140pm 6个C-C-C键角都相同,为120°
2. 苯的结构 sp2 H H H H H H 近代化学键的电子理论指出: (1) 苯环上所有原子都处在同一平面上; (2) 6个C都是sp2杂化,每个碳都以3个sp2 杂化轨道分别与2个C和1个H结合形 成三个σ键; 现代技术测定证明:6个C和6个H都在同一平面 6个C-C键等长,140pm 6个C-C-C键角都相同, 为120° (3) 余下的6个p轨道都垂直于此平面,相互平行, p轨道彼此侧 面交叠形成一个封闭的大π键,使π电子高度离域,达到完全平 均化,致使苯环中6个C-C键长完全相等,无单、双键之分

根据分子轨道理论:苯分子中6个C的2pz轨道组成6个π分子轨道 能级图: 三个节面 餐要 二个节面(简并轨道) 一个节面(简并轨道:能 量相同的轨道) 无节面
根据分子轨道理论: 苯分子中6个C的2pz轨道组成6个π分子轨道 能级图: 无节面 一个节面(简并轨道:能 量相同的轨道) 二个节面(简并轨道) 三个节面 E

解释: 1.氢化热低:苯分子中形成一个闭合的大π键,π电子云高 度离域,体系能量降低而稳定。 2.易取代,不易加成:因为加成反应会破坏大π键,使稳定 的苯转变为不稳定的1,3-环己二烯,故难进行;π电子云利于 亲电试剂的进攻,取代反应不会破坏大π键而易进行
解释: 1. 氢化热低:苯分子中形成一个闭合的大π键, π电子云高 度离域,体系能量降低而稳定。 2. 易取代,不易加成:因为加成反应会破坏大π键,使稳定 的苯转变为不稳定的1,3-环己二烯,故难进行;π电子云利于 亲电试剂的进攻,取代反应不会破坏大π键而易进行