
第二章化学反应的方向 §2.1 热力学第一定律 §2.2 化学反应的热效应 §2.3 吉布斯能和化学反应的方向
第二章 化学反应的方向 § 2.1 热力学第一定律 § 2.2 化学反应的热效应 § 2.3 吉布斯能和化学反应的方向

物质A与物质B能吞发生化学反应生成新的物质? 如果反应能发生,它是放热还是吸热反应?吸收(或放 出)多少热量? 这些反应进行到什么程度为止? 这些问题都属于化学热力学的研究范畴。 热力学(thermodynamics)是研究各种形式的能量 (如:热能、电能、化学能等)转换规律的科学。它的基 础就是热力学第一定律和热力学第二定律。 化学热力学是热力学原理在化学中的应用
物质 A 与物质 B 能否发生化学反应生成新的物质 C? 如果反应能发生,它是放热还是吸热反应?吸收(或放 出)多少热量? 这些反应进行到什么程度为止? 这些问题都属于化学热力学的研究范畴。 热力学(thermodynamics)是研究各种形式的能量 (如:热能、电能、化学能等)转换规律的科学。它的基 础就是热力学第一定律和热力学第二定律。 化学热力学是热力学原理在化学中的应用
§2.1 热力学第一定律 一、 基本概念 (一)体系和环境 体系(system):热力学中被研究的对象。 体系以外并且与体系密切相关的部分称为环境 (surrounding)o 烧杯中的溶 烧杯和周围的空 液是体系。 气都属于环境
一、基本概念 体系(system):热力学中被研究的对象。 体系以外并且与体系密切相关的部分称为环境 (surrounding)。 烧杯中的溶 液是体系。 烧杯和周围的空 气都属于环境 §2.1 热力学第一定律 (一)体系和环境
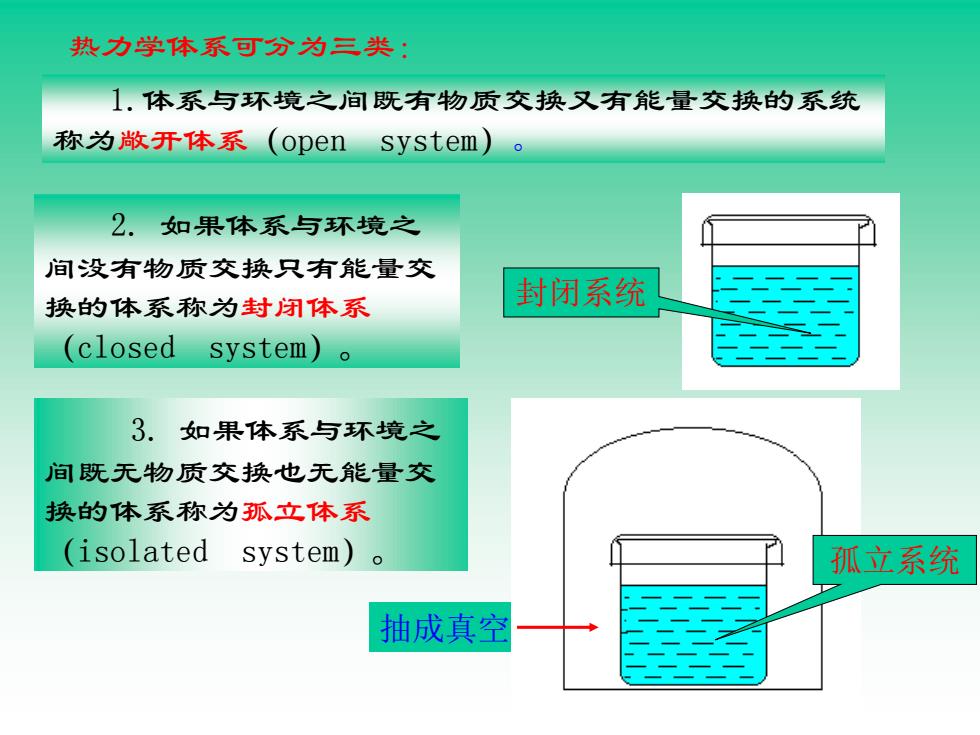
热力学体系可分为三类: 1.体系与环境之间既有物质交换又有能量交换的系统 称为敞开体系(open system) 2.如果体系与环境之 间没有物质交换只有能量交 换的体系称为封闭体系 封闭系统 (closed system)o 3.如果体系与环境之 间既无物质交换也无能量交 换的体系称为孤立体系 (isolated system)o 孤立系统 抽成真空
2. 如果体系与环境之 间没有物质交换只有能量交 换的体系称为封闭体系 (closed system)。 封闭系统 3. 如果体系与环境之 间既无物质交换也无能量交 换的体系称为孤立体系 (isolated system)。 抽成真空 孤立系统 热力学体系可分为三类: 1.体系与环境之间既有物质交换又有能量交换的系统 称为敞开体系(open system)

(三) 状态和状态函数 状态由一系列表征体系性质的物理量所确定 下来的体系的一种存在形式,称为体系的状态。 状态函数确定体系状态的物理量,称为状态国数。 例如某理想气体体系 n=2mol,p=1.013×105Pa,V=44.8dm3,T=273K 这就是一种状态。是由、p、V、T所确定下来的体 系的一种存在形式。 因而n、p、V、T都是体系的状态函数。 状态一定,则体系的状态函数一定。体系的一个或几 个状态函数发生了变化,则体系的状态发生变化
状态 由一系列表征体系性质的物理量所确定 下来的体系的一种存在形式,称为体系的状态。 状态函数 确定体系状态的物理量,称为状态函数。 例如某理想气体体系 n = 2 mol, p = 1.013 10 5 Pa, V = 44.8 dm 3 ,T = 273 K 这就是一种状态。是由 n、p、V、T 所确定下来的体 系的一种存在形式。 因而 n、p、V、T 都是体系的状态函数。 状态一定,则体系的状态函数一定。体系的一个或几 个状态函数发生了变化,则体系的状态发生变化。 (二) 状态和状态函数