第五章 Huckel分子轨道法 离 1.正常的离域 π键:m=n n66 键的类型 2.多电子 的离域π 门43 键:m>n 02s2 3.缺电子的离域π键:m<n [HC-CH-CH2]i n23 9
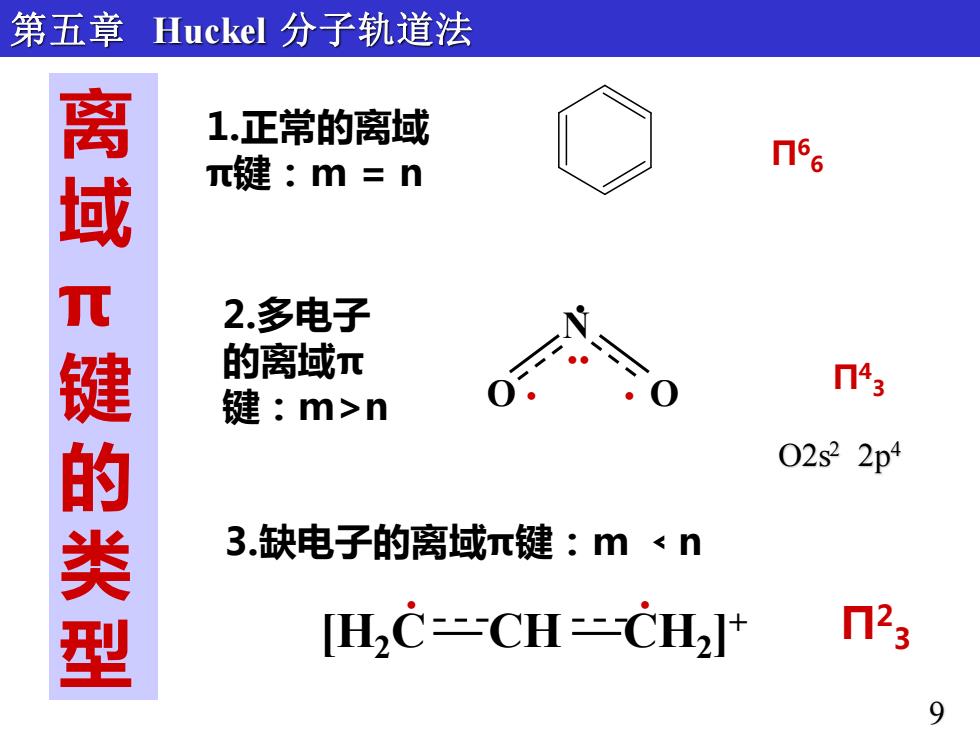
离 域 π 键 的 类 型 Π6 6 1.正常的离域 π键:m = n 2.多电子 的离域π 键:m>n 3.缺电子的离域π键:m ﹤n Π2 [H 3 2C CH CH2 ] + . . Π4 3 . . . N O O . 第五章 Huckel 分子轨道法 9 O2s2 2p4
第五章 Huckel分子轨道法 n4x3 0=C=0 nys 0 2s22p4 C:价电子层为2s22p2,碳以sp杂化轨道与每个氧原 子的2p轨道形成两个σ键 三个原子的p,轨道垂直于通过键轴的平面,形成(π,)34键 另外,三个原子的P,轨道也同样形成一个大π键(π,)34,这二个 大π键互相垂直 4x3N=N=O04y 2s22p3 2s22p4 4
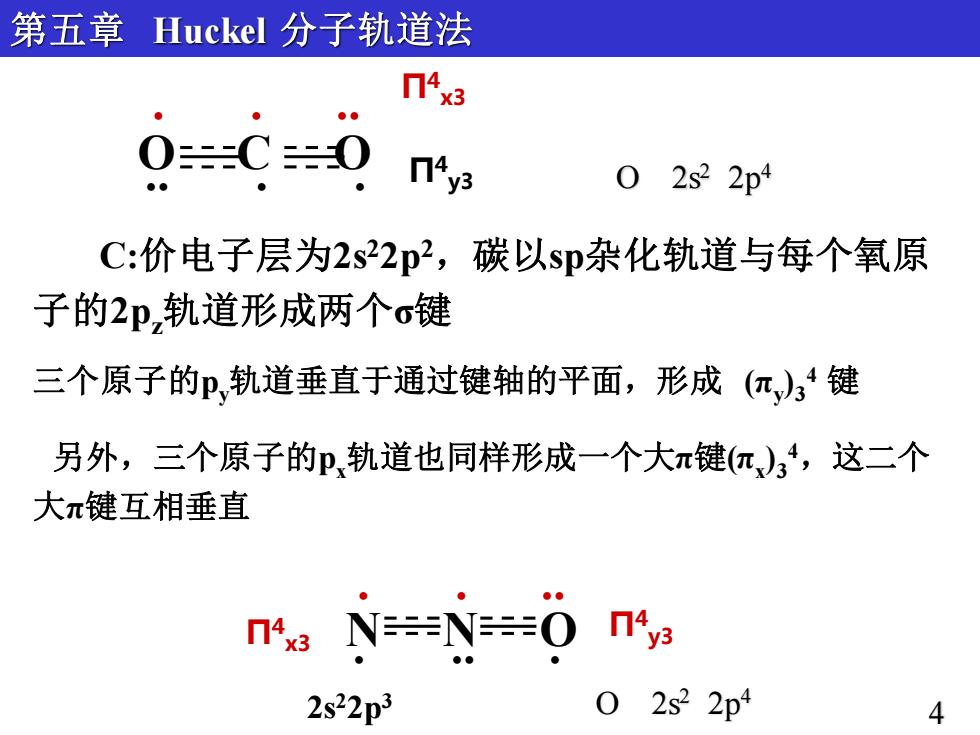
Π4 y3 O C O . . . . . . Π4 x3 Π4 Π y3 4 x3 N N O . . . . . . 第五章 Huckel 分子轨道法 C:价电子层为2s22p2,碳以sp杂化轨道与每个氧原 子的2pz轨道形成两个σ键 三个原子的py轨道垂直于通过键轴的平面,形成 (πy ) 3 4 键 另外,三个原子的px轨道也同样形成一个大π键(πx ) 3 4,这二个 大π键互相垂直 4 O 2s2 2p4 2s22p3 O 2s2 2p4
第五章Huckel分子轨道法 N2s2 2p3 02s22p'z2px2p2) NO2分子,实验测定为角形结构 ∠ONO=1329 可判断N原子采取不等性sp杂化用以形成o键,剩余 一个p轨道单占据,垂直于分子平面,与O原子平行 的p轨道形成 Ts 7
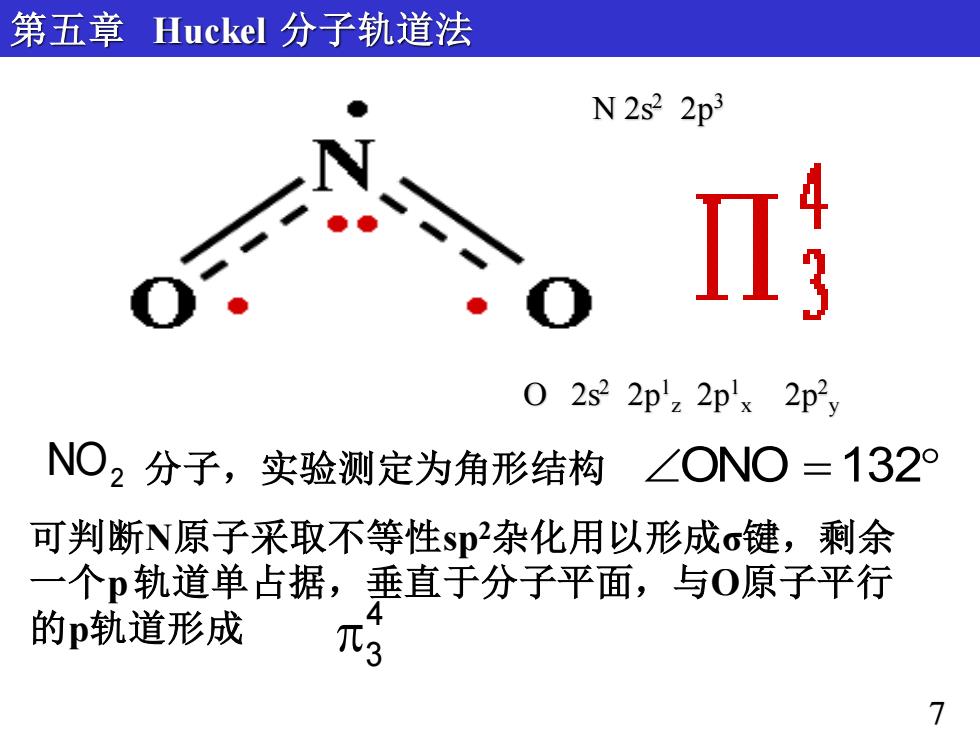
NO2 分子,实验测定为角形结构 ONO = 132 可判断N原子采取不等性sp2杂化用以形成σ键,剩余 一个p轨道单占据,垂直于分子平面,与O原子平行 的p轨道形成 4 3 第五章 Huckel 分子轨道法 7 O 2s2 2p1 z 2p1 x 2p2 y N 2s2 2p3

第五章Huckel分子轨道法 H,C-CH-CH-O n44 sp2 C 2s2 2p2 O 2s2 2p!2p's 2p2y R一 Π43 N2s2 2p3 8
Π4 4 H2C CH CH O . . . . O R C NH2 . . . Π4 3 第五章 Huckel 分子轨道法 8 sp2 C 2s2 2p2 O 2s2 2p1 z 2p1 x 2p2 y N 2s2 2p3

第五章Huckel分子轨道法 (四)无机共轭分子 1.二氧化氮NO2: sp2 N2s2 2p3 80022p 33 n43 能量的高低:33>43 此分子的结构为湾曲性;有未成对电子,应有顺磁性。 10
1. 二氧化氮 NO2 : (四)无机共轭分子 Π3 3 . . . N O O . Π4 3 . . . N O O . 能量的高低: Π4 Π 3 3 3 ﹥ 第五章 Huckel 分子轨道法 此分子的结构为湾曲性;有未成对电子,应有顺磁性。 10 sp2 N 2s2 2p3 O 2s2 2p4