
第一节 水分 水是生命活动不可缺少的物质。从提供人体能量的角度看,水不是一种营养 物质,但若从人体生存的角度看,水不仅是最大量、同时也是最重要的营养物质。 水分在食品中也具有重要的意义,它既是构成食品质量的重要内容,又是影响食 品在贮藏、流通中稳定性的最重要的因素之一。 食品中的水分是构成食品食用品质的一项重要指标。对于鲜活食品,尤其是 蔬菜水果,含水量大,细胞饱满而且膨压大,产品具有脆硬的“齿感”;而且许 多呈味物质是可溶性的,它们溶解在大量汁液中,使产品充分体现出自身的风味 品质。食品中水分含量的高低会影响食品的物理性质,如密度、比热、粘度、软 硬度等,从而影响食用时的口感、冷热感和咀嚼感等。食品的含水量还会影响食 品的形状、色泽、光泽和香气,不仅会刺激人的感觉器官,而且会影响食用者的 心理作用和条件反射,是组成食品风味的一个方面。 食品的水分含量,尤其是水分活度,直接影响食品的耐藏性。水分对食品微 生物的活动产生很大的影响,较高的水分含量有利于微生物的生长繁殖,易造成 食品的腐败变质;水分还与食品中营养成分的变化、风味物质的变化以及外观形 态的变化有着密切的关系。蛋白质的变性、脂肪的氧化酸败、淀粉的老化、维生 素的损失;香气物质的挥发;色素的分解、褐变反应、粘度的改变等都与水分相 关,水分是影响食品质量的重要因素。食品加工中水分的变化也会对加工品的稳 定性、结构质地产生较大的影响。食品加工中往往会针对不同的原料,采用不同 的方法造成食品中水分的变化,如通过干燥、利用高糖度和高盐度使食品中的水 分除去或被结合,从而有效地抑制化学变化和微生物的作用,延长食品的保藏期 和货架期。 研究水和食品的关系是食品科学的重要内容之一。 一、 水的基本性质 (一) (一) 水的结构 每个水分子是由 2 个氢原子和 1 个氧原子靠共价键结合形成的,其中原子的 排列使水分子具有极性,这种分子的极性使水分子间产生吸引力;同时,水分子 之间在氢原子和氧原子之间能形成较强的氢键作用力,这种氢键作用力比一般的 共价键作用力要小得多,但比分子间由极性等其他原因造成的作用力要大。水分 子在三维空间内形成多重氢键键合,使分子间存在很大的吸引力,从而促使水分 子之间的缔合作用,形成较大的分子聚集体——缔合分子。无论是在固态、液态 或是气态,大多数水分子一般都以不同聚集度的缔合分子形式存在。 液态水中大多数水分子不以单分子状态存在,而是以若干个水分子缔合的形 式存在,可表示成[(H2O)n]。缔合分子中的极性静电引力和氢键作用力的能量 特点决定了缔合体的结构是不稳定的,而且缔合体中包含的水分子单体的数目也 不尽相同并处于不断的变化中,一定条件下,不同的缔合体之间通过水分子的得 失处于动态平衡。 冰是由水分子有序排列形成的结晶,其中每个水分子以氢键缔合另外 4 个水 分子形成四面体结构,这 4 个水分子位于四面体的顶点,四面体中每个水分子都 参与形成另外的四面体,这样无数个四面体形成了庞大的非紧密堆积的冰晶体。 (二) (二) 水的基本性质 1.水的密度 水在 4℃时密度最大,当温度升高和降低时,水的体积膨胀
第一节 水分 水是生命活动不可缺少的物质。从提供人体能量的角度看,水不是一种营养 物质,但若从人体生存的角度看,水不仅是最大量、同时也是最重要的营养物质。 水分在食品中也具有重要的意义,它既是构成食品质量的重要内容,又是影响食 品在贮藏、流通中稳定性的最重要的因素之一。 食品中的水分是构成食品食用品质的一项重要指标。对于鲜活食品,尤其是 蔬菜水果,含水量大,细胞饱满而且膨压大,产品具有脆硬的“齿感”;而且许 多呈味物质是可溶性的,它们溶解在大量汁液中,使产品充分体现出自身的风味 品质。食品中水分含量的高低会影响食品的物理性质,如密度、比热、粘度、软 硬度等,从而影响食用时的口感、冷热感和咀嚼感等。食品的含水量还会影响食 品的形状、色泽、光泽和香气,不仅会刺激人的感觉器官,而且会影响食用者的 心理作用和条件反射,是组成食品风味的一个方面。 食品的水分含量,尤其是水分活度,直接影响食品的耐藏性。水分对食品微 生物的活动产生很大的影响,较高的水分含量有利于微生物的生长繁殖,易造成 食品的腐败变质;水分还与食品中营养成分的变化、风味物质的变化以及外观形 态的变化有着密切的关系。蛋白质的变性、脂肪的氧化酸败、淀粉的老化、维生 素的损失;香气物质的挥发;色素的分解、褐变反应、粘度的改变等都与水分相 关,水分是影响食品质量的重要因素。食品加工中水分的变化也会对加工品的稳 定性、结构质地产生较大的影响。食品加工中往往会针对不同的原料,采用不同 的方法造成食品中水分的变化,如通过干燥、利用高糖度和高盐度使食品中的水 分除去或被结合,从而有效地抑制化学变化和微生物的作用,延长食品的保藏期 和货架期。 研究水和食品的关系是食品科学的重要内容之一。 一、 水的基本性质 (一) (一) 水的结构 每个水分子是由 2 个氢原子和 1 个氧原子靠共价键结合形成的,其中原子的 排列使水分子具有极性,这种分子的极性使水分子间产生吸引力;同时,水分子 之间在氢原子和氧原子之间能形成较强的氢键作用力,这种氢键作用力比一般的 共价键作用力要小得多,但比分子间由极性等其他原因造成的作用力要大。水分 子在三维空间内形成多重氢键键合,使分子间存在很大的吸引力,从而促使水分 子之间的缔合作用,形成较大的分子聚集体——缔合分子。无论是在固态、液态 或是气态,大多数水分子一般都以不同聚集度的缔合分子形式存在。 液态水中大多数水分子不以单分子状态存在,而是以若干个水分子缔合的形 式存在,可表示成[(H2O)n]。缔合分子中的极性静电引力和氢键作用力的能量 特点决定了缔合体的结构是不稳定的,而且缔合体中包含的水分子单体的数目也 不尽相同并处于不断的变化中,一定条件下,不同的缔合体之间通过水分子的得 失处于动态平衡。 冰是由水分子有序排列形成的结晶,其中每个水分子以氢键缔合另外 4 个水 分子形成四面体结构,这 4 个水分子位于四面体的顶点,四面体中每个水分子都 参与形成另外的四面体,这样无数个四面体形成了庞大的非紧密堆积的冰晶体。 (二) (二) 水的基本性质 1.水的密度 水在 4℃时密度最大,当温度升高和降低时,水的体积膨胀

而密度变小。这种变化的主要原因是温度的变化影响了缔合水分子中氢键的结合 程度,从而改变了邻近水分子间的距离以及水分子的结合数,同时改变了水缔合 体的大小,引起水密度的变化,也会影响到水缔合体的移动性。在速冻食品的生 产和食品包装材料的选择上,都必须充分考虑到这一特点。 2.水的沸点和熔点 与结构相似的物质比较,水的沸点和熔点都相当高。 水的沸点随压力的增大而升高,在减压的情况下,水的沸点降低,这一性质特点 在食品加工中均有应用。在食品生产中利用高压可获得较高的蒸汽温度,不仅可 以使不易煮熟的食品物料迅速煮熟,同时利用高温可以起到杀菌作用;在浓缩食 品物料时,为了较好地保存食品中的一些营养成分,往往需要在较低的温度下进 行,采用适当的真空即可达到这一目的。 常压下水的熔点(冰点)是 0 ℃。但纯水在 0 ℃时并不马上结冰,通常先 被冷却成过冷状态,只有当温度降低到开始出现稳定的晶核时,或在振动的促进 下会立即向冰晶体转化并在转化过程中放出相变潜热使温度回升到 0 ℃。开始 出现稳定晶核时的温度叫过冷温度。如果外加晶核,则不必达到过冷温度就能结 冰。晶核少时由于冰晶主要围绕有限的晶核长大,因而生成的冰晶较粗大;晶核 多时生成的冰晶较小。食品冻藏时提倡速冻,可以生成较小的冰晶颗粒,减小冰 晶形成对食品结构质地的破坏,冻结时间的缩短也有利于更好地限制微生物的活 动,这些都有利于保持较好的食品品质。 当水中溶有溶质时,水的沸点升高、冰点降低。 3.水的比热 水中缔合分子的存在,需要额外的能量来破坏其中的氢键结 合力,因此水的比热较大。这一特点也使水具有一定的保温作用,使水温不易受 气温的变化而变化。 4.水的介电常数(促进电解质电离的能力) 促使电解质电离的能力在化 学上可以用介电常数来量化。某种物质的介电常数越高,其促进电解质电离的能 力也越强。20 ℃时水的介电常数为 80.36,而大多数生物体干物质的介电常数 为 2.2~4.0,物质中含水量增加时,其介电常数将明显增大。由于水的介电常数 较大,因此能促进电解质的电离。 5.作为溶剂的性质 水不仅能溶解离子型化合物,许多非离子型的有机化 合物也可与水形成氢键而溶于水中,例如醇类、醛类、酮类以及食品中的营养成 分蛋白质、糖类等;某些不溶于水的蛋白质以及脂肪等,在适当的条件下分散在 水中能形成乳浊液或胶体溶液,一定条件下这种乳浊液能稳定存在。比如牛奶中 的乳脂经均质后形成稳定的乳浊液,不易离析且容易被人体吸收;冰淇淋就是以 脂分散于水中形成的乳化态为主体的食品。 二、食品中水分的性质 各种食品都是多成分体系,它们的含水量可能各不相同,但其中水分与非水 物质间的相互作用使食品中的水分以不同的形式存在,性质也不尽相同,对食品 的耐藏性、加工特性也产生不同的影响,所以区分食品中不同形式的水分是很有 必要的。 (一)自由水和结合水 食品中的水分以各种不同的状态存在,有的学者将其分为自由态、水合态、 胶体吸润态、表面吸附态等,也有的学者称之为构成水、邻近水、多层水和体相 水等。在食品界还普遍流行着自由水和结合水的概念,这一区分在实际应用时也 较为方便
而密度变小。这种变化的主要原因是温度的变化影响了缔合水分子中氢键的结合 程度,从而改变了邻近水分子间的距离以及水分子的结合数,同时改变了水缔合 体的大小,引起水密度的变化,也会影响到水缔合体的移动性。在速冻食品的生 产和食品包装材料的选择上,都必须充分考虑到这一特点。 2.水的沸点和熔点 与结构相似的物质比较,水的沸点和熔点都相当高。 水的沸点随压力的增大而升高,在减压的情况下,水的沸点降低,这一性质特点 在食品加工中均有应用。在食品生产中利用高压可获得较高的蒸汽温度,不仅可 以使不易煮熟的食品物料迅速煮熟,同时利用高温可以起到杀菌作用;在浓缩食 品物料时,为了较好地保存食品中的一些营养成分,往往需要在较低的温度下进 行,采用适当的真空即可达到这一目的。 常压下水的熔点(冰点)是 0 ℃。但纯水在 0 ℃时并不马上结冰,通常先 被冷却成过冷状态,只有当温度降低到开始出现稳定的晶核时,或在振动的促进 下会立即向冰晶体转化并在转化过程中放出相变潜热使温度回升到 0 ℃。开始 出现稳定晶核时的温度叫过冷温度。如果外加晶核,则不必达到过冷温度就能结 冰。晶核少时由于冰晶主要围绕有限的晶核长大,因而生成的冰晶较粗大;晶核 多时生成的冰晶较小。食品冻藏时提倡速冻,可以生成较小的冰晶颗粒,减小冰 晶形成对食品结构质地的破坏,冻结时间的缩短也有利于更好地限制微生物的活 动,这些都有利于保持较好的食品品质。 当水中溶有溶质时,水的沸点升高、冰点降低。 3.水的比热 水中缔合分子的存在,需要额外的能量来破坏其中的氢键结 合力,因此水的比热较大。这一特点也使水具有一定的保温作用,使水温不易受 气温的变化而变化。 4.水的介电常数(促进电解质电离的能力) 促使电解质电离的能力在化 学上可以用介电常数来量化。某种物质的介电常数越高,其促进电解质电离的能 力也越强。20 ℃时水的介电常数为 80.36,而大多数生物体干物质的介电常数 为 2.2~4.0,物质中含水量增加时,其介电常数将明显增大。由于水的介电常数 较大,因此能促进电解质的电离。 5.作为溶剂的性质 水不仅能溶解离子型化合物,许多非离子型的有机化 合物也可与水形成氢键而溶于水中,例如醇类、醛类、酮类以及食品中的营养成 分蛋白质、糖类等;某些不溶于水的蛋白质以及脂肪等,在适当的条件下分散在 水中能形成乳浊液或胶体溶液,一定条件下这种乳浊液能稳定存在。比如牛奶中 的乳脂经均质后形成稳定的乳浊液,不易离析且容易被人体吸收;冰淇淋就是以 脂分散于水中形成的乳化态为主体的食品。 二、食品中水分的性质 各种食品都是多成分体系,它们的含水量可能各不相同,但其中水分与非水 物质间的相互作用使食品中的水分以不同的形式存在,性质也不尽相同,对食品 的耐藏性、加工特性也产生不同的影响,所以区分食品中不同形式的水分是很有 必要的。 (一)自由水和结合水 食品中的水分以各种不同的状态存在,有的学者将其分为自由态、水合态、 胶体吸润态、表面吸附态等,也有的学者称之为构成水、邻近水、多层水和体相 水等。在食品界还普遍流行着自由水和结合水的概念,这一区分在实际应用时也 较为方便

自由水也称游离水,借助毛细管作用力存在于细胞间隙、细胞液中以及制成 食品的结构组织中。自由水具有普通水的性质,容易结冰、可作溶剂,与一般的 水无本质的区别,在食品中自由水会因蒸发而减少,也会因吸湿而增加,利用加 热的方法容易把它从食品中分离出来;它可以被微生物利用,与食品的腐败变质 有重要的关系,因而直接影响食品的保藏性,食品是否被微生物感染,并不决定 于食品中水分的总含量,而仅决定于食品中自由水的含量。 结合水也称束缚水,是指与食品中一些化合物的活性基团以氢键等形式结合 的水。这种水往往是与食品中的蛋白质、淀粉、果胶物质、纤维素等成分相结合 的,但这些有机高分子物质的不同基团与水形成的氢键作用力有所不同,一般蛋 白质分子中的氨基、羧基和果胶物质中未酯化的羧基与水形成的氢键作用力大, 结合得比较牢固,称为单分子层结合水;蛋白质中的酰胺基、淀粉、果胶物质、 纤维素等分子中的羟基与水形成的氢键作用力较小,不牢固,称为半结合水或多 分子层结合水。结合水的性质与自由水有很大的区别,主要体现在以下几个方面: 1.食品中结合水的量与有机大分子极性基团的数量有比较固定的比例关系。 据测定,每 100 g 蛋白质可结合的水分平均高达 50 g、每 100 g 淀粉的持水能 力在 30~40 g 之间。 2.由于结合水被结合着,不易蒸发,所以其蒸气压比同温下普通水的蒸气 压低,因此结合水的沸点高于普通水,一般加热手段不能将其从食品分离出来; 而结合水的冰点低于普通水,使其不易结冰,甚至环境温度低于-20 ℃时还不结 冰,冰点可下降至-40 ℃,由于这一性质,使含水量很低的植物的种子和微生物 的孢子(几乎只含结合水)能在很低的温度下保持生命力,而多汁的果蔬、肉类 等组织,因含大量的自由水,在冰冻时细胞结构易被冰晶破坏,解冻时组织容易 崩溃。 3.结合水不起溶剂的作用,也不能被微生物利用;一般加热操作不易去除 结合水,所以在食品干燥操作中只有很少一部分的结合水被去除。 4.结合水对食品的风味起着重大的作用。不易去除的结合水如果被强行与 食品分离时,往往使食品的风味质量造成很大的改变。 从严格意义上说,食品的水分都是被结合着的,只是结合程度不同而已,因 此,自由水与结合水并没有严格的界限区分,一般认为自由水是以物理吸附力与 食品结合,而束缚水是以化学力与食品结合,两者合称为食品中的含水量,可以 干基表示或湿基表示,通常以质量分数来表示。 (二)平衡水分 食品总是存在于一定的环境条件中的,食品中的水分会因外界条件的改变而 变化,所以食品的含水量必须以一定的环境条件为前提才有意义。 食品中所含水分具有一定的蒸气压,外界空气中的水分也有一定的蒸气压, 根据热力学原理,只有当两者相等时,水分才能在两者之间达到平衡状态,没有 宏观上的转移。如果两者的水蒸气压不相等,也即不处于平衡状态,那么食品的 水分就会通过释放或吸收来达到与外界空气的平衡。在一定温度和湿度条件下, 当食品内部的水蒸气压与外界空气的水蒸气压达到平衡时,食品中的水分含量保 持一定的数值,即食品的平衡水分含量。 三、水分活度 (一)水分活度的概念 食品中的水分或多或少都受到不同程度的束缚,被束缚的程度越大,水形成
自由水也称游离水,借助毛细管作用力存在于细胞间隙、细胞液中以及制成 食品的结构组织中。自由水具有普通水的性质,容易结冰、可作溶剂,与一般的 水无本质的区别,在食品中自由水会因蒸发而减少,也会因吸湿而增加,利用加 热的方法容易把它从食品中分离出来;它可以被微生物利用,与食品的腐败变质 有重要的关系,因而直接影响食品的保藏性,食品是否被微生物感染,并不决定 于食品中水分的总含量,而仅决定于食品中自由水的含量。 结合水也称束缚水,是指与食品中一些化合物的活性基团以氢键等形式结合 的水。这种水往往是与食品中的蛋白质、淀粉、果胶物质、纤维素等成分相结合 的,但这些有机高分子物质的不同基团与水形成的氢键作用力有所不同,一般蛋 白质分子中的氨基、羧基和果胶物质中未酯化的羧基与水形成的氢键作用力大, 结合得比较牢固,称为单分子层结合水;蛋白质中的酰胺基、淀粉、果胶物质、 纤维素等分子中的羟基与水形成的氢键作用力较小,不牢固,称为半结合水或多 分子层结合水。结合水的性质与自由水有很大的区别,主要体现在以下几个方面: 1.食品中结合水的量与有机大分子极性基团的数量有比较固定的比例关系。 据测定,每 100 g 蛋白质可结合的水分平均高达 50 g、每 100 g 淀粉的持水能 力在 30~40 g 之间。 2.由于结合水被结合着,不易蒸发,所以其蒸气压比同温下普通水的蒸气 压低,因此结合水的沸点高于普通水,一般加热手段不能将其从食品分离出来; 而结合水的冰点低于普通水,使其不易结冰,甚至环境温度低于-20 ℃时还不结 冰,冰点可下降至-40 ℃,由于这一性质,使含水量很低的植物的种子和微生物 的孢子(几乎只含结合水)能在很低的温度下保持生命力,而多汁的果蔬、肉类 等组织,因含大量的自由水,在冰冻时细胞结构易被冰晶破坏,解冻时组织容易 崩溃。 3.结合水不起溶剂的作用,也不能被微生物利用;一般加热操作不易去除 结合水,所以在食品干燥操作中只有很少一部分的结合水被去除。 4.结合水对食品的风味起着重大的作用。不易去除的结合水如果被强行与 食品分离时,往往使食品的风味质量造成很大的改变。 从严格意义上说,食品的水分都是被结合着的,只是结合程度不同而已,因 此,自由水与结合水并没有严格的界限区分,一般认为自由水是以物理吸附力与 食品结合,而束缚水是以化学力与食品结合,两者合称为食品中的含水量,可以 干基表示或湿基表示,通常以质量分数来表示。 (二)平衡水分 食品总是存在于一定的环境条件中的,食品中的水分会因外界条件的改变而 变化,所以食品的含水量必须以一定的环境条件为前提才有意义。 食品中所含水分具有一定的蒸气压,外界空气中的水分也有一定的蒸气压, 根据热力学原理,只有当两者相等时,水分才能在两者之间达到平衡状态,没有 宏观上的转移。如果两者的水蒸气压不相等,也即不处于平衡状态,那么食品的 水分就会通过释放或吸收来达到与外界空气的平衡。在一定温度和湿度条件下, 当食品内部的水蒸气压与外界空气的水蒸气压达到平衡时,食品中的水分含量保 持一定的数值,即食品的平衡水分含量。 三、水分活度 (一)水分活度的概念 食品中的水分或多或少都受到不同程度的束缚,被束缚的程度越大,水形成
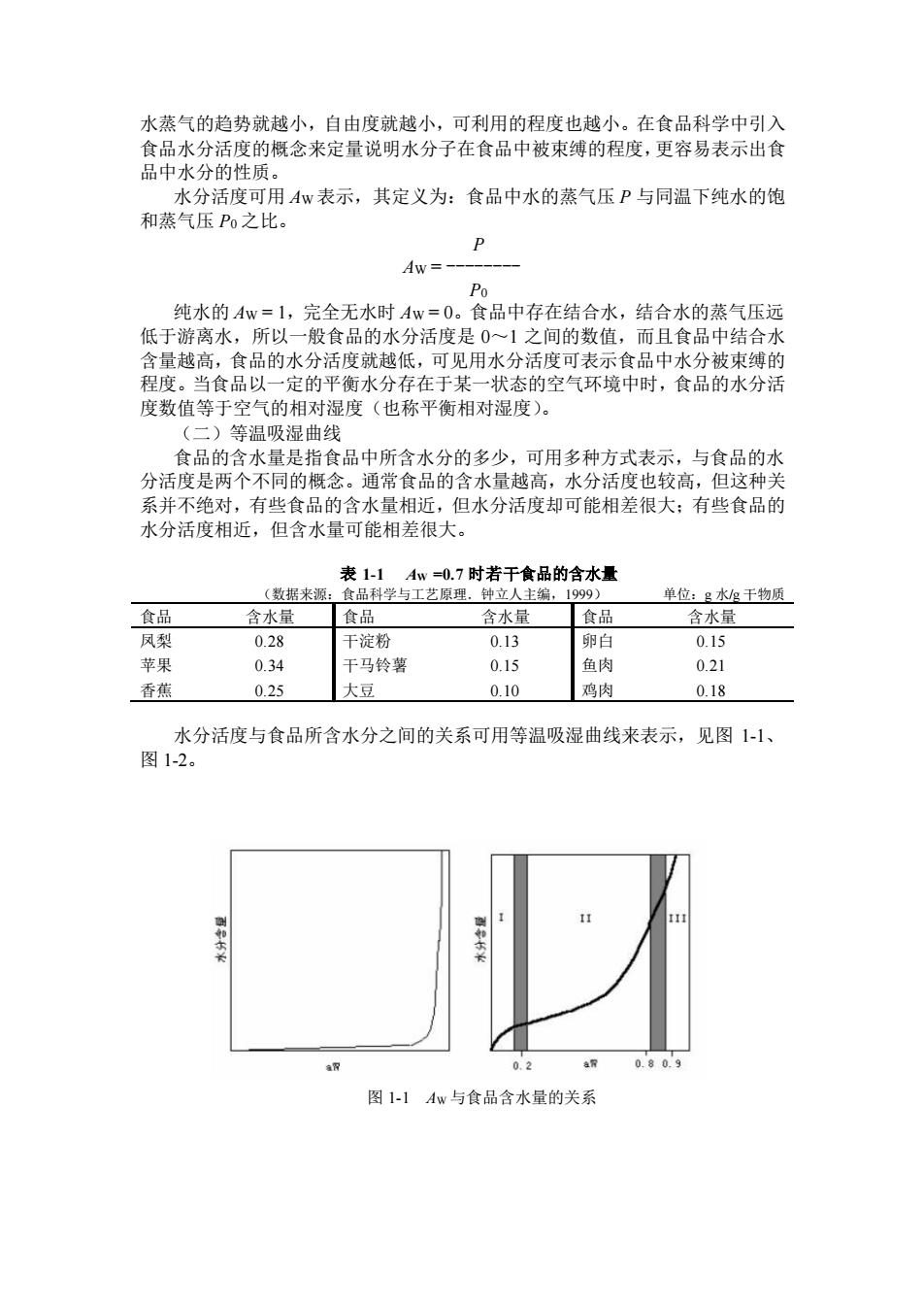
水蒸气的趋势就越小,自由度就越小,可利用的程度也越小。在食品科学中引入 食品水分活度的概念来定量说明水分子在食品中被束缚的程度,更容易表示出食 品中水分的性质。 水分活度可用 AW表示,其定义为:食品中水的蒸气压 P 与同温下纯水的饱 和蒸气压 P0 之比。 P AW = - P0 纯水的 AW = 1,完全无水时 AW = 0。食品中存在结合水,结合水的蒸气压远 低于游离水,所以一般食品的水分活度是 0~1 之间的数值,而且食品中结合水 含量越高,食品的水分活度就越低,可见用水分活度可表示食品中水分被束缚的 程度。当食品以一定的平衡水分存在于某一状态的空气环境中时,食品的水分活 度数值等于空气的相对湿度(也称平衡相对湿度)。 (二)等温吸湿曲线 食品的含水量是指食品中所含水分的多少,可用多种方式表示,与食品的水 分活度是两个不同的概念。通常食品的含水量越高,水分活度也较高,但这种关 系并不绝对,有些食品的含水量相近,但水分活度却可能相差很大;有些食品的 水分活度相近,但含水量可能相差很大。 表 1-1 AW =0.7 时若干食品的含水量 (数据来源:食品科学与工艺原理.钟立人主编,1999) 单位:g 水/g 干物质 食品 含水量 食品 含水量 食品 含水量 凤梨 0.28 干淀粉 0.13 卵白 0.15 苹果 0.34 干马铃薯 0.15 鱼肉 0.21 香蕉 0.25 大豆 0.10 鸡肉 0.18 水分活度与食品所含水分之间的关系可用等温吸湿曲线来表示,见图 1-1、 图 1-2。 图 1-1 AW 与食品含水量的关系
水蒸气的趋势就越小,自由度就越小,可利用的程度也越小。在食品科学中引入 食品水分活度的概念来定量说明水分子在食品中被束缚的程度,更容易表示出食 品中水分的性质。 水分活度可用 AW表示,其定义为:食品中水的蒸气压 P 与同温下纯水的饱 和蒸气压 P0 之比。 P AW = - P0 纯水的 AW = 1,完全无水时 AW = 0。食品中存在结合水,结合水的蒸气压远 低于游离水,所以一般食品的水分活度是 0~1 之间的数值,而且食品中结合水 含量越高,食品的水分活度就越低,可见用水分活度可表示食品中水分被束缚的 程度。当食品以一定的平衡水分存在于某一状态的空气环境中时,食品的水分活 度数值等于空气的相对湿度(也称平衡相对湿度)。 (二)等温吸湿曲线 食品的含水量是指食品中所含水分的多少,可用多种方式表示,与食品的水 分活度是两个不同的概念。通常食品的含水量越高,水分活度也较高,但这种关 系并不绝对,有些食品的含水量相近,但水分活度却可能相差很大;有些食品的 水分活度相近,但含水量可能相差很大。 表 1-1 AW =0.7 时若干食品的含水量 (数据来源:食品科学与工艺原理.钟立人主编,1999) 单位:g 水/g 干物质 食品 含水量 食品 含水量 食品 含水量 凤梨 0.28 干淀粉 0.13 卵白 0.15 苹果 0.34 干马铃薯 0.15 鱼肉 0.21 香蕉 0.25 大豆 0.10 鸡肉 0.18 水分活度与食品所含水分之间的关系可用等温吸湿曲线来表示,见图 1-1、 图 1-2。 图 1-1 AW 与食品含水量的关系
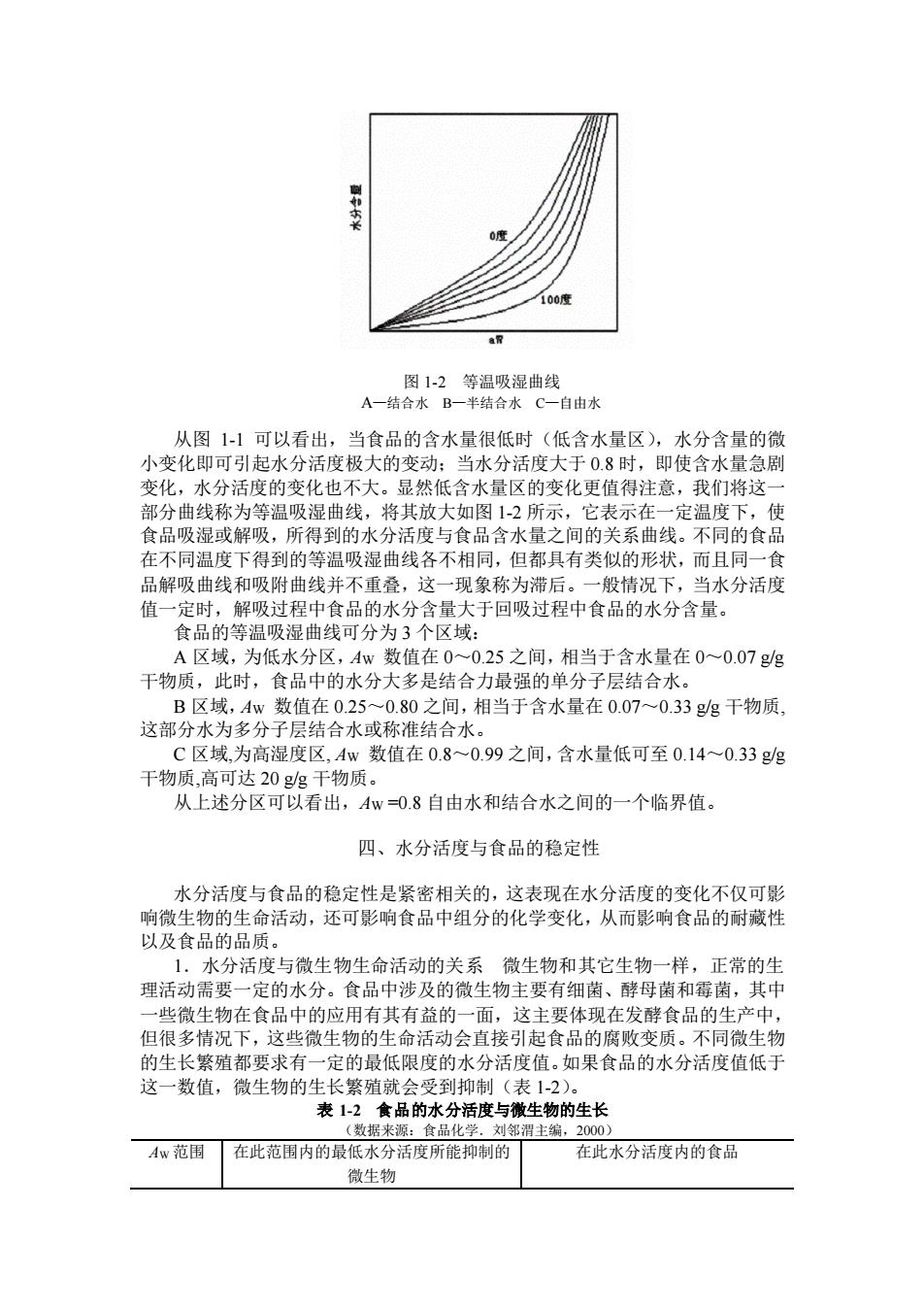
图 1-2 等温吸湿曲线 A—结合水 B—半结合水 C—自由水 从图 1-1 可以看出,当食品的含水量很低时(低含水量区),水分含量的微 小变化即可引起水分活度极大的变动;当水分活度大于 0.8 时,即使含水量急剧 变化,水分活度的变化也不大。显然低含水量区的变化更值得注意,我们将这一 部分曲线称为等温吸湿曲线,将其放大如图 1-2 所示,它表示在一定温度下,使 食品吸湿或解吸,所得到的水分活度与食品含水量之间的关系曲线。不同的食品 在不同温度下得到的等温吸湿曲线各不相同,但都具有类似的形状,而且同一食 品解吸曲线和吸附曲线并不重叠,这一现象称为滞后。一般情况下,当水分活度 值一定时,解吸过程中食品的水分含量大于回吸过程中食品的水分含量。 食品的等温吸湿曲线可分为 3 个区域: A 区域,为低水分区,AW 数值在 0~0.25 之间,相当于含水量在 0~0.07 g/g 干物质,此时,食品中的水分大多是结合力最强的单分子层结合水。 B 区域,AW 数值在 0.25~0.80 之间,相当于含水量在 0.07~0.33 g/g 干物质, 这部分水为多分子层结合水或称准结合水。 C 区域,为高湿度区, AW 数值在 0.8~0.99 之间,含水量低可至 0.14~0.33 g/g 干物质,高可达 20 g/g 干物质。 从上述分区可以看出,AW =0.8 自由水和结合水之间的一个临界值。 四、水分活度与食品的稳定性 水分活度与食品的稳定性是紧密相关的,这表现在水分活度的变化不仅可影 响微生物的生命活动,还可影响食品中组分的化学变化,从而影响食品的耐藏性 以及食品的品质。 1.水分活度与微生物生命活动的关系 微生物和其它生物一样,正常的生 理活动需要一定的水分。食品中涉及的微生物主要有细菌、酵母菌和霉菌,其中 一些微生物在食品中的应用有其有益的一面,这主要体现在发酵食品的生产中, 但很多情况下,这些微生物的生命活动会直接引起食品的腐败变质。不同微生物 的生长繁殖都要求有一定的最低限度的水分活度值。如果食品的水分活度值低于 这一数值,微生物的生长繁殖就会受到抑制(表 1-2)。 表 1-2 食品的水分活度与微生物的生长 (数据来源:食品化学.刘邻渭主编,2000) AW 范围 在此范围内的最低水分活度所能抑制的 微生物 在此水分活度内的食品
图 1-2 等温吸湿曲线 A—结合水 B—半结合水 C—自由水 从图 1-1 可以看出,当食品的含水量很低时(低含水量区),水分含量的微 小变化即可引起水分活度极大的变动;当水分活度大于 0.8 时,即使含水量急剧 变化,水分活度的变化也不大。显然低含水量区的变化更值得注意,我们将这一 部分曲线称为等温吸湿曲线,将其放大如图 1-2 所示,它表示在一定温度下,使 食品吸湿或解吸,所得到的水分活度与食品含水量之间的关系曲线。不同的食品 在不同温度下得到的等温吸湿曲线各不相同,但都具有类似的形状,而且同一食 品解吸曲线和吸附曲线并不重叠,这一现象称为滞后。一般情况下,当水分活度 值一定时,解吸过程中食品的水分含量大于回吸过程中食品的水分含量。 食品的等温吸湿曲线可分为 3 个区域: A 区域,为低水分区,AW 数值在 0~0.25 之间,相当于含水量在 0~0.07 g/g 干物质,此时,食品中的水分大多是结合力最强的单分子层结合水。 B 区域,AW 数值在 0.25~0.80 之间,相当于含水量在 0.07~0.33 g/g 干物质, 这部分水为多分子层结合水或称准结合水。 C 区域,为高湿度区, AW 数值在 0.8~0.99 之间,含水量低可至 0.14~0.33 g/g 干物质,高可达 20 g/g 干物质。 从上述分区可以看出,AW =0.8 自由水和结合水之间的一个临界值。 四、水分活度与食品的稳定性 水分活度与食品的稳定性是紧密相关的,这表现在水分活度的变化不仅可影 响微生物的生命活动,还可影响食品中组分的化学变化,从而影响食品的耐藏性 以及食品的品质。 1.水分活度与微生物生命活动的关系 微生物和其它生物一样,正常的生 理活动需要一定的水分。食品中涉及的微生物主要有细菌、酵母菌和霉菌,其中 一些微生物在食品中的应用有其有益的一面,这主要体现在发酵食品的生产中, 但很多情况下,这些微生物的生命活动会直接引起食品的腐败变质。不同微生物 的生长繁殖都要求有一定的最低限度的水分活度值。如果食品的水分活度值低于 这一数值,微生物的生长繁殖就会受到抑制(表 1-2)。 表 1-2 食品的水分活度与微生物的生长 (数据来源:食品化学.刘邻渭主编,2000) AW 范围 在此范围内的最低水分活度所能抑制的 微生物 在此水分活度内的食品