
2,二军化成(©⊙ 固体二氧化碳 干冰 经典的分子结构:O=C=0 C=O双键键长124pm(在CH3-C-CH中) C三O叁键键长113pm CO2中,碳、氧之间键长116pm C:sp杂化
2.二氧化碳 (CO2 ) 4 3 Π :O C O : 经典的分子结构:O=C=O O C=O双键键长124pm (在CH3 -C-CH3中) C O叁键键长113pm CO2中,碳、氧之间键长116pm C:sp杂化 固体二氧化碳 干冰
.瑞形其品 CO2溶于水,大部分CO2H20, 极小部分HCO3 H,CO,-H+HCO K94410r HCO,-H'+CO K9=4710 CO,2的结构: C032(6+3×8+2=32e)与BF3(5+3×9=32e) 为等电子体。 C:sp杂化
3.碳酸及其盐 CO2溶于水,大部分CO2 •H2O, 极小部分H2CO3 CO3 2-的结构: CO3 2- (6+3×8+2=32e- )与BF3 (5+3×9=32e- ) 为等电子体。 C:sp2杂化 C O O O 2- 6 Π 4 -7 1 - H2CO3 H + HCO3 = 4.4×10 + K -11 2 2- 3 - HCO3 H + CO = 4.7×10 + K
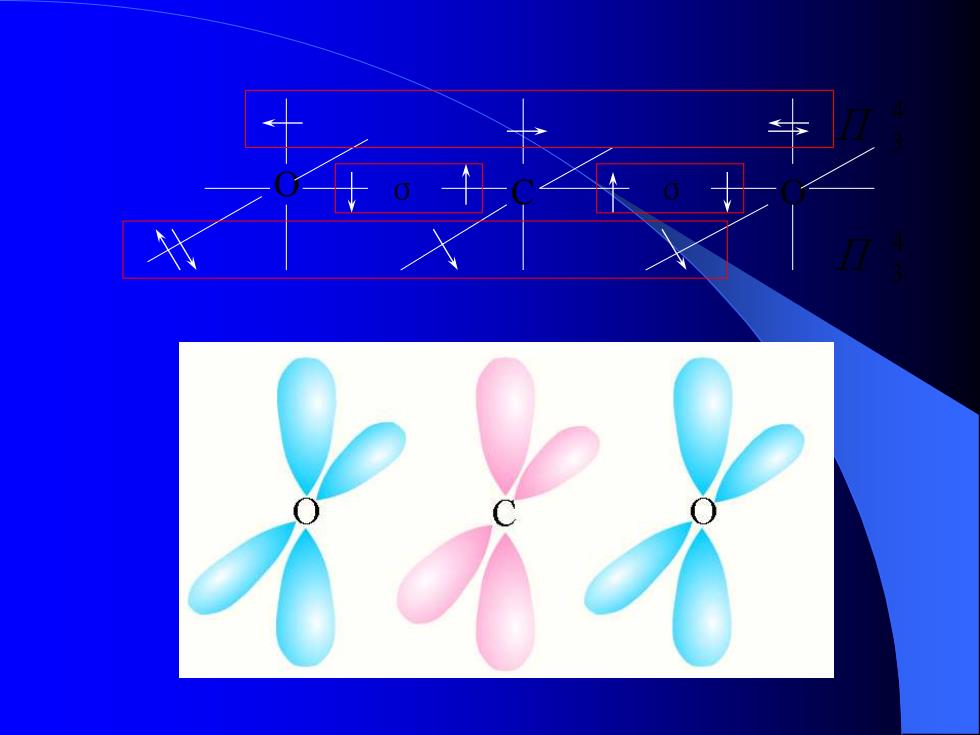
O σ C σ O 4 3 Π 4 3 Π

金属离子加入可溶性碳酸盐时,生成 沉淀的类型: ①氢氧化物碱性较强的金属离子与之反应生 成碳酸盐沉淀。 例如:Ba2+、Sr2+、Ca2+和Ag等。 Ba24+CO→BaCO(s ②氢氧化物碱性较弱的金属离子与之反应生 成碳酸羟盐(碱式碳酸盐)沉淀。 例如:Pb2+、Bi3+、Cu2+、Cd2+、Zn2+ Hg2+、Co2+、Ni2+和Mg2+等
① 氢氧化物碱性较强的金属离子与之反应生 成碳酸盐沉淀。 例如:Ba2+ 、Sr2+ 、Ca2+和Ag+等。 金属离子加入可溶性碳酸盐时,生成 沉淀的类型: Ba CO BaCO (s) 3 2- 3 2+ + ⎯→ ②氢氧化物碱性较弱的金属离子与之反应生 成碳酸羟盐(碱式碳酸盐)沉淀。 例如:Pb2+ 、Bi3+ 、Cu2+ 、Cd2+ 、Zn2+ 、 Hg2+ 、Co2+ 、Ni2+和Mg2+等

2Mg+2CO,+H,O-Mg,(OH),CO(s)00 2Cu2+2CO+H,O-Cu,(OH)CO (S)C0 ③水解性强、两性的金属离子与之反应生 成氢氧化物沉淀例如:A13+、Fe3+、Cr3+ Sn2*、Sn4+和Sb3+等。 2AI+3CO+3H,Q-2Al(OH)(S)13C0 (g
③ 水解性强、两性的金属离子与之反应生 成氢氧化物沉淀。例如:Al3+ 、Fe3+ 、Cr3+ 、 Sn2+ 、Sn4+和Sb3+等。 2Al 3CO 3H O 2Al(OH) (s) 3CO (g) 2 3 2 2- 3 3 + + + + 2Mg 2CO H O Mg (OH) CO (s) CO (g) 2 2 2 3 2 2- 3 2 + + + + 2Cu 2CO H O Cu (OH) CO (s) CO (g) 2 2 2 3 2 2- 3 2 + + + +