
练习 例:分别计算BasO4在纯水和0.01mol/LNaNO3溶液中 的溶解度 解:已知Ksp(Baso.)=1.1×10-07G=y0=067 BaSO.在水中溶解度 S=Ksp (BaSo)=1.1x1010=1.0x10-mol/L BaSO,在0.01mol1/LNaNO,溶液中溶解度 S= 1.1×100 =1.57×103mol/L 0.67×0.67
练习 例:分别计算BaSO4在纯水和0.01mol/LNaNO3溶液中 的溶解度 解: 10 ( ) 1.1 10 4 − 已知KSP BaSO = 2 0.67 4 2+ = − = Ba SO S K mol L BaSO S P BaSO 1.1 10 1.0 10 / 1 0 5 4 4 − − = ( ) = = 在水中溶解度 mol L K S BaSO mol LNaNO B a S O S P BaSO 1.57 10 / 0.67 0.67 1.1 10 0.01 / 5 0 1 0 4 3 2 4 2 4 − − = = = + − ( ) 在 溶液中溶解度

练习 例: PbS04在不同浓度Na2S04溶液中溶解度变化 C(mol/L) 0 0.001 0.01 0.02 0.04 0.10 0.20 (mmol/L 0.15 0.024 0.016 0.014 0.013 0.016 0.023 讨论: Ca,so,=0-0.04mol/L时,Ca,so↑,Spso↓ 一同离子效应为主 Ca,so,>0.04m0lIL时,Ca,so↑,Srso↑ →盐效应为主
练习 例: 讨论: 同离子效应为主 时, , = 2 4 2 4 4 0 ~ 0.04 / CNa S O mol L CNa S O SPbSO 盐效应为主 时, , 2 4 2 4 4 0.04 / CNa S O mol L CNa S O SPbSO C(mol/L) 0 0.001 0.01 0.02 0.04 0.10 0.20 S(mmol/L) 0.15 0.024 0.016 0.014 0.013 0.016 0.023 PbSO4在不同浓度Na2 SO4溶液中溶解度变化

3.酸效应:溶液酸度对沉淀溶解度的影响称为~ 讨论: √酸度对强酸型沉淀物的溶解度影响不大, 但对弱酸型或多元酸型沉淀物的溶解度影响较大 pHI,[H+]1,St 回 注: 因为酸度变化,构晶离子会与溶液中的H+或OH反 应,降低了构晶离子的浓度,使沉淀溶解平衡移向 溶解,从而使沉淀溶解度增大
3. 酸效应:溶液酸度对沉淀溶解度的影响称为~ 讨论: ✓ 酸度对强酸型沉淀物的溶解度影响不大, ✓ 但对弱酸型或多元酸型沉淀物的溶解度影响较大 pH↓,[H+]↑,S↑ 注: 因为酸度变化,构晶离子会与溶液中的H+或OH-反 应,降低了构晶离子的浓度,使沉淀溶解平衡移向 溶解,从而使沉淀溶解度增大
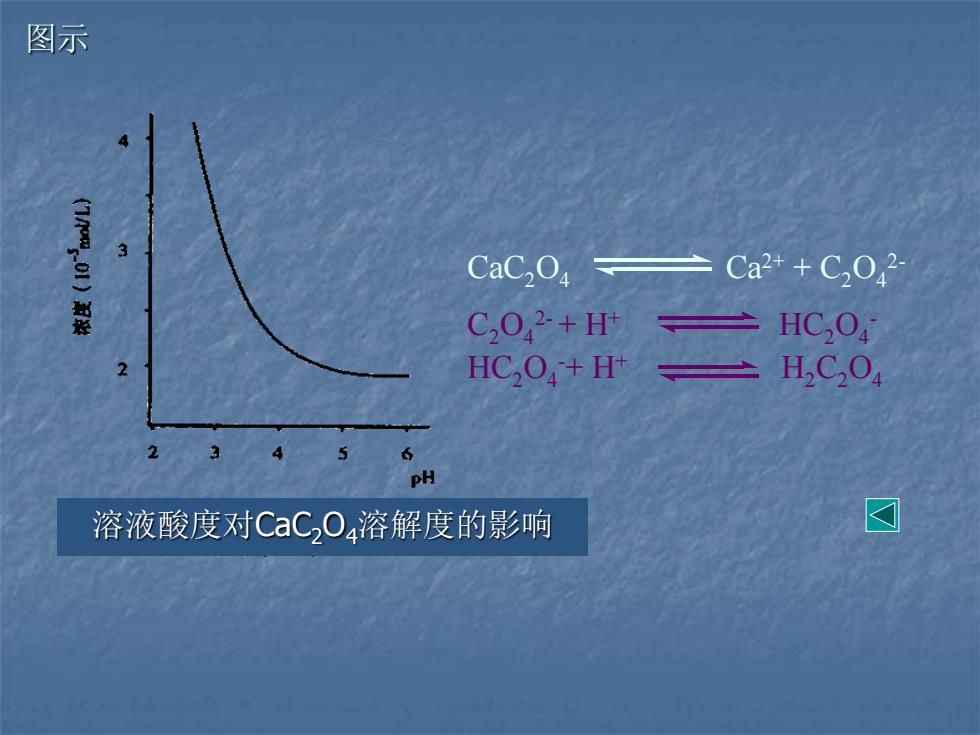
图示 CaC,O Ca2++C2042 C20,2+H HC2O HC,O+H" HC204 PH 溶液酸度对CaC,O4溶解度的影响 ☒
图示 溶液酸度对CaC2O4溶解度的影响 CaC2O4 Ca2+ + C2O4 2- C2O4 2- + H+ HC2O4 - HC2O4 -+ H+ H2C2O4

练习 例:试比较pH=2.0和pH=4.0的条件下CaC2O4的沉 淀 解:已资解度-4×10,Ka=59×10,K=64×10 C,0] Kal'Ka2 IC,O IH'P+Ka[H']+KaKa2 acoi →1o,0I=90的-c,oi1=y K-1c1e01-0的-=k。&aS →S= pH=2.0→62=0.0054,S=6.1×10mol/L pH=4.0→62=0.39,S=7.2×10-mol/L
练习 例:试比较 pH = 2.0和 pH = 4.0的条件下CaC2O4的沉 淀 解: 溶解度。 5 2 2 1 9 ( ) 4 10 5.9 10 6.4 10 2 4 − − − 已知KSP CaC O = ,Ka = ,Ka = − − = + + = = − + + − 2 2 4 2 2 4 1 [ ]' [ ] [ ] [ ] 1 1 2 2 1 2 2 2 4 2 2 4 a a a C O a a C O H K H K K K K C O C O [ ] ' [ ] [ ]' 2 2 4 2 2 4 2 2 4 2 2 2 4 2 4 C O S C O C O C O C O = = − = − − − − 2 2 2 4 2 2 2 4 ' 2 ' [ ][ ] [ ][ ]' 2 2 4 2 2 4 2 2 4 K S Ca C O K K Ca C O S P C O C O S P C O S P = = = = − = − − + − + − − − = = 2 2 4 2 2 4 ' SP C O C O SP K K S pH 2.0 0.0054 S' 6.1 10 mol / L 4 2 − = = , = pH 4.0 0.39 S' 7.2 10 mol / L 5 2 − = = , =