
第五章 化学平衡 广东工业大学轻化学院
第五章 化学平衡 广东工业大学轻化学院

摩尔反应吉布斯函数与反应进度的关系 恒温恒压下,dG=∑4dng dng vadg 则dG=∑V4d5→(6G/a5)hn=∑Vs“s=A,Gm A=-△,Gm=-(6G/a5)np 5/mol=1,系统只有产物; 5/mol=0,系统只有反应物; 0<5/mol<1,系统反应物和产物共存
摩尔反应吉布斯函数与反应进度的关系 r m T p r m B T p B B B B B B B B B B A G G dG d G G dG dn dn d , , 则 恒温恒压下, 系统反应物和产物共存。 系统只有反应物; 系统只有产物; 0 / 1, / 0, / 1, mol mol mol
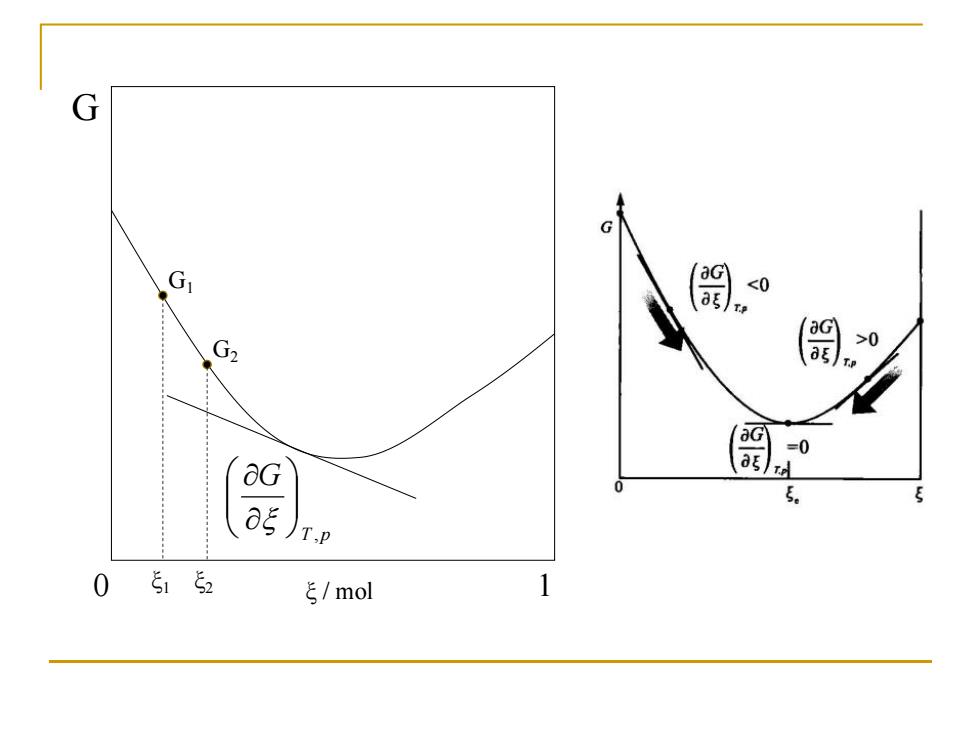
G G <0 ∂G >0 aG =0 5. ag T,p 0 5152 /mol
0 1 T p G , G G1 G2 ξ1 ξ2 ξ / mol

a4+bB →cC+dD G,=5(c4e+d:4o)+(-5ia44+b4a) G2=52(cc+d4o)+(1-52au4+b4a) △G=△5(cc+d·4D)-△5(a4A+b4B) 5=0时,只有反应物;5=1时,只有产物:0<5<1时,反应物和产物共存。 AG=AG =(ee+d:4o)-(a4,+b:4a) 单位进度的反应吉布斯函数变
r m C D A B B B C D A B C D A B C D A B c d a b G G G c d a b G c d a b G c d a b 0时,只有反应物; 1时,只有产物;0 1时,反应物和产物共存。 1 1 2 2 2 1 1 1 aA bB cC dD 单位进度的反应吉布斯函数变

摩尔反应吉布斯函数与化学反应亲和势 吉布斯函数判据 <自发 △,Gm≤0 恒温恒压、非体积功为零) =平衡 定义 A=-△,Gm A称为化学亲和势,简称亲和势。是在恒温恒压及非 体积功为零时化学反应进行的推动力。 A>0化学反应自发进行;A=0反应处于平衡;A<0反 应不能自发进行,而是逆向自发进行
摩尔反应吉布斯函数与化学反应亲和势 r m r m A G G 定义 恒温恒压、非体积功为零 平衡 自发 吉布斯函数判据 0 A称为化学亲和势,简称亲和势。是在恒温恒压及非 体积功为零时化学反应进行的推动力。 A>0化学反应自发进行;A=0反应处于平衡;A<0反 应不能自发进行,而是逆向自发进行