
p-π共轭体系: +C: ACB-ACH>AC 电负性越大的电子,+C效应越 同族元素: +c:cAc Acc 主量子数越大,原子半径越大,p轨道与双键中的 π轨道重叠越困难,电子离域程度小,十C越小。 共轭效应与诱导效应在一个分子中往往是并存的, 有时两种作用的方向是相反的。 静态时: (分子没有参加反应)一I>+C cLec 动态时: (分子处于反应中) +c>-1&t8
p - π共轭体系: +C: C C NR2 > C C OH > C C F 电负性越大的电子,+C 效应越 同族元素: 小 +C: C C F C C Cl C C Br C C I 主量子数越大,原子半径越大,p 轨道与双键中的 π轨道重叠越困难,电子离域程度小,+C 越小。 共轭效应与诱导效应在一个分子中往往是并存的, 有时两种作用的方向是相反的. 静态时: (分子没有参加反应)-I > +C C C Cl δ δ C C Cl δ δ +C > -I 动态时: (分子处于反应中〕

2.超共轭效应(Hyperconjugation 当C一H键与双键碳相连时, C一H键的强度减弱,H原子的 活性增加。 羰基化合物的α一C原子 的H原子在取代反应中是活泼 的 H Ho 0-0 σ-π超共轭体系
2. 超共轭效应(Hyperconjugation) H C H H CH CH2 当C-H键与双键碳相连时, C-H键的强度减弱,H原子的 活性增加。 H C H H CH O 羰基化合物的α-C 原子 的H原子在取代反应中是活泼 的 C C C p p sp3 C C H H H C H H H σ π σ σ H1s -超共轭体系
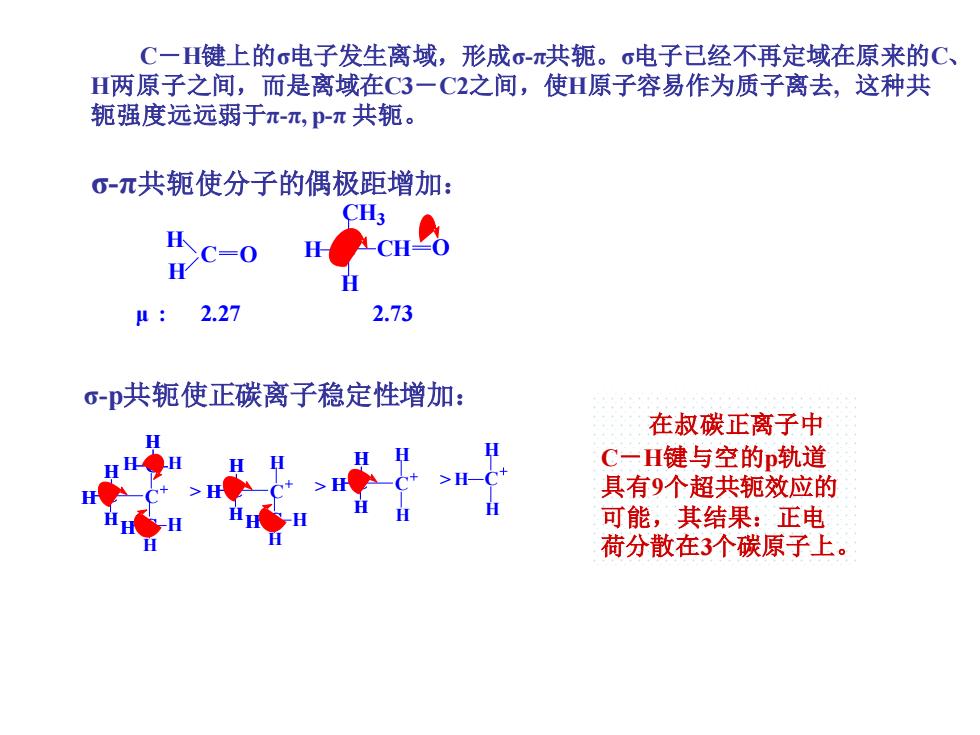
C一H键上的σ电子发生离域,形成σ-共轭。σ电子已经不再定域在原来的C、 H两原子之间,而是离域在C3一C2之间,使原子容易作为质子离去,这种共 轭强度远远弱于π-π,p-π共轭。 σ-π共轭使分子的偶极距增加: CH3 H C-0 μ:2.27 2.73 σ-p共轭使正碳离子稳定性增加: 在叔碳正离子中 C一H键与空的p轨道 具有9个超共轭效应的 可能,其结果:正电 荷分散在3个碳原子上
C-H键上的σ电子发生离域,形成σ-π共轭。σ电子已经不再定域在原来的C、 H两原子之间,而是离域在C3-C2之间,使H原子容易作为质子离去, 这种共 轭强度远远弱于π-π, p-π 共轭。 σ-π共轭使分子的偶极距增加: C O H H H C CH3 H CH O μ : 2.27 2.73 σ-p共轭使正碳离子稳定性增加: H C C H H C H H H H C H H > H C C H HH C H H > H H C C H H > H H C H H H 在叔碳正离子中 C-H键与空的p轨道 具有9个超共轭效应的 可能,其结果:正电 荷分散在3个碳原子上
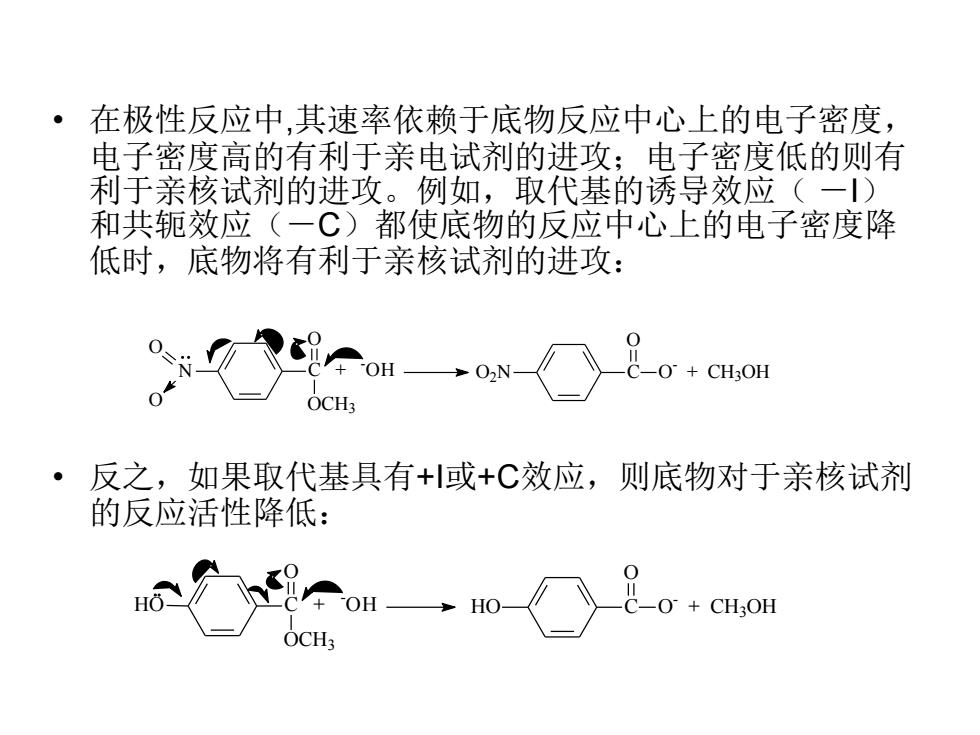
在极性反应中,其速率依赖于底物反应中心上的电子密度, 电子密度高的有利于亲电试剂的进攻;电子密度低的则有 利于亲核试剂的进攻。例如,取代基的诱导效应(一) 和共轭效应(一C)都使底物的反应中心上的电子密度降 低时,底物将有利于亲核试剂的进攻: 02N CH3OH 。 反之,如果取代基具有+或+C效应,则底物对于亲核试剂 的反应活性降低: HO- O+CH3OH OCH
• 在极性反应中,其速率依赖于底物反应中心上的电子密度, 电子密度高的有利于亲电试剂的进攻;电子密度低的则有 利于亲核试剂的进攻。例如,取代基的诱导效应( -I) 和共轭效应(-C)都使底物的反应中心上的电子密度降 低时,底物将有利于亲核试剂的进攻: • 反之,如果取代基具有+I或+C效应,则底物对于亲核试剂 的反应活性降低: N C + -OH O OCH3 O O O2N C O - + CH3OH O HO C + - OH O OCH3 HO C O - + CH3OH O
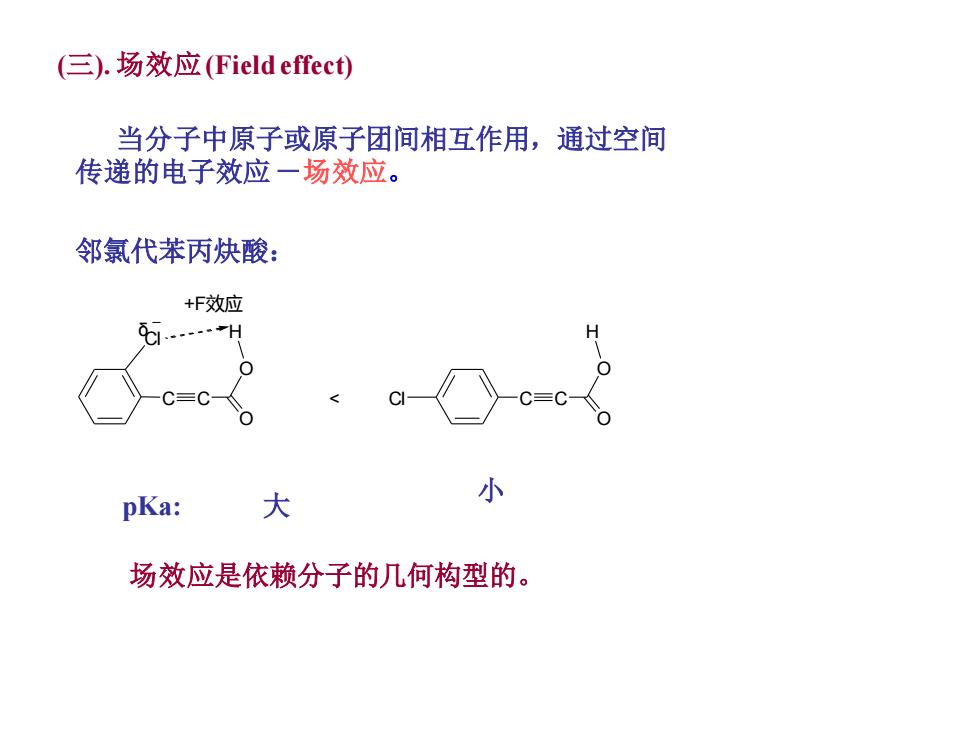
(三).场效应(Field effect) 当分子中原子或原子团间相互作用,通过空间 传递的电子效应一场效应。 邻氯代苯丙炔酸: +F效应 6…H O C=C〈 SC- 小 pKa: 大 场效应是依赖分子的几何构型的
(三). 场效应(Field effect) 当分子中原子或原子团间相互作用,通过空间 传递的电子效应-场效应。 邻氯代苯丙炔酸: pKa: 大 小 场效应是依赖分子的几何构型的。 C C < δ +F效应 O O H Cl C C O O H Cl