
例 题 例2:用氧化值法写出疏化亚铜与硝酸反应的方程式 6-(-2)=8×3=24 3Cu2S+22NO3→6Cu(N03)2+3H2S04+10N0 2-(5))=-3×10=30 (2-1)×2=2×3=6 区别:离子电子法只适用于配平水溶液中有介质参 加的复杂反应;对于一般简单的氧化还原反应氧化值法 较迅速且不限于水溶液中的反应
例 题 例2:用氧化值法写出 硫化亚铜与硝酸反应的方程式 Cu2S + HNO3 → Cu(NO3)2 + H2SO4 + NO (2-1) ×2 = 2 ×10 = -30 6 -(-2 )= 8 ×3= 24 3 22 6 10 + H2O 2 -(5 )= -3 ×3= 6 3 8 区别:离子-电子法只适用于配平水溶液中有介质参 加的复杂反应;对于一般简单的氧化还原反应氧化值法 较迅速且不限于水溶液中的反应

电极电势及其应用 ○原电池 ●电极电势和标准电极电势 ◆影响电极电势的因素 ⊙电极电势的应用
电极电势及其应用 ◎原电池 ●电极电势和标准电极电势 ◆影响电极电势的因素 ◎电极电势的应用

1【 原电池(primary cell) 实验: Zn与CuSO溶液的置换反应 Zn Zn棒逐渐溶解 CS0 现象 溶液的天蓝色减退 有红棕色疏松的铜 在Zn棒表面析出 所发生的反应 溶液的温度渐升 Zn-2e→Zn2+ Cu 2++2e →Cu Zn+Cu2+→Cu+Zn2+
原电池(primary cell) 现象 Zn棒逐渐溶解 溶液的天蓝色减退 有红棕色疏松的铜 在Zn棒表面析出 溶液的温度渐升 Zn-2e→Zn2+ Cu 2++2e →Cu 所发生的反应 Zn+ Cu 2+ →Cu +Zn2+ 实 验: Zn与CuSO4溶液的置换反应 CuSO4 Zn
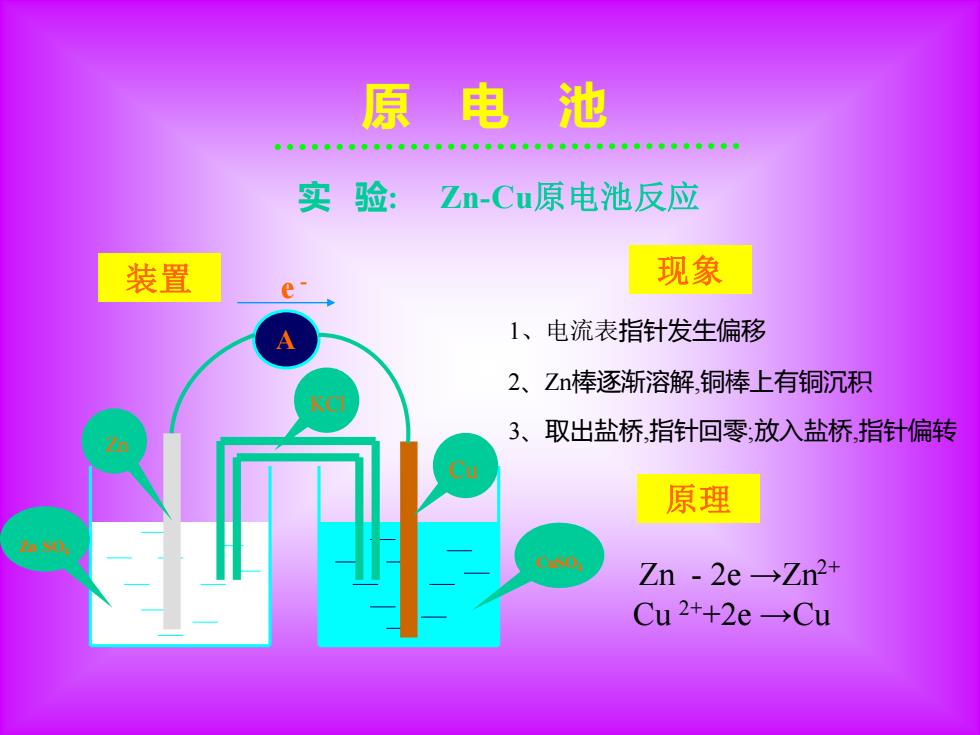
原电池 实验:Zm-Cu原电池反应 装置 现象 1、电流表指针发生偏移 2、Zn棒逐渐溶解,铜棒上有铜沉积 3、取出盐桥,指针回零放入盐桥,指针偏转 原理 Zn-2e→Zn2+ Cu2++2e→Cu
原 电 池 实 验: Zn-Cu原电池反应 3、取出盐桥,指针回零;放入盐桥,指针偏转 1、电流表指针发生偏移 2、Zn棒逐渐溶解,铜棒上有铜沉积 Cu CuSO4 Zn SO4 Zn A e - KCl 装置 现象 原理 Zn - 2e →Zn2+ Cu 2++2e →Cu
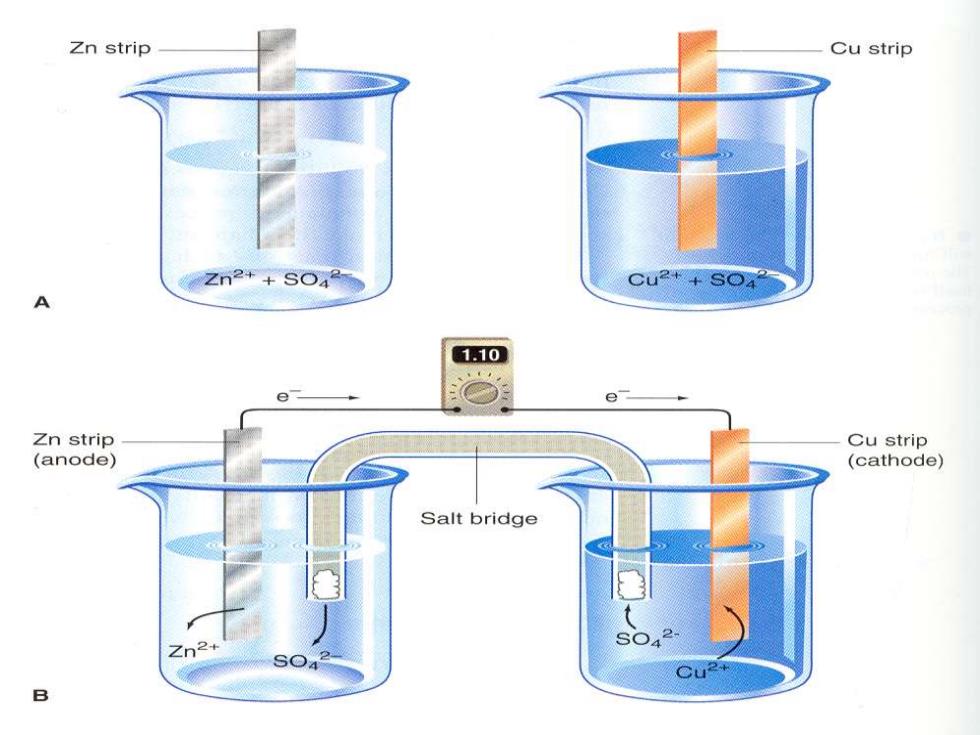
Zn strip Cu strip Zn2++SO u2++G A 1.10 e Zn strip Cu strip (anode) (cathode)】 Salt bridge Zn2+ SO ◇