
·价键理论继承了Lewis共用电子对的概念。 ·以量子力学为基础。 ·揭示了共价键的本质一原子轨道重叠, 原子核间电子概率密度大吸引原子核而成键。 无机化学电子教菜
• 价键理论继承了Lewis共用电子对的概念。 • 以量子力学为基础。 • 揭示了共价键的本质——原子轨道重叠, 原子核间电子概率密度大吸引原子核而成键
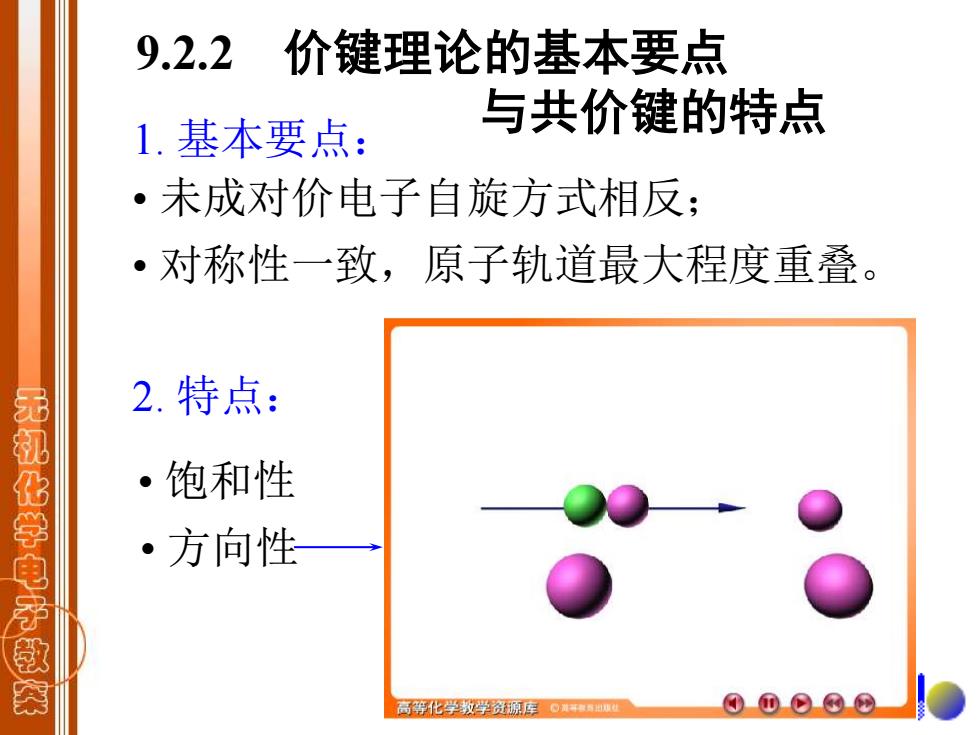
9.2.2 价键理论的基本要点 1.基本要点: 与共价键的特点 ·未成对价电子自旋方式相反; ·对称性一致,原子轨道最大程度重叠。 2.特点: 无机化学电子救 ·饱和性 ·方向性 高等化学数学资源库。: 00⊙©⊙
1. 基本要点: • 未成对价电子自旋方式相反; • 对称性一致,原子轨道最大程度重叠。 2. 特点: • 方向性 • 饱和性 9.2.2 价键理论的基本要点 与共价键的特点
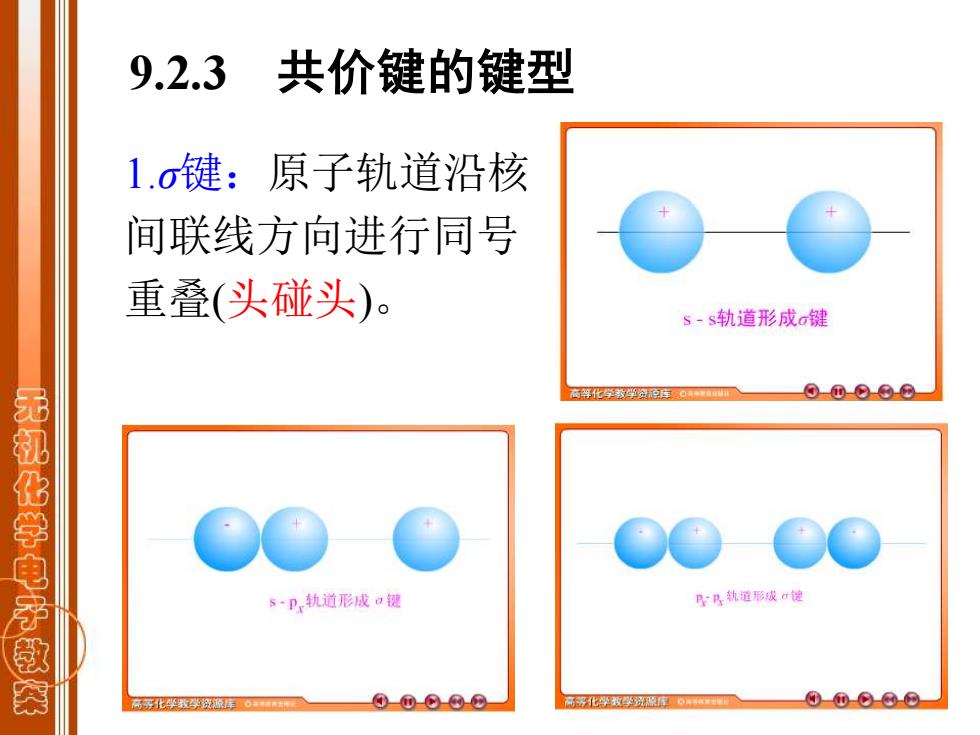
9.2.3 共价键的键型 1.σ键:原子轨道沿核 间联线方向进行同号 重叠(头碰头)。 s-s轨道形成a键 高等化学教学会的年白* 00-⊙-8-0 无机化学电子 s·p,轨道形成a键 店具轨道形成:键 茵 化华数学袋源年。 @0⊙@0 00-0-@-⊙
1.σ键:原子轨道沿核 间联线方向进行同号 重叠(头碰头)。 9.2.3 共价键的键型
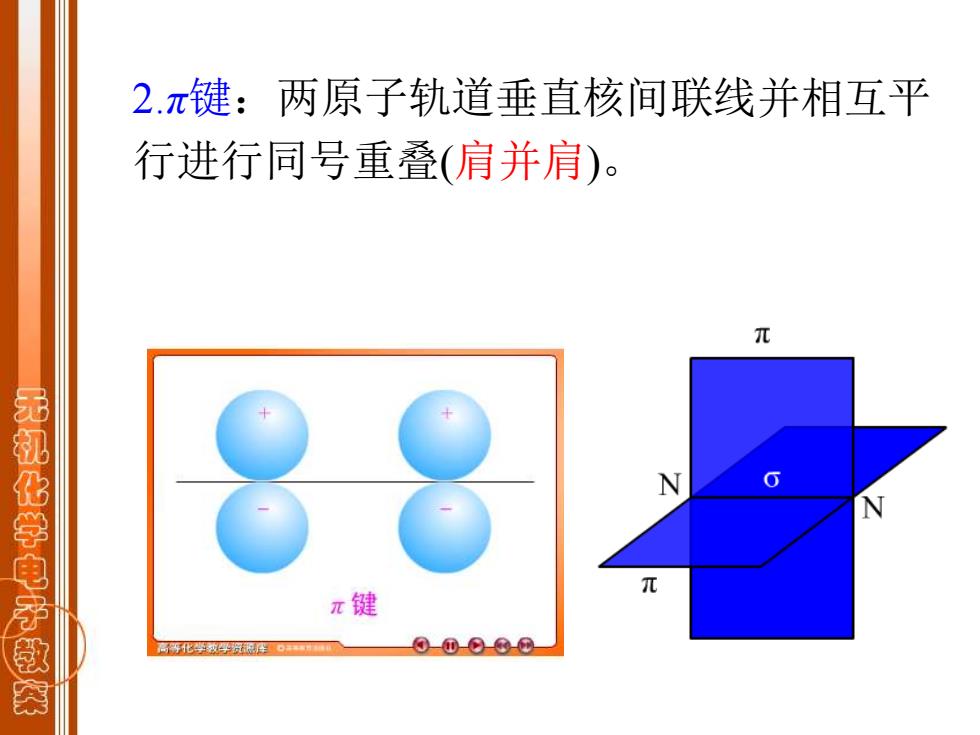
2.π键:两原子轨道垂直核间联线并相互平 行进行同号重叠(肩并肩)。 元 无机化学电子救 N G π键 0-0-⊙⊙-0
2.π键:两原子轨道垂直核间联线并相互平 行进行同号重叠(肩并肩)
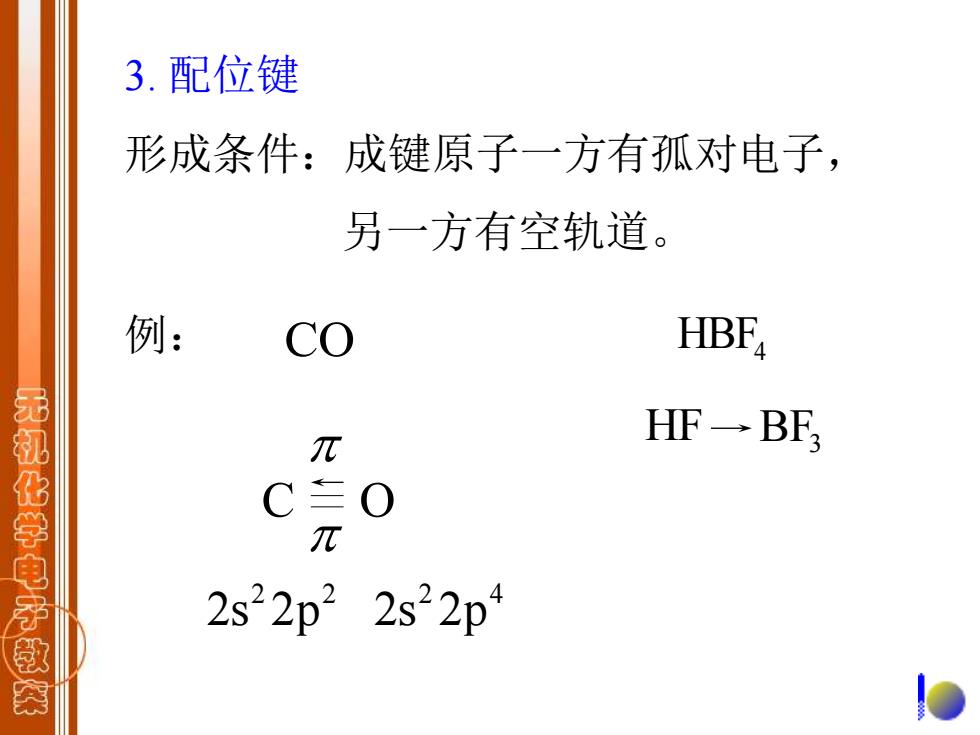
3.配位键 形成条件:成键原子一方有孤对电子, 另一方有空轨道。 例: co HBF HF→BF 无机化学电子教茶 C π 2s22p22s22p lo
3. 配位键 形成条件:成键原子一方有孤对电子, 另一方有空轨道。 CO HBF4 2 2 2s 2p 2 4 2s 2p HF BF3 C O 例: