
第7章 共价健与分子结构 §7.1价键理论 ☒ §7.2杂化轨道理论 园 §7.3价层电子对互斥理论 §7.4分子轨道理论 §7.5分子间力和氢键 §7.6晶体结构与性质
第7章 共价健与分子结构 §7.1价键理论 §7.3价层电子对互斥理论 §7.4分子轨道理论 §7.5分子间力和氢键 §7.2 杂化轨道理论 §7.6晶体结构与性质

除稀有气体可以单原子稳定 存在。其他物质均以分子或晶体 形式存在。由原子按一定方式组 合,原子或离子间以作用力化学 键组合,形成内部结构一一一决定分 子的性质及分子间的作用力一一一物 质的性质
除稀有气体可以单原子稳定 存在,其他物质均以分子或晶体 形式存在,由原子按一定方式组 合,原子或离子间以作用力化学 键组合,形成内部结构-决定分 子的性质及分子间的作用力-物 质的性质

第七章共价健分子结构 7.1价键理论 1916年路易斯提出经典的共价键理论。 认为:原子结合成分子时,是由成键原子双方 各自提供外层单电子组成共用电子对吸引两个 原子核,共用电子对形成后,使每个原子的电 子组态都达到稀有气体的8电子稳定结构即八 隅律,把这种由“共用电子对”维系的化学作 用力称为共价键
第七章 共价键分子结构 1916年路易斯提出经典的共价键理论。 认为:原子结合成分子时,是由成键原子双方 各自提供外层单电子组成共用电子对吸引两个 原子核,共用电子对形成后,使每个原子的电 子组态都达到稀有气体的8电子稳定结构即八 隅律,把这种由“共用电子对”维系的化学作 用力称为共价键。 7.1 价键理论
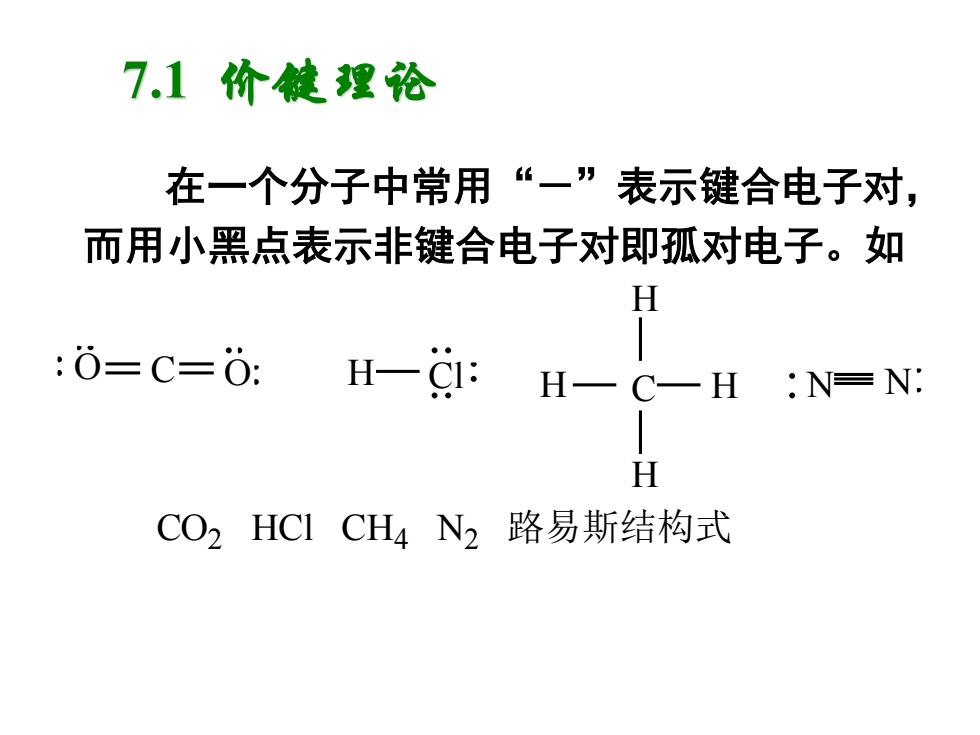
7.1价健理论 在一个分子中常用“一”表示键合电子对, 而用小黑点表示非键合电子对即孤对电子。如 H :0=C=0: / H-C1: H一C一H:N=N: H CO2HC1CH4N2路易斯结构式
在一个分子中常用“-”表示键合电子对, 而用小黑点表示非键合电子对即孤对电子。如 O C O H Cl C H H H H N N CO2 HCl CH4 N2 路易斯结构式 7.1 价键理论
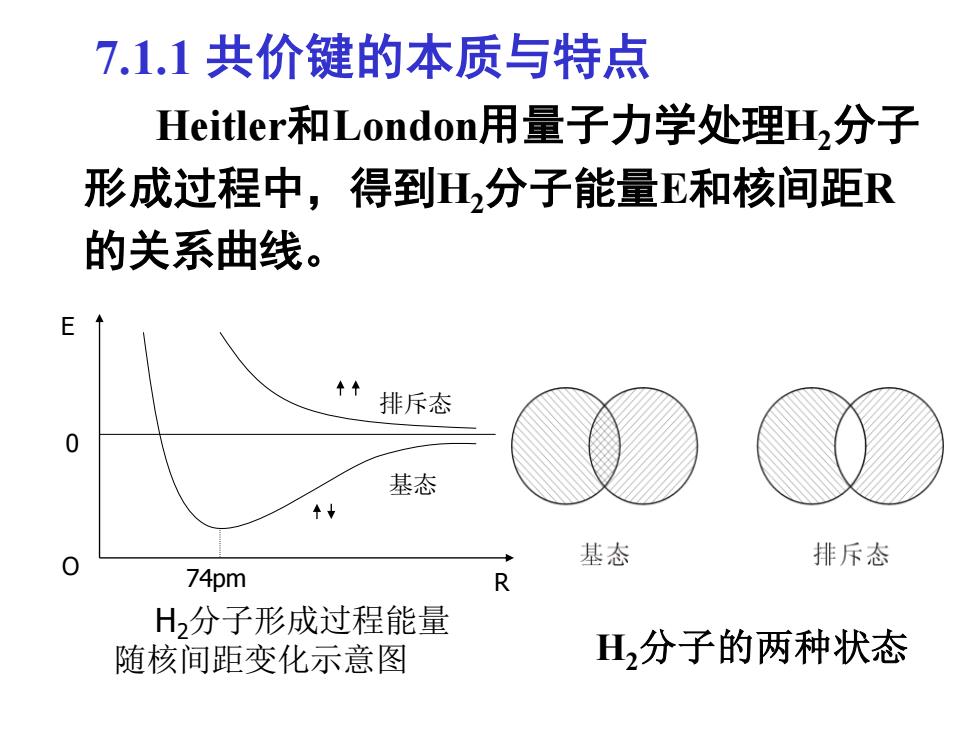
7.1.1共价键的本质与特点 Heitler和London)用量子力学处理H,分子 形成过程中,得到H2分子能量E和核间距R 的关系曲线。 排斥态 基态 基态 排斥态 74pm R H2分子形成过程能量 随核间距变化示意图 H,分子的两种状态
7.1.1 共价键的本质与特点 Heitler和London用量子力学处理H2分子 形成过程中,得到H2分子能量E和核间距R 的关系曲线。 H2分子的两种状态 排斥态 基态 0 O R E 74pm H2分子形成过程能量 随核间距变化示意图