
电化学原理和应用一应用化学专业 绪论 本章主要内容: 一、电化学的研究对象和主要内容 二、电化学的形成与发展简史 三、电化学的应用领域及其进展 四、教学内容与教学安排 上一内容 ·下一内容 ◇回主目录 5返▣
上一内容 下一内容 回主目录 返回 电化学原理和应用——应用化学专业 本章主要内容: 一、电化学的研究对象和主要内容 二、电化学的形成与发展简史 三、电化学的应用领域及其进展 四、教学内容与教学安排

电化学的定义 电化学是研究电能和化学能之间的相互转化及转化过程中 有关规律的科学。(傅献彩,2005;贾梦秋,2004) 。电化学是研究电的作用和化学作用相互关系的化学分支。 (巴德,2005) ,电化学是研究电子导电相和离子导电相之间的界面上所发 生的各种界面效应,同时伴有电现象发生的化学反应的科 学。(李荻,2008;谢德明,2009) 上一内容 下一内容 ◇回主目录 5返回
上一内容 下一内容 回主目录 返回 电化学的定义 • 电化学是研究电能和化学能之间的相互转化及转化过程中 有关规律的科学。(傅献彩,2005;贾梦秋,2004) • 电化学是研究电的作用和化学作用相互关系的化学分支。 (巴德,2005) • 电化学是研究电子导电相和离子导电相之间的界面上所发 生的各种界面效应,同时伴有电现象发生的化学反应的科 学。(李荻,2008;谢德明,2009)
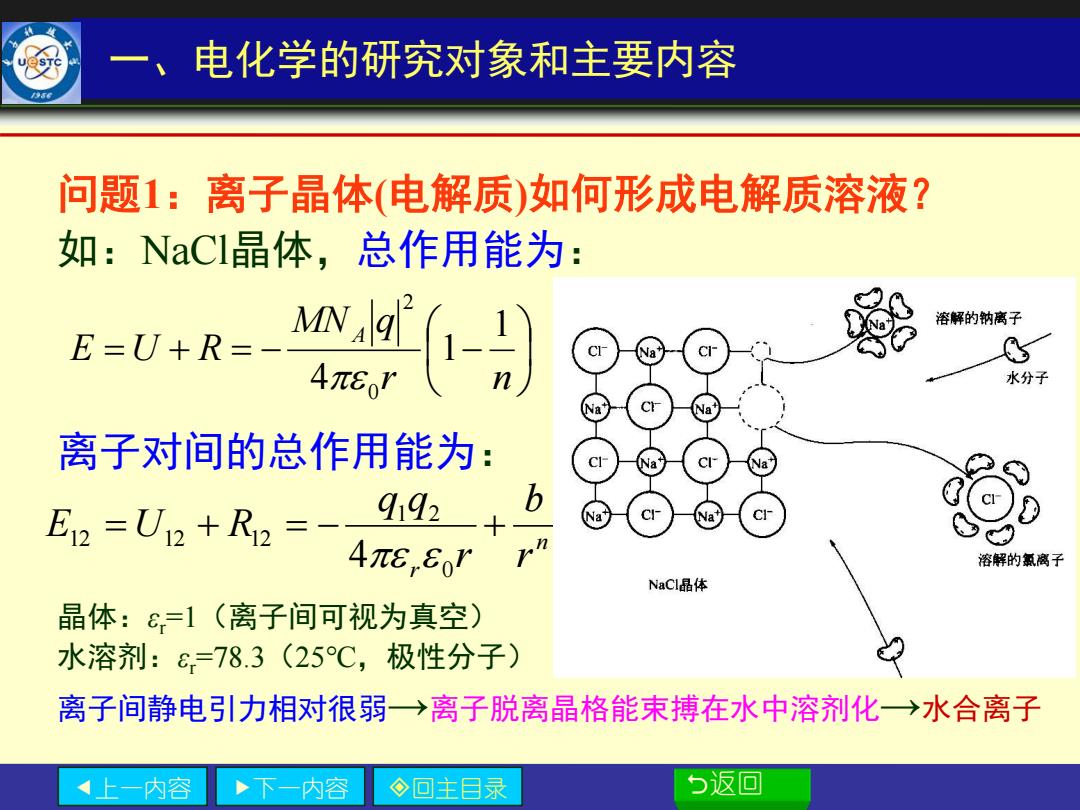
一、电化学的研究对象和主要内容 问题1:离子晶体(电解质)如何形成电解质溶液? 如:NaCl晶体,总作用能为: 溶解的钠离子 E=U+R=-- 水分子 离子对间的总作用能为: b E2=U2+R2=- 9492」 4π8,Eo' 溶解的氯离子 NaCl晶体 晶体:=1(离子间可视为真空) 水溶剂:=78.3(25℃,极性分子) 离子间静电引力相对很弱→离子脱离晶格能束搏在水中溶剂化→水合离子 内容 下一内容 ◇回主目录 返回
上一内容 下一内容 回主目录 返回 问题1:离子晶体(电解质)如何形成电解质溶液? 如:NaCl晶体,总作用能为: 离子对间的总作用能为: 晶体:εr=1(离子间可视为真空) 水溶剂:εr=78.3(25℃,极性分子) 离子间静电引力相对很弱→离子脱离晶格能束搏在水中溶剂化→水合离子 一、电化学的研究对象和主要内容 = + = − − r n MN q E U R A 1 1 4 0 2 n r r b r q q E =U + R = − + 0 1 2 12 12 12 4
一、电化学的研究对象与主要内容 问题2:电化学的研究对象是什么? 下面分析三种常见的导电回路: 1、电子导电回路 现象:负载—灯丝加热而发光。 实质:部分电能转化为热能。 形成电流的载流子:自由电子。 自由电子(或空穴)的定向运动 电子导体或第一类导体。 第一类导体材质:金属、合金、石墨及某些固态金属化合物 电子导体 电工学和电子学研究的对象。 内容 下一内容 ◇回主目录 5返回
上一内容 下一内容 回主目录 返回 一、电化学的研究对象与主要内容 问题2:电化学的研究对象是什么? 下面分析三种常见的导电回路: 1、电子导电回路 现象:负载——灯丝加热而发光。 实质:部分电能转化为热能。 形成电流的载流子:自由电子。 自由电子(或空穴)的定向运动——电子导体或第一类导体。 第一类导体材质:金属、合金、石墨及某些固态金属化合物 电子导体——电工学和电子学研究的对象
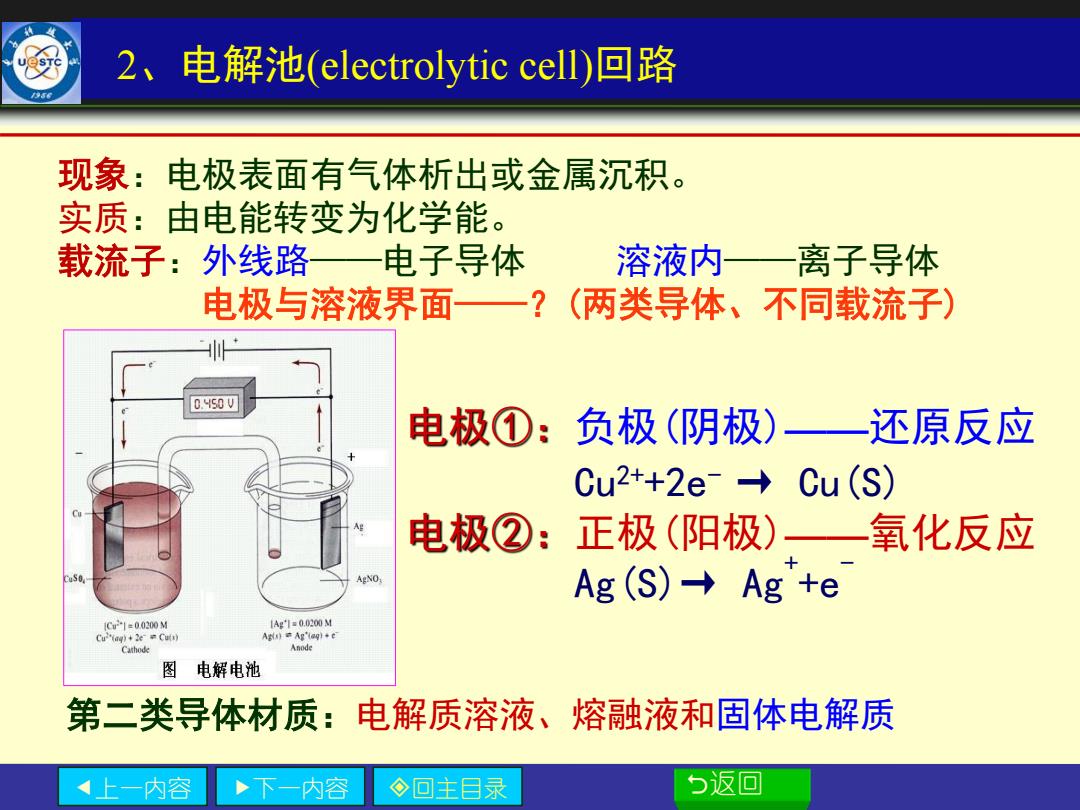
2、电解池(electrolytic cell)▣路 现象:电极表面有气体析出或金属沉积。 实质:由电能转变为化学能。 载流子:外线路— 电子导体 溶液内—离子导体 电极与溶液界面一?(两类导体、不同载流子) D.4S0 V 电极①:负极(阴极)—还原反应 Cu2++2e→ Cu(S) 电极②: 正极(阳极)— 氧化反应 AgNO Ag(S)→Ag+e 1Cr1=0.0200M 1Ag'1=0.020M Cu'(ag)+2e Cut) A料)章Ag'q}+e Cathode Anode 图电解电池 第二类导体材质:电解质溶液、熔融液和固体电解质 上 内容 下一内容 ◇回主目录 5返回
上一内容 下一内容 回主目录 返回 2、电解池(electrolytic cell)回路 现象:电极表面有气体析出或金属沉积。 实质:由电能转变为化学能。 载流子:外线路——电子导体 溶液内——离子导体 电极与溶液界面——?(两类导体、不同载流子) 电极①:负极(阴极)——还原反应 Cu2++2e- → Cu(S) 电极②:正极(阳极)——氧化反应 Ag(S)→ Ag+ +e- 第二类导体材质:电解质溶液、熔融液和固体电解质