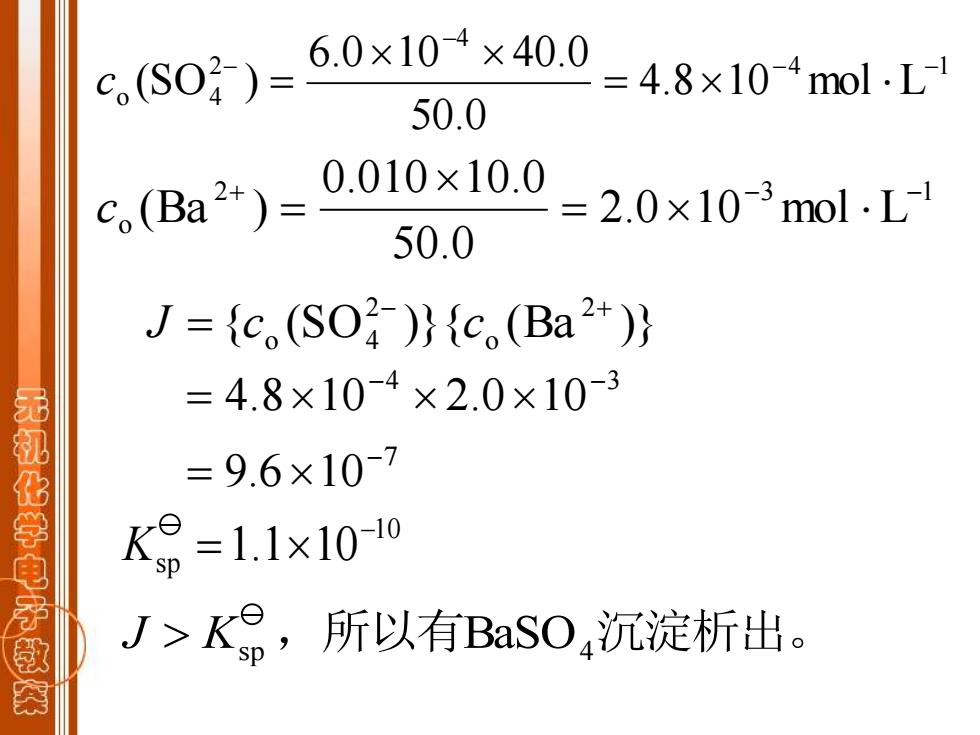
co(SO2)= 6.0×104×40. 2=4.8x104molL 50.0 c(Ba2+)= 0.010×10.0=2.0×103mol.L 50.0 J={c(SO)}{c.(Ba2+)} =4.8×10-4×2.0×10-3 无机化学电子款 =9.6×10-7 K9=1.1x1010 J>K,所以有BaSO,沉淀析出
4 1 4 2 o 4 4.8 10 mol L 50.0 6.0 10 40.0 (SO ) - - - - = c = 7 9.6 10- = 4 3 4.8 10 2.0 10 - - = { (SO )}{ (Ba )} 2 o 2 o 4 - + J = c c 2 3 1 o 2.0 10 mol L 50.0 0.010 10.0 (Ba ) + - - = c = 10 sp 1.1 10- K = J > Ksp ,所以有BaSO4 沉淀析出

BaSO(s)-Ba2*(aq)+SO (aq) 反应前浓度mol.L1) 2.0×103 4.8×10-4 反应后浓度mol.L)2.0x103-4.8x104 0 平衡浓度(mol.L1) 1.52×10-3+x X (1.52×103+x)x=1.1×1010 x很小,1.52×103+x≈1.52×103 无机化学电子教 x=7.3×108 c(S0})=7.3×10-8mol.L (BaS04)=(4.8×10-4-x)×50.0×233 ≈4.8x10×50.0×233=5.6g0
3 2.0 10- 4 4.8 10- /(mol L ) -1 反应前浓度 3 10 (1.52 10 ) 1.1 10 - - + x x = 3 3 1.52 10 1.52 10 - - x很小, + x 3 4 2.0 10 4.8 10 - - /(mol L ) - 0 -1 反应后浓度 + x -3 /(mol L ) 1.52 10 x -1 平衡浓度 BaSO (s) Ba (aq) SO (aq) 2 4 2 4 + - + 4.8 10 50.0 233 5.6g 4 = - (BaSO ) (4.8 10 ) 50.0 233 4 4 = - - m x 2 8 1 (SO4 ) 7.3 10 mol L - - - c = 8 7.3 10- x =