
R光谱 羧酸中的C=0: 单体 二缔合体 RCOOH 1770-1750cm-1 ~1710cm-1 CH,=CHCOOH ~1720cm-1 ~1690cm-1 ArCOOH 1700-1690cm 羧酸中的OH: ~3550cm1 3000~2500cm 羧酸中的C-O ~1250cm-1
羧酸中的C=O: 单体 二缔合体 RCOOH 1770~1750cm-1 ~1710cm-1 CH2=CHCOOH ~ 1720 cm-1 ~1690cm-1 ArCOOH 1700-1690cm- 羧酸中的OH: ~ 3550 cm-1 3000 ~2500cm- 羧酸中的C-O ~ 1250 cm-1 IR光谱
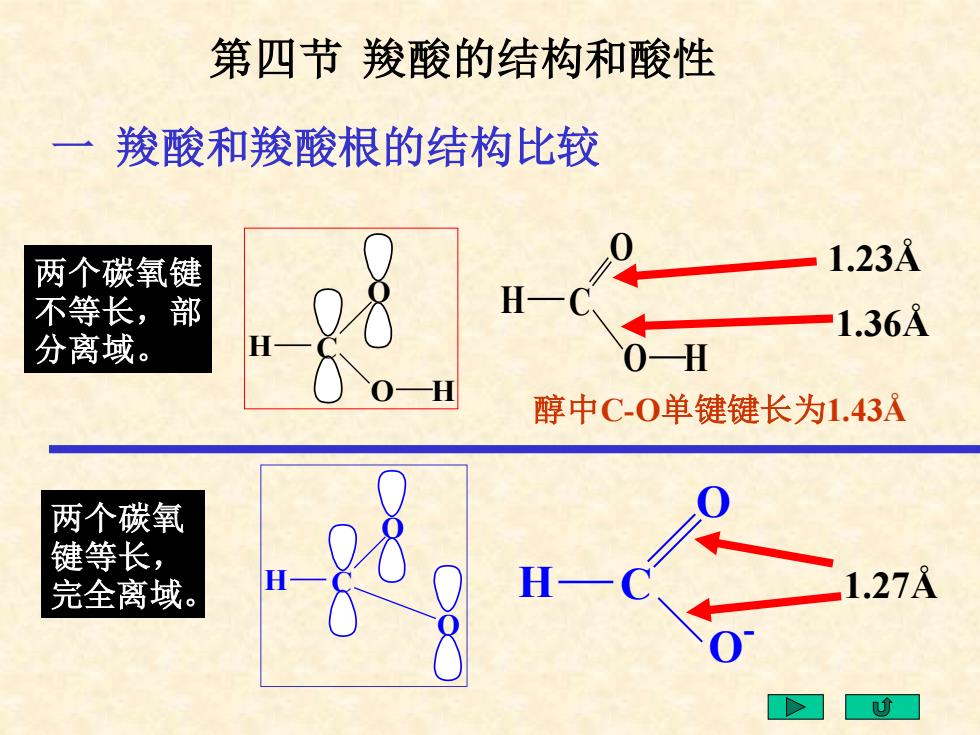
第四节羧酸的结构和酸性 羧酸和羧酸根的结构比较 两个碳氧键 1.23A 不等长,部 08 H- 1.36A 分离域。 H 0-H 醇中C-0单键键长为1.43A 两个碳氧 键等长, 完全离域。 1.27A
两个碳氧键 不等长,部 分离域。 两个碳氧 键等长, 完全离域。 第四节 羧酸的结构和酸性 H C O O H C O O - H C O O H H C O O H 1.36Å 1.23Å 1.27Å 醇中C-O单键键长为1.43Å 一 羧酸和羧酸根的结构比较

二讨论 1羧酸根比较稳定,所以羧酸的氢能解离 而表现出酸性。 2多数的羧酸是弱酸,pKa约为4-5 (大部分的羧酸是以未解离的分子形式存在)
2 多数的羧酸是弱酸,pKa约为4-5 (大部分的羧酸是以未解离的分子形式存在) 二 讨论 1 羧酸根比较稳定,所以羧酸的氢能解离 而表现出酸性

3取代基对羧酸酸性的影响 (1)电子效应的影响: 吸电子取代基使酸性增大,给电子取代基使酸性减少, HCOOH C.Hs-COOH CH:COOH pka 3.37 4.20 4.73 (2)空间效应: 利于H离解的空间结构 0H 酸性强,不利于H离解的空 间结构酸性弱. (3)分子内的氢键也能 使羧酸的酸性增强
(1)电子效应的影响: 吸电子取代基使酸性增大,给电子取代基使酸性减少. HCOOH C6H5 -COOH CH3COOH pka 3.37 4.20 4.73 3 取代基对羧酸酸性的影响 O H O O H (3)分子内的氢键也能 使羧酸的酸性增强。 (2)空间效应: 利于H+离解的空间结构 酸性强,不利于H+离解的空 间结构酸性弱

4芳香羧酸的情况分析 取代基具有吸电子共轭效应时,酸性强弱顺序为: 邻>对>间 取代基具有给电子共轭效应时,酸性强弱顺序为: 邻>间>对 具体分析: 邻位(诱导、共轭、场、氢键效应、空间效应 均要考虑。) 对位(诱导很小、共轭为主。) 间位(诱导为主、共轭很小。)
4 芳香羧酸的情况分析 取代基具有吸电子共轭效应时,酸性强弱顺序为: 邻 > 对 > 间 取代基具有给电子共轭效应时,酸性强弱顺序为: 邻 > 间 > 对 具体分析: 邻 位(诱导、共轭、场、氢键效应、空间效应 均要考虑。) 对 位(诱导很小、共轭为主。) 间 位(诱导为主、共轭很小。)