
4.2.2预测反应方向 反应商: 对于一般的化学反应: aA(g)+bB(aq)+cC(s)=xX(g)+yY(aq)+zZ(1) 任意状态下: 无机化学电子教茶 J延[p,(/pP]'[c,Y)/e]" [P,(A)/P][c,B)/c8]b
对于一般的化学反应: 4.2.2 预测反应方向 任意状态下: aA (g)+ bB(aq)+cC(s) xX(g)+yY(aq)+zZ(l) b i a i y i x i p p c c p p c c J [ (A)/ ] [ (B)/ ] [ (X) / ] [ (Y)/ ] = def 反应商:
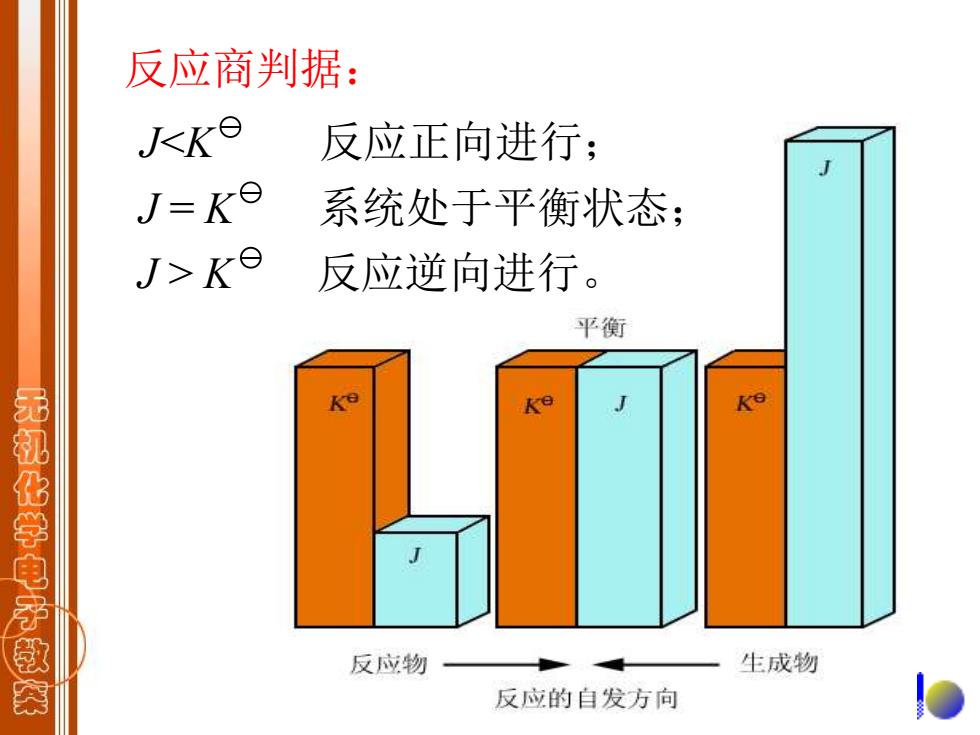
反应商判据: KKe 反应正向进行; J=ke 系统处于平衡状态: J>Ke 反应逆向进行。 平衡 Ke 无机化学电子救 反应物 生成物 反应的自发方向
反应商判据: J<K 反应正向进行; J = K 系统处于平衡状态; J > K 反应逆向进行

4.2.3计算平衡组成 例题:已知反应CO(g+C12(g)=COCl2(g) 在定温定容条件下进行,373K时K9=1.5×108。 反应开始时c(C0)=0.0350molL1, co(Cl2)=0.0270molL1,co(C0C2)=0。计算 373K反应达到平衡时各物种的分压和CO的 平衡转化率。 化学电子 解:pV=nRT因为T、V不变,pxnB P(B)=c(B)RT Po(C0)=(0.0350×8.314×373)kPa=108.5kPa 闲 po(Cl2)=(0.0270×8.314×373)kPa=83.7kPa
p ( B) = c ( B) RT 解:pV = nRT 因为T 、V 不变,p∝nB p0 (CO)=(0.0350×8.314×373)kPa=108.5 kPa p0 (Cl2 )=(0.0270×8.314×373)kPa=83.7 kPa 4.2.3 计算平衡组成 反应开始时c0 (CO)=0.0350mol·L-1 , c0 (Cl2 )=0.0270mol·L-1 ,c0 (COCl2 )=0。计算 373K反应达到平衡时各物种的分压和CO的 平衡转化率。 例题:已知反应CO(g)+Cl2 (g) COCl2 (g) 在定温定容条件下进行,373K时K =1.5108

解: CO(g+C12(g)=C0C12(g) 开始c/(molL1) 0.0350 0.0270 0 开始pp/kPa 108.5 83.7 0 假设CL,全部转化 108.5-83.7 0 83.7 又设COCI2转化x x X -x 平衡py/kPa 24.8+x X 83.7-x 无机化学电子款 K- p(COCI,)/pe (83.7-x)/100 o网489) 100 =1.5×108
开始cB/(mol·L-1 ) 0.0350 0.0270 0 开始pB/kPa 108.5 83.7 0 假设Cl2全部转化 108.5-83.7 0 83.7 又设COCl 2转化x x x -x 平衡pB/kPa 24.8+x x 83.7-x 解: CO(g)+Cl2 (g) COCl 2 (g) (CO)/ (Cl )/ (COCl )/ 2 2 p p p p p p K = 8 = 1.510 ( ) + − = 100 100 24.8 83.7 /100 x x x

因为K很大,x很小, 假设83.7-x≈83.7, 24.8+x≈24.8。 83.7×100 =1.5×10 x=2.3×106 24.8x 平衡时:p(CO)=24.8kPa,p(Cl2)=2.3×10-6kPa p(COC12)=83.7kPa 无机化学电子教菜 a(Co)=Bo(CO)-Ps(Co) Po(CO) 108.5-24.8 ×100% 108.5 =77.1%
8 6 1.5 10 2.3 10 24.8 83.7 100 − = = x x 平衡时:p(CO)=24.8kPa ,p(Cl2 )=2.3 10-6 kPa p(COCl2 )=83.7kPa 假设 83.7-x ≈ 83.7, 24.8+x ≈24.8 。 因为K 很大,x很小, ( ) ( ) ( ) (CO) CO CO CO 0 0 eq p p − p = = 77.1% 100% 108.5 108.5 24.8 − =