
首先酯丛金属钠获得一个电子还原为自由基负离子,然后从醇中 盛基成为麓,金润过精的参攻靖,于精赣青新阳 夺 目由基, 再从羽得到 消除 RR+m→R86一R-owo阳 0 H RCH2OH 反应实创 CH(CH210CH2OH 75% Na E0,GcGH2h0c01E0HHoGH,CH2w9Hg0H7% 醛酮也可以用本法还原,得到相应的醇: CH3(CHsCHO CHCHOACHCH)CHOH a Bucherer反应 萘酚及具衍生物在亚硫酸或亚硫酸氢盐存在下和氨进行高温反应, 可得萘胺行生物,反应是可逆的。 个OH NAHSO5NloC-6m NaHSO3.OH 除去氨而得 反应机理
反应实例 Bucherer 反应 反应机理
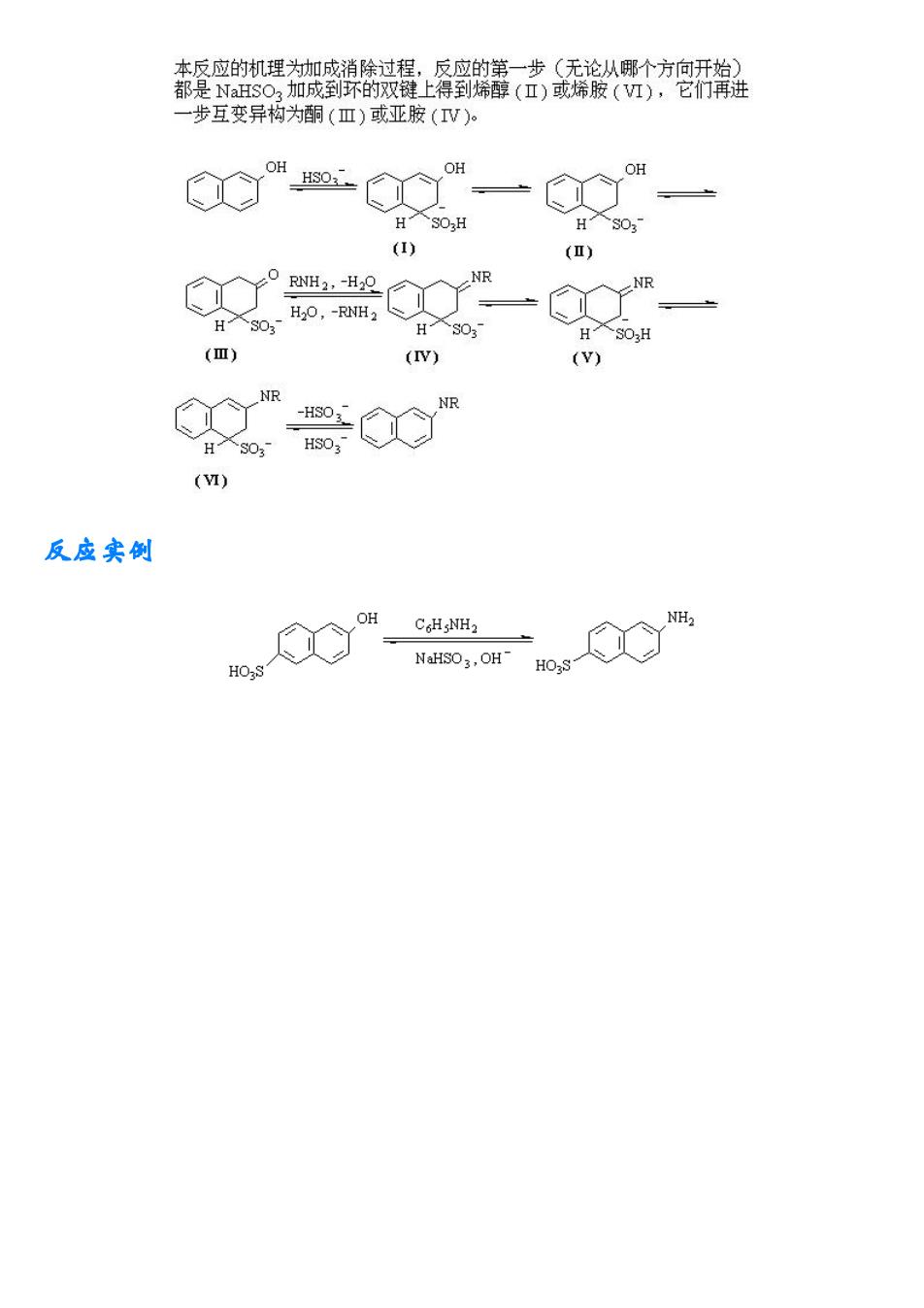
餐机理茄得蜜著,教开棉 -步互变异构为酮(Ⅲ)或亚胺(IV)。 OH HSOH (I) () H入S0H (Ⅲ) (V) ( 器0 (M) 反应实例 to
反应实例

Cannizzaro反应 -CHO NOH、cH,oH+Gco: HCHO NO CH3OH HCO 软无花淡缸原子种不美务生这样跑环反 还原 醛被还原甲醇 如甲和凝 HCHO C HCHOHCCH 具有-活泼氢原子的和甲醇首先发生羟醛缩合反应,得到无-活泼 氢原子的B羟基醛,然后再与甲醛进行交叉Cannizzaro反应,如乙醛和 甲醛反应得到季戊四醇: HCHO 反应机理 这个反应可能是经过下列的步骤: 的氢带着 染 C6H5- 一H OH · 0 -H→c-8-oH+cw,-&-H OH CHCO2+CHCH2OH 当此反应在重水中进行时,所得醇的碳原子上不含重氢,表明这些 -氢原子是由另一分子醛得到的而不是来自反应介质。 反应实创
Cannizzaro 反应 反应机理 反应实例

CHO 8-CHO NOH OH 2) ○6-c0 Chichibabin反应 的:陵贸幸数保。贤 据,则得氨基吡啶,但产率很低。 ◇+,mEp· N人NHNa N人NH2 本法是在杂环上引入氨的简便有效的方法,广泛酒用于务种氢杂背 紫味等以清球空高化剂 反应机理 转移反序贺置銎侧暮子保能是晚望李里 的2-氨基此啶(江),此小量的(反可以作为质子的给子体,最后的 产物是2-氨基吡啶的钠盐,用水分解得到2-氨基吡啶: Ne+NH2 (I) (Ⅱ) Ne'NH2 +HCN 、+H2+ 人NH Na () (0) H20 NH Na' +NaOH
Chichibabin 反应 反应机理
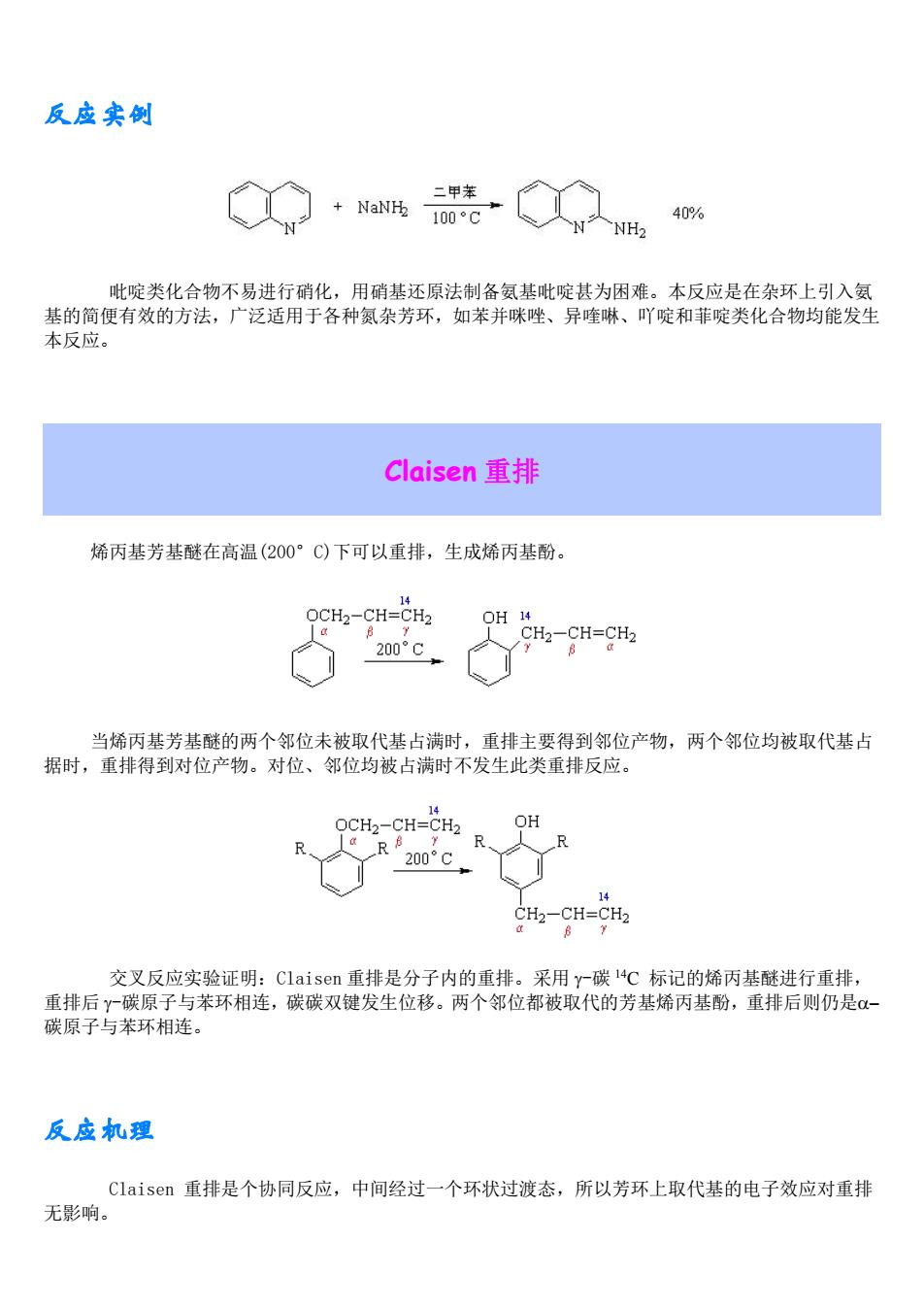
反应实创 吡啶类化合物不易进行硝化,用硝基还原法制备氨基吡啶甚为困难。本反应是在杂环上引入氨 基的简便有效的方法,广泛适用于各种氮杂芳环,如苯并咪唑、异喹啉、吖啶和菲啶类化合物均能发生 本反应 Claisen重排 烯丙基芳基醚在高温(200°C)下可以重排,生成烯丙基酚。 OCH2-CH-CH OH 14 200°c CHa-CH-CHa 当烯丙基芳基醚的两个邻位未被取代基占满时,重排主要得到邻位产物,两个邻位均被取代基占 据时,重排得到对位产物。对位、邻位均被占满时不发生此类重排反应。 OH R、 R 200°c CH2-CH=CH2 交叉反应实验证明:Claisen重排是分子内的重排。采用y一碳14C标记的烯丙基醚进行重排, 重排后y一碳原子与苯环相连,碳碳双键发生位移。两个邻位都被取代的芳基烯丙基酚,重排后则仍是α 碳原子与苯环相连。 反应机理 laisen重排是个协同反应,中间经过一个环状过渡态,所以芳环上取代基的电子效应对重排 无影响
反应实例 吡啶类化合物不易进行硝化,用硝基还原法制备氨基吡啶甚为困难。本反应是在杂环上引入氨 基的简便有效的方法,广泛适用于各种氮杂芳环,如苯并咪唑、异喹啉、吖啶和菲啶类化合物均能发生 本反应。 Claisen 重排 烯丙基芳基醚在高温(200°C)下可以重排,生成烯丙基酚。 当烯丙基芳基醚的两个邻位未被取代基占满时,重排主要得到邻位产物,两个邻位均被取代基占 据时,重排得到对位产物。对位、邻位均被占满时不发生此类重排反应。 交叉反应实验证明:Claisen 重排是分子内的重排。采用 -碳 14C 标记的烯丙基醚进行重排, 重排后 -碳原子与苯环相连,碳碳双键发生位移。两个邻位都被取代的芳基烯丙基酚,重排后则仍是 碳原子与苯环相连。 反应机理 Claisen 重排是个协同反应,中间经过一个环状过渡态,所以芳环上取代基的电子效应对重排 无影响