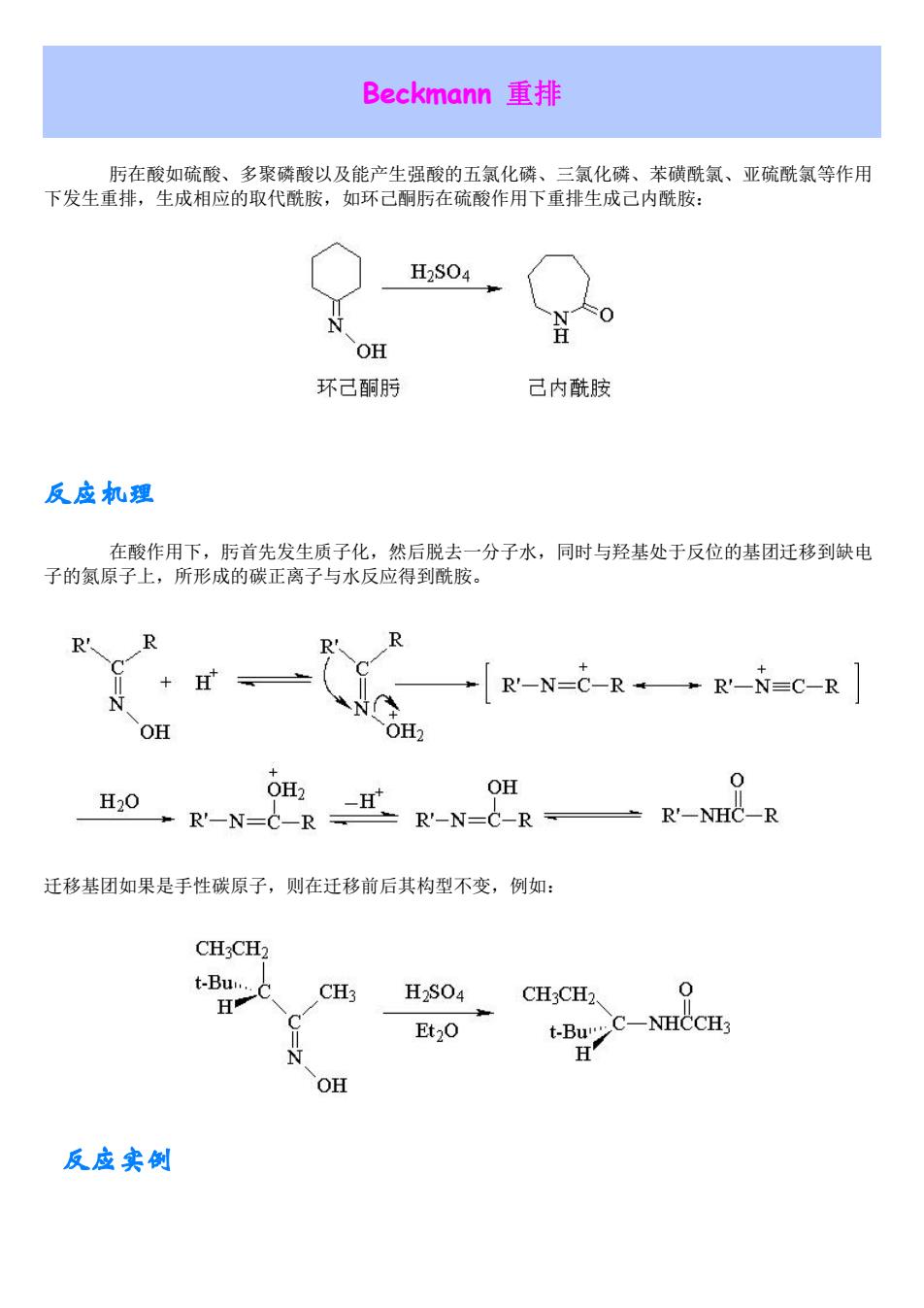
Beckmann重排 肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用 下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺: H2S04 0 OH 环己酮肟 己内酰胺 反应机理 在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁移到缺电 子的氮原子上,所形成的碳正离子与水反应得到酰胺。 R R +H' +[R'-N=C-R→R'-N=C-R OH OH2 OH 0 H20 +R'-N=C-R= 迁移基团如果是手性碳原子,则在迁移前后其构型不变,例如: CH:CH CH3 H2S04 CH3CH2 Et2O BCNHCCH OH 反应实创
Beckmann 重排 肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用 下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺: 反应机理 在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁移到缺电 子的氮原子上,所形成的碳正离子与水反应得到酰胺。 迁移基团如果是手性碳原子,则在迁移前后其构型不变,例如: 反应实例
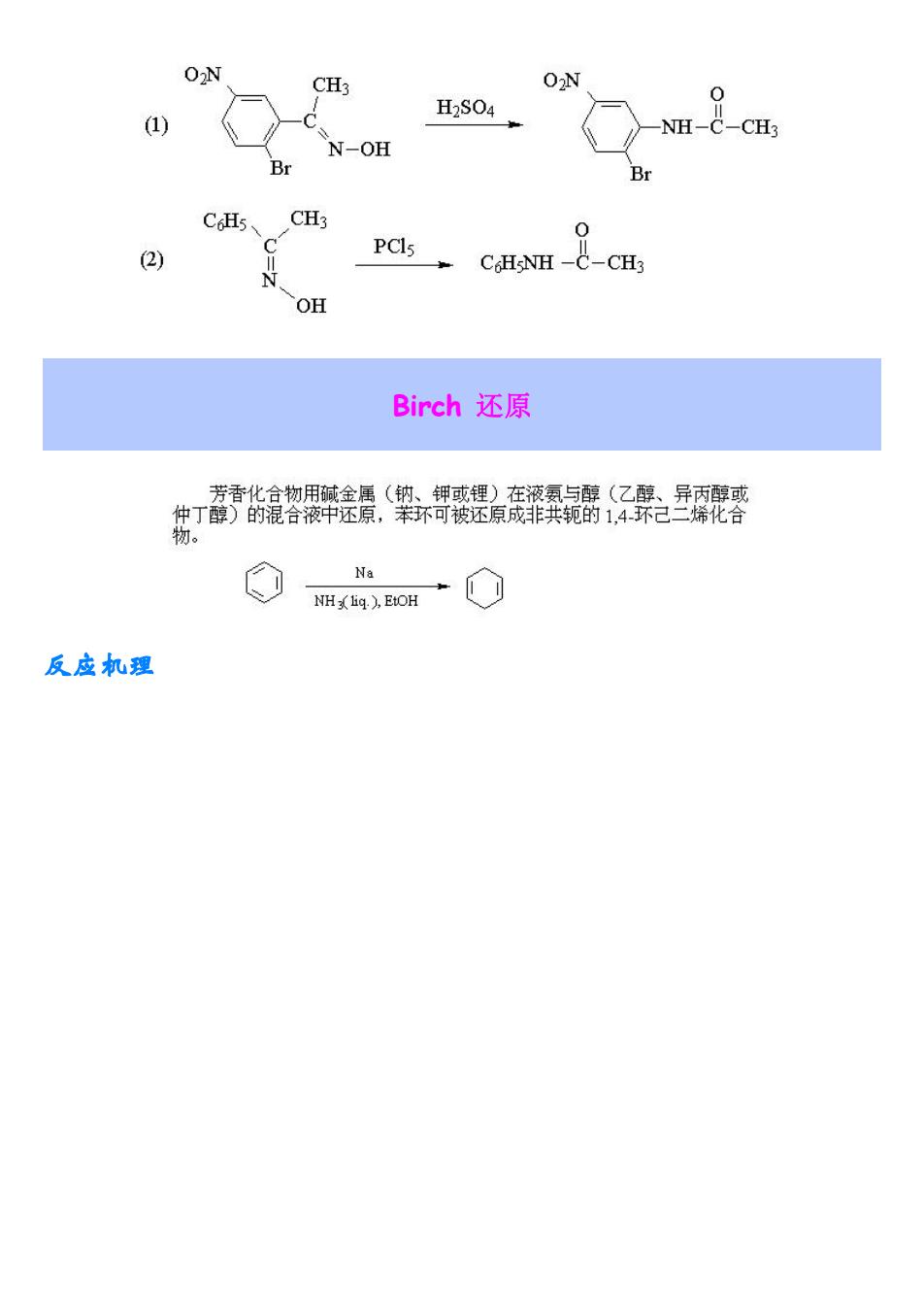
CH ON 1) H2S04 )NH-CHs N-OH CH5、 CH (2) CoHSNH-C-CH3 OH Birch还原 忠器枭聚器 O Na mHx4EoH→○ 反应机理
Birch 还原 反应机理

首先是钠和液氨作用生成溶剂化点子,然后苯环得到一个电子生 从2中最个电子生成冠,( 由子恋成花 Na NH3-Na'+e 00一⊙一0] “良一g一-一 “的 w) 环属影花换离质品来视监的中同陕原子上质子化比在末碳原子 ÷0÷的 反应实创 取代的苯也能发生还原,并且通常得到单一的还原产物。例如: 照4合 Na N,().EOHCH☆ Na
反应实例
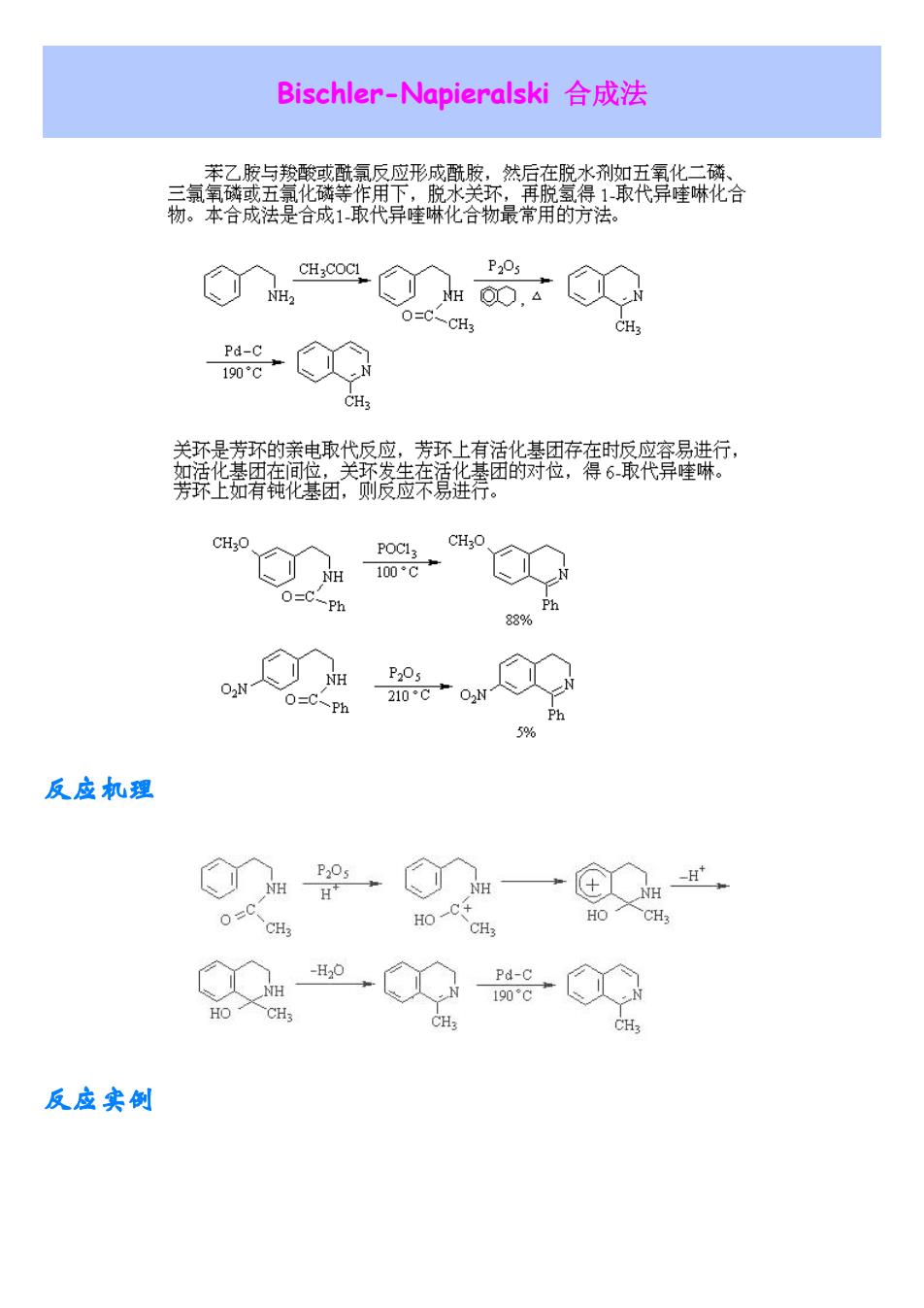
Bischler-Napieralski合成法 物。本合成法是合成1取代异哇琳化合物最常用的方法。 ,4a.粉.。 0= CH3 CH, 芳环上如有钝化基团,则反应不易进寿。 Ph 88% oO 反应机理 反应实创
Bischler-Napieralski 合成法 反应机理 反应实例
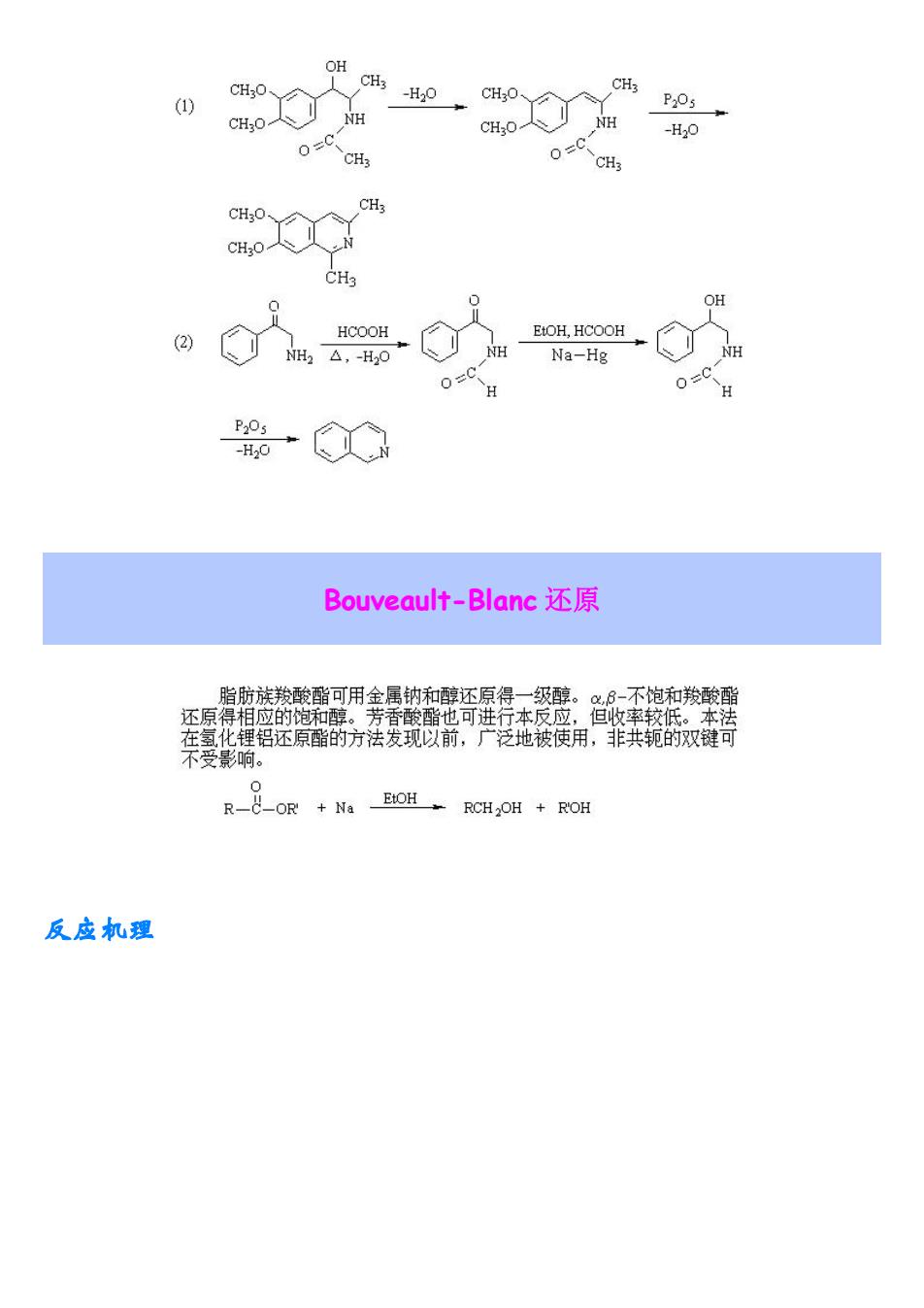
OH 0) HpHo个人CH0 -H0 CH3 OH (2 ◇出,0 Na-Hg 00H Bouveault-Blanc还原 R-OR+Ns RCH:OH+ROH 反应机理
Bouveault-Blanc 还原 反应机理