
第五章 化学平衡 Chapter 5.Chemical equilibrium §5-1化学反应的吉布斯函数变化 §5-2理想气体反应等温方程及标准平衡常数 §5-3理想气体反应平衡常数与平衡组成 §5-4标准摩尔反应吉布斯函数计算 §5-5温度对标准平衡常数的影响 §5-6压力和反应物组成对平衡的影响 §5-7同时平衡反应 §5-8真实气体反应平衡衡
第五章 化学平衡 Chapter 5. Chemical equilibrium §5-1化学反应的吉布斯函数变化 §5-2理想气体反应等温方程及标准平衡常数 §5-3理想气体反应平衡常数与平衡组成 §5-4标准摩尔反应吉布斯函数计算 §5-5温度对标准平衡常数的影响 §5-6压力和反应物组成对平衡的影响 §5-7同时平衡反应 §5-8真实气体反应平衡

§5-0引言 用热力学的方法研究化学反应的方向和限度 1、在反应条件下的反应方向和极限产率; 2、改变反应条件如:压力、温度物料配比等,得到 更大的产率; 3、通过理论计算同实际生产对比,估计提高产率的 幅度
§5--0 引言 用热力学的方法研究化学反应的方向和限度 1、在反应条件下的反应方向和极限产率; 2、改变反应条件如:压力、温度物料配比等,得到 更大的产率; 3、通过理论计算同实际生产对比,估计提高产率的 幅度。 1、在反应条件下的反应方向和极限产率; 2、改变反应条件如:压力、温度物料配比等,得到 更大的产率; 3、通过理论计算同实际生产对比,估计提高产率的 幅度
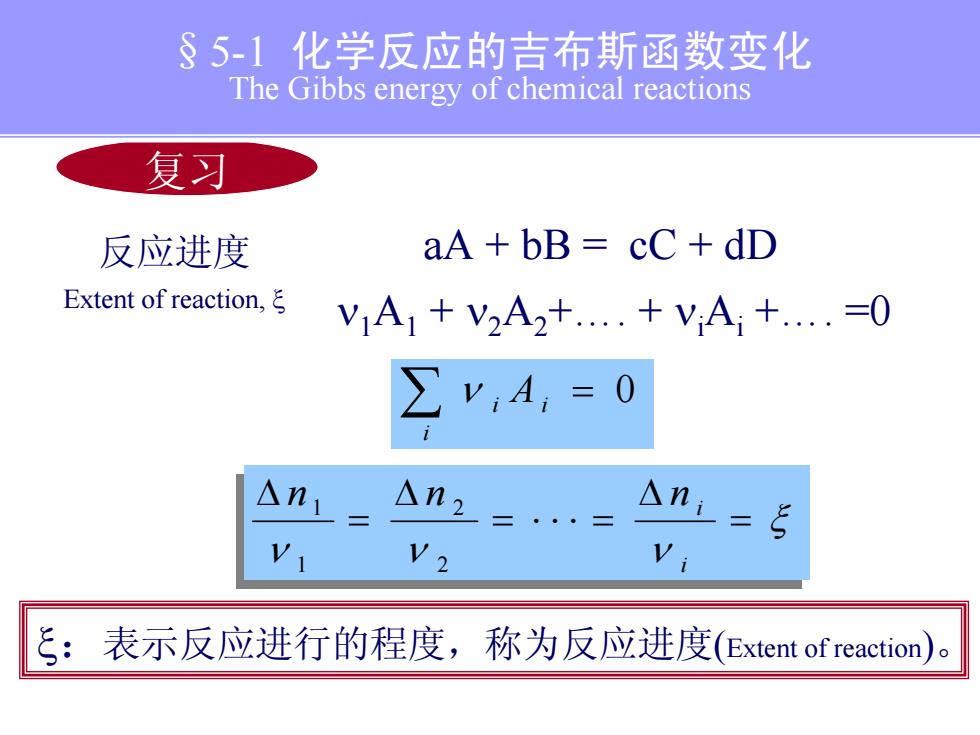
§5-1化学反应的吉布斯函数变化 The Gibbs energy of chemical reactions 复习 反应进度 aA+bB=cC+dD Extent of reaction,ξ V1A1+V2A2+..+VA;+.=0 ∑,A,=0 △n1 △n2 △ni 三:表示反应进行的程度,称为反应进度(Extent of reaction)
§ φ 5-1 化学反应的吉布斯函数变化 The Gibbs energy of chemical reactions 复习 反应进度 Extent of reaction, ξ aA + bB = cC + dD ν1A1 + ν2A2+…. + νiAi +…. =0 ∑ i = 0 i ν i A ξ νν ν = Δ =⋅⋅⋅= Δ = Δ i nn n i 2 2 1 1 ξ:表示反应进行的程度,称为反应进度(Extent of reaction)
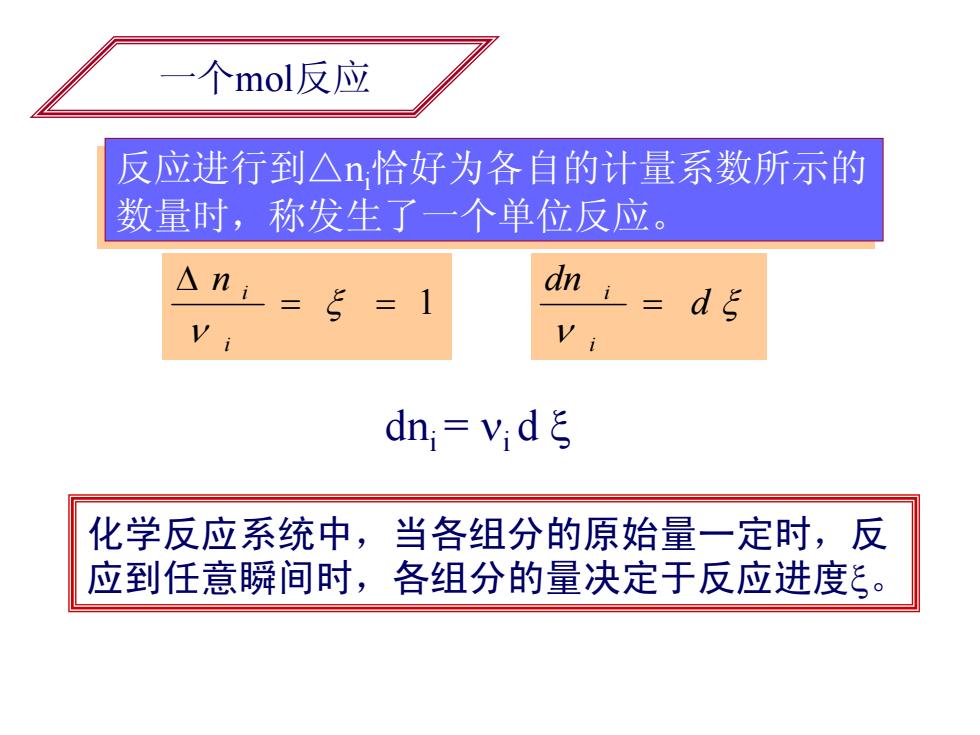
个mol反应 反应进行到△n,恰好为各自的计量系数所示的 数量时,称发生了一个单位反应。 dn i= dn=v;dξ 化学反应系统中,当各组分的原始量一定时,反 应到任意瞬间时,各组分的量决定于反应进度ξ
一个mol反应 φ 反应进行到△ni恰好为各自的计量系数所示的 数量时,称发生了一个单位反应。 反应进行到△ni恰好为各自的计量系数所示的 数量时,称发生了一个单位反应。 == 1 Δ ξ ν i n i ξ ν d dn i i = 化学反应系统中,当各组分的原始量一定时,反 应到任意瞬间时,各组分的量决定于反应进度ξ。 dni = νi d ξ

一、摩尔反应吉布斯函数变 The reaction Gibbs energy of molecular T、P,进行一个微小反应时组成不变 dG=∑Ldnp B dn=v:dξ dG=∑4sdna=∑4avsd5 B aG 定义 5 =∑VBB=A,Gm T.P 摩尔反应吉布斯函数变
一、摩尔反应吉布斯函数变 The reaction Gibbs energy of molecular 一、摩尔反应吉布斯函数变 The reaction Gibbs energy of molecular T 、 P,进行一个微小反应时组成不变 B B B dG = ∑ μ dn dn i = ν i d ξ dG μ dn B dξνμ B B B B = ∑ B = ∑ 定义 B mr B B PT G G = Δ= ⎟ ⎟ ⎠ ⎞ ⎜ ⎜ ⎝ ⎛ ∂ ∂ ∑ μν ξ , -------摩尔反应吉布斯函数变