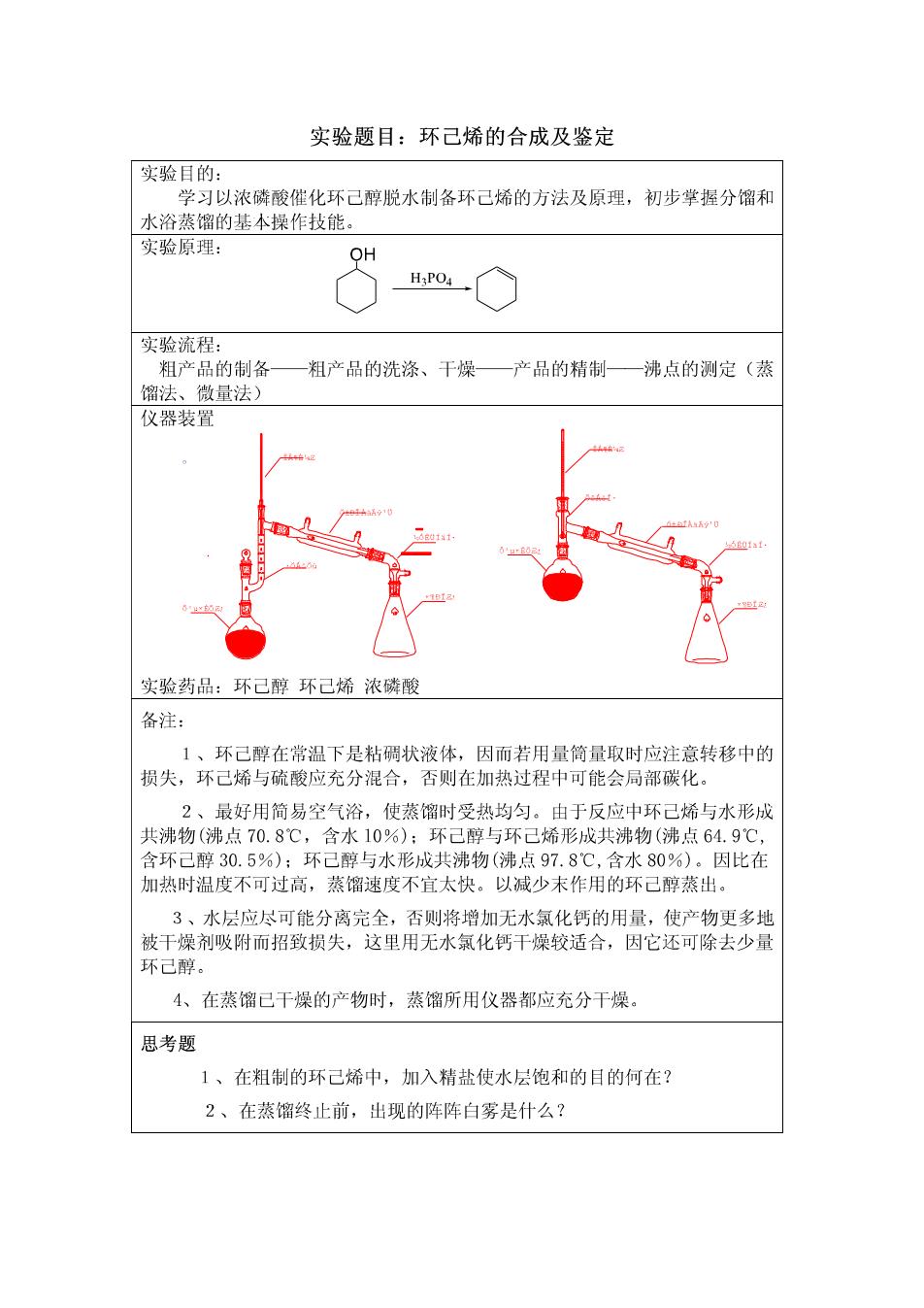
实验题目:环己烯的合成及鉴定 实验目的: 学习以浓磷酸催化环己醇脱水制备环己烯的方法及原理,初步掌握分馏和 水浴蒸馏的基本操作技能。 实验原理: OH 实验流程: 粗产品的制备- 粗产品的洗涤、干燥—产品的精制一沸点的测定(蒸 馏法、微量法) 仪器装置 实验药品:环己醇环己烯浓磷酸 备注: 1、环己醇在常温下是粘碉状液体,因而若用量筒量取时应注意转移中的 损失,环己烯与硫酸应充分混合,否则在加热过程中可能会局部碳化。 2、最好用简易空气浴,使蒸馏时受热均匀。由于反应中环己烯与水形成 共沸物(沸点70.8℃,含水10%):环己醇与环己烯形成共沸物(沸点64.9℃, 含环己醇30.5%):环己醇与水形成共沸物(沸点97.8℃,含水80%)。因比有 加热时温度不可过高,蒸馏速度不宜太快。以减少末作用的环己醇蒸出。 3、水层应尽可能分离完全,否则将增加无水氯化钙的用量,使产物更多地 被干燥剂吸附而招致损失,这里用无水氯化钙干燥较适合,因它还可除去少量 环己醇。 4、在蒸馏已干燥的产物时,蒸馏所用仪器都应充分干燥。 思考题 1、在粗制的环己烯中,加入精盐使水层饱和的目的何在? 2、在蒸馏终止前,出现的阵阵白雾是什么?
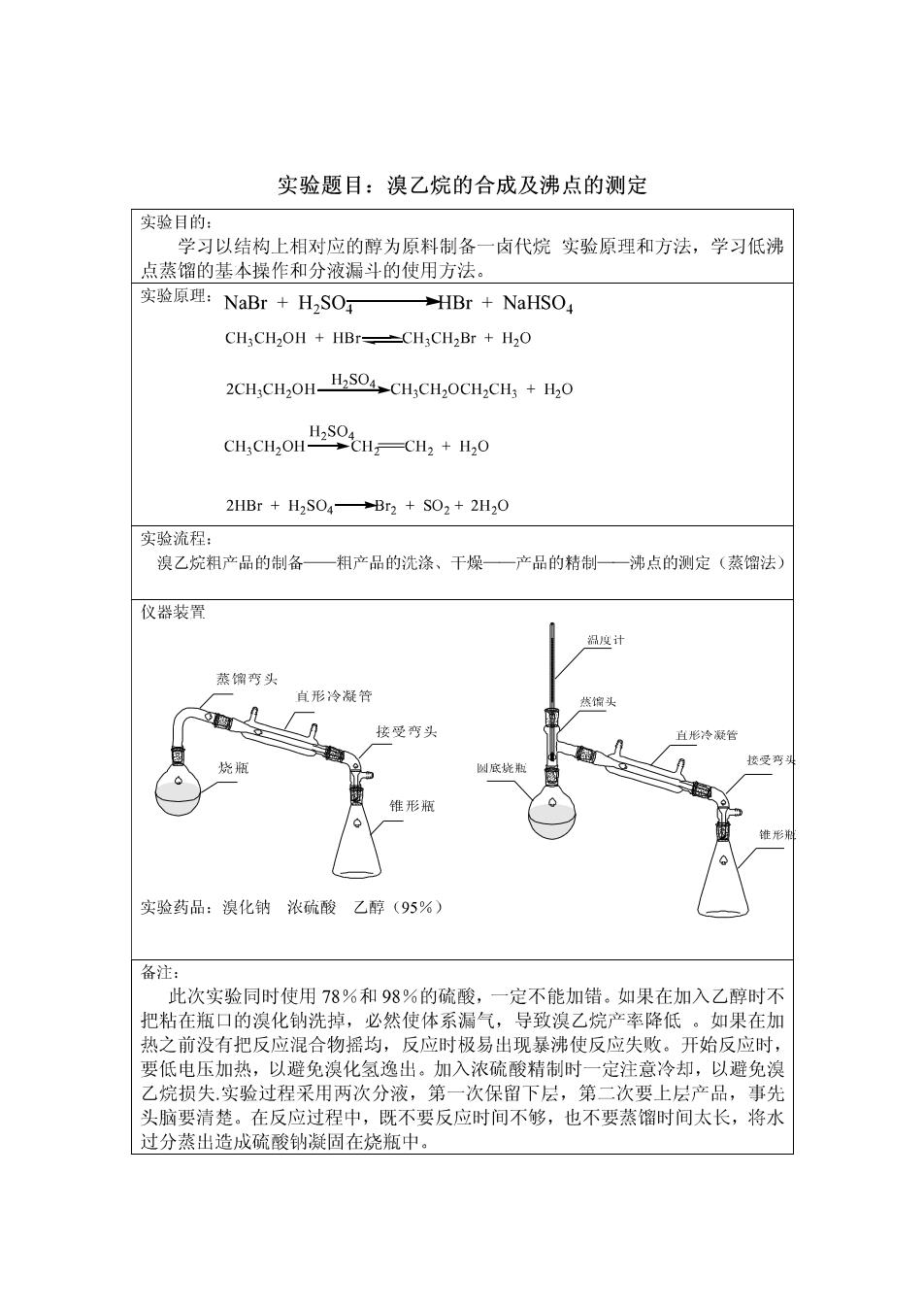
实验题目:溴乙烷的合成及沸点的测定 实验目的: 学习以结构上相对应的醇为原料制备一肉代烷实验原理和方法,学习低沸 点蒸馏的基本操作和分液漏斗的使用方法。 实验原理:NaBr+HzSO HBr NaHSO CH;CH2OH HBr=CH;CH2Br H2O 2CHCHO-S4CHCHOCHCHHO CHCHOH SCHCH+0 2HBr H2SO-Br2+SO2+2H2O 实验流程 溴乙烷粗产品的制备—相产品的洗涤、干埃一产品的精制—沸点的测定(蒸馏法 仪器装骨 度 蒸馏巧头 真形冷凝管 头 接受列头 直彩冷凝管 烧厢 形招 实验药品:溴化钠浓硫酸乙醇(95%) 备注: 此次实验同时使用78%和98%的硫酸,一定不能加错。如果在加入乙醇时不 把粘在瓶口的溴化钠洗掉,必然使体系漏气,导致溴乙烷产率降低。如果在加 热之前没有把反应混合物摇均,反应时极易出现暴沸使反应失败。开始反应时, 要低电压举以免液化氧冷出:加入浓硫酸精时一定注意冷却,以避免浪 一次保留下层,第二次要上层产品 事先 头脑要清楚。在反应过程中,既不要反应时间不够,也不要蒸馏时间太长,将水 过分蒸出造成硫酸钠凝固在烧瓶中

实验题目:1-溴丁烷的制备 实验目的: 1,学习以溴化钠、浓儿S0,和正丁醇制备1-溴丁烷的原理和方法。 2.学习带有吸收有害气体装置的回流等基本操作。 实验原理: NaBr+H2SO4 HBr+NaHSO4 n-C4HgOH+HBr=n--CaHgBr+H2O CH.CH.CH.CH.OHMSOCHCHCH-CHCHCH-CHCH+HO 2CH CH-CH CH-OHSCH.CH2CH.+H2O 实验流程 水、浓硫酸、 回流 蒸馏 严残液 正丁醇、溴化钠 20min 个馏山液(粗正溴丁烷) 洗涤 干燥 蒸馏 ①水②浓硫酸③水④饱和碳酸氢钠⑤水无水氯化钙 9-1030正说了旋 实验药品及仪器装置: 电热套、回流冷凝管、圆底烧瓶、蒸馏装置、分液漏斗、浓HS0、正丁醇、NaBr、 NaO、CaCl、aHC0、折光仪气体吸收装置的正确使用,萃取、洗涤、测折光 气体吸收装置的正确使用,萃取、洗涤、测折光

(1) 2 实验关键及注意事项 1、掌握气体吸收装置的正确安装和使用 2、浓硫酸要分批加入,混合均匀。 3、反应过程中不时摇动烧瓶,或加入磁力搅拌搅拌反应,促使反应完全。 4、正溴丁烷是否蒸完,可以从下列几方面判断:①蒸出液是否由混浊变为澄清: ②蒸馏瓶中的上层油状大物是否消失:③取一试管收集几滴馏出液:加水摇 动观察无油味出现。如无,表示馏出液中己无有机物、蒸馏完成。 5、洗后产物呈红色,可用少量的饱和亚硫酸氢钠水溶液洗涤以除去由于浓硫酸 的氧化作用生成的游离溴。 问题讨论: 1、反应后的粗产物中含有哪些杂质?各步洗涤的目的何在? 2、用分液漏斗时,正溴丁烷时而在上层,时而在下层,如不知道产物的密度时, 可用什么简便的方法加以判别? 3、为什么用饱和碳酸氢钠溶液洗涤前先要用水洗一次? 4.,本实验中,浓硫酸起何作用?其用量及浓度对实验有何影响? 反应后的粗产品中含有哪些杂质?它们是如何被除去的?

实验题目:2-甲基-2-氯丙烷的制备 实验目的: 1.学习以浓盐酸、叔丁醇为原料制备2甲基-2氯丙烷的实验原理和过程 2.进一步巩固蒸馏的基本操作和分液漏斗的使用方法 实验原理: CH3 H+HC→HC OH 路·0 实验流程: 1、在50ml圆底烧瓶中,放置4ml叔丁醇和10.5ml浓盐酸,不断搅拌10~ in后, 转入分液漏斗 静置, 待明显分层 去水 2、有机层分别用水、5%碳酸氢钠溶液、水各2.5ml洗涤,再用无水氯化钙 干燥。 3、干燥后的产品转入蒸馏烧瓶中,加入沸石,接受瓶置于冰水浴中。 4、在水浴上蒸馏收集50一51℃馏分。 5、计算产率。 仪器装置实验药品: 底烧瓶分液漏斗、5%NaHCO,溶液、无水氯化钙、烧杯、温度计 电热套、冷凝管、尾接管、三角烧瓶、沸石 备注: 1.在洗涤粗产品时,若碳酸氢钠溶液浓度过高,洗涤时间过长,将对产物有 何影响?为什么? 2.重点是充分震荡、蒸馏精制