
(2) 与水作用 ● 碱金属被水氧化的反应为: 2 M(s) + 2 H2O (l) → 2 M+(aq) + 2 OH-(aq) + H2(g) ● 碱土金属被水氧化的反应为: M(s) + 2 H2O (l)→ M+(aq) + 2 OH-(aq) + H2(g) 远不如相邻碱金属那样剧烈, 镁和铍在水和空气中因生成致密 的氧化物保护膜而显得十分稳定。 Li Na K
(2) 与水作用 ● 碱金属被水氧化的反应为: 2 M(s) + 2 H2O (l) → 2 M+(aq) + 2 OH-(aq) + H2(g) ● 碱土金属被水氧化的反应为: M(s) + 2 H2O (l)→ M+(aq) + 2 OH-(aq) + H2(g) 远不如相邻碱金属那样剧烈, 镁和铍在水和空气中因生成致密 的氧化物保护膜而显得十分稳定。 Li Na K
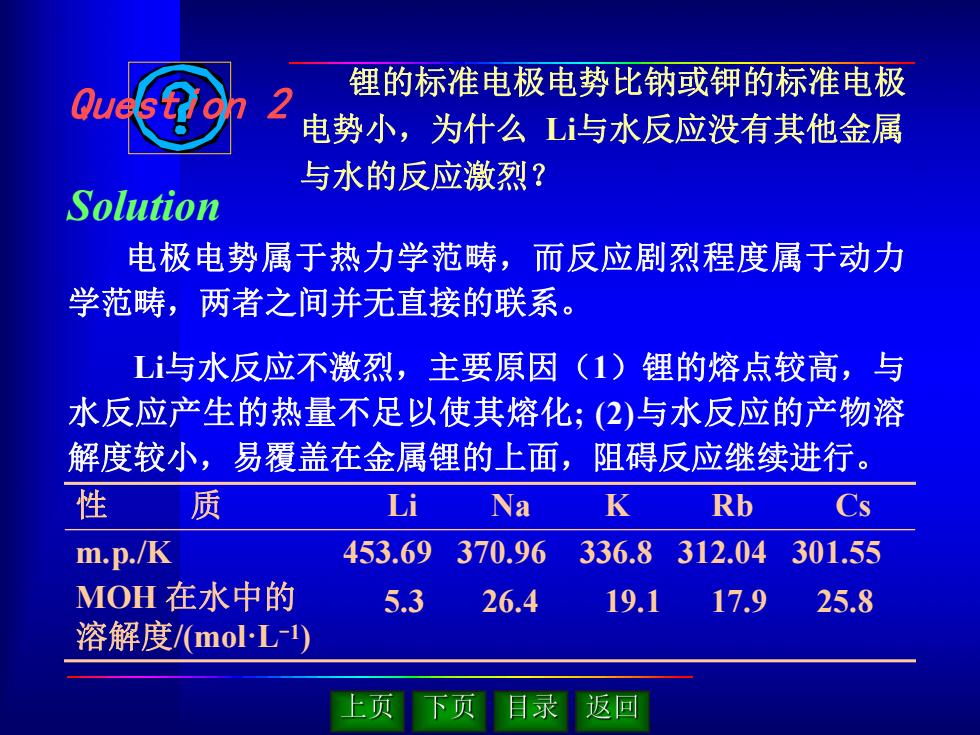
锂的标准电极电势比钠或钾的标准电极 电势小,为什么 Li与水反应没有其他金属 与水的反应激烈? 电极电势属于热力学范畴,而反应剧烈程度属于动力 学范畴,两者之间并无直接的联系。 Li与水反应不激烈,主要原因(1)锂的熔点较高,与 水反应产生的热量不足以使其熔化; (2)与水反应的产物溶 解度较小,易覆盖在金属锂的上面,阻碍反应继续进行。 5.3 26.4 19.1 17.9 25.8 性 质 Li Na K Rb Cs m.p./K 453.69 370.96 336.8 312.04 301.55 MOH 在水中的 溶解度/(mol·L-1) Question 2 Solution
锂的标准电极电势比钠或钾的标准电极 电势小,为什么 Li与水反应没有其他金属 与水的反应激烈? 电极电势属于热力学范畴,而反应剧烈程度属于动力 学范畴,两者之间并无直接的联系。 Li与水反应不激烈,主要原因(1)锂的熔点较高,与 水反应产生的热量不足以使其熔化; (2)与水反应的产物溶 解度较小,易覆盖在金属锂的上面,阻碍反应继续进行。 5.3 26.4 19.1 17.9 25.8 性 质 Li Na K Rb Cs m.p./K 453.69 370.96 336.8 312.04 301.55 MOH 在水中的 溶解度/(mol·L-1) Question 2 Solution
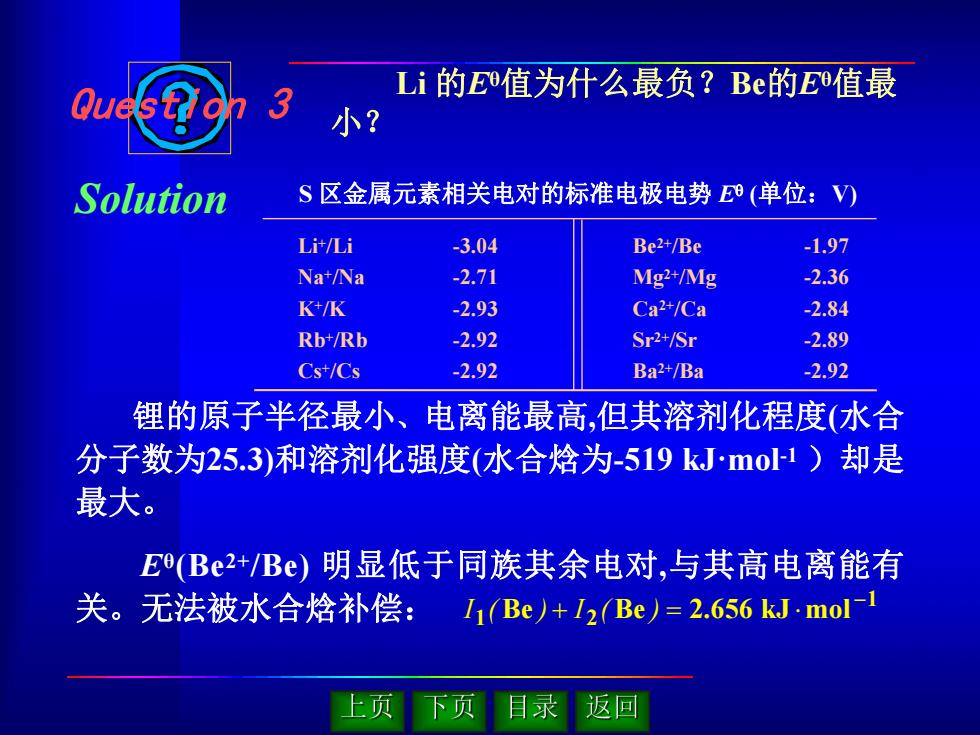
Li 的Eθ值为什么最负?Be的Eθ值最 小? S 区金属元素相关电对的标准电极电势 E (单位:V) Li+/Li Na +/Na K+/K Rb+/Rb Cs +/Cs -3.04 -2.71 -2.93 -2.92 -2.92 Be 2+/Be Mg 2+/Mg Ca 2+/Ca Sr 2+/Sr Ba 2+/Ba -1.97 -2.36 -2.84 -2.89 -2.92 Question 3 Solution 锂的原子半径最小、电离能最高,但其溶剂化程度(水合 分子数为25.3)和溶剂化强度(水合焓为-519 kJ·mol -1 )却是 最大。 Eθ(Be 2+/Be) 明显低于同族其余电对,与其高电离能有 关。无法被水合焓补偿: 1 1 Be 2 Be 2.656 kJ mol I ( ) I ( )
Li 的Eθ值为什么最负?Be的Eθ值最 小? S 区金属元素相关电对的标准电极电势 E (单位:V) Li+/Li Na +/Na K+/K Rb+/Rb Cs +/Cs -3.04 -2.71 -2.93 -2.92 -2.92 Be 2+/Be Mg 2+/Mg Ca 2+/Ca Sr 2+/Sr Ba 2+/Ba -1.97 -2.36 -2.84 -2.89 -2.92 Question 3 Solution 锂的原子半径最小、电离能最高,但其溶剂化程度(水合 分子数为25.3)和溶剂化强度(水合焓为-519 kJ·mol -1 )却是 最大。 Eθ(Be 2+/Be) 明显低于同族其余电对,与其高电离能有 关。无法被水合焓补偿: 1 1 Be 2 Be 2.656 kJ mol I ( ) I ( )
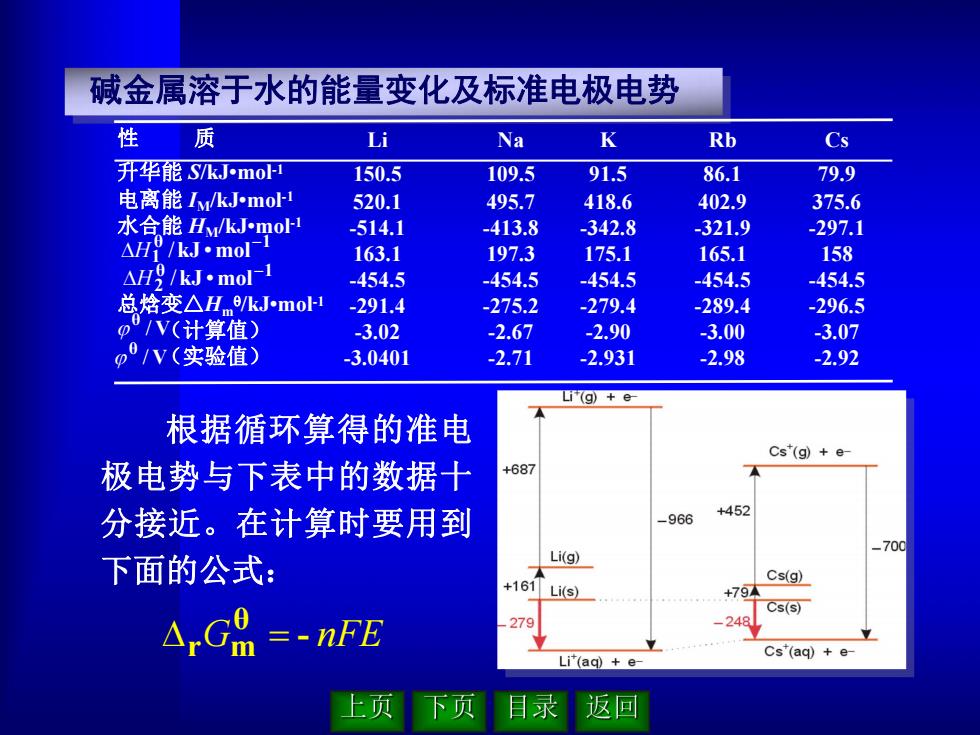
根据循环算得的准电 极电势与下表中的数据十 分接近。在计算时要用到 下面的公式: G - nFE θ r m 碱金属溶于水的能量变化及标准电极电势 Na 109.5 495.7 -413.8 197.3 -454.5 -275.2 -2.67 -2.71 性 质 升华能 S/kJ•mol -1 电离能 IM/kJ•mol -1 水合能 HM/kJ•mol -1 总焓变△Hm /kJ•mol -1 (计算值) (实验值) Li 150.5 520.1 -514.1 163.1 -454.5 -291.4 -3.02 -3.0401 K 91.5 418.6 -342.8 175.1 -454.5 -279.4 -2.90 -2.931 Rb 86.1 402.9 -321.9 165.1 -454.5 -289.4 -3.00 -2.98 Cs 79.9 375.6 -297.1 158 -454.5 -296.5 -3.07 -2.92 θ 1 1 kJ •mol H / θ 1 2 kJ •mol H / V θ / V θ /
根据循环算得的准电 极电势与下表中的数据十 分接近。在计算时要用到 下面的公式: G - nFE θ r m 碱金属溶于水的能量变化及标准电极电势 Na 109.5 495.7 -413.8 197.3 -454.5 -275.2 -2.67 -2.71 性 质 升华能 S/kJ•mol -1 电离能 IM/kJ•mol -1 水合能 HM/kJ•mol -1 总焓变△Hm /kJ•mol -1 (计算值) (实验值) Li 150.5 520.1 -514.1 163.1 -454.5 -291.4 -3.02 -3.0401 K 91.5 418.6 -342.8 175.1 -454.5 -279.4 -2.90 -2.931 Rb 86.1 402.9 -321.9 165.1 -454.5 -289.4 -3.00 -2.98 Cs 79.9 375.6 -297.1 158 -454.5 -296.5 -3.07 -2.92 θ 1 1 kJ •mol H / θ 1 2 kJ •mol H / V θ / V θ /

(3) 焰色反应 (flame reaction) 元 素 Li Na K Rb Cs Ca Sr Ba 颜 色 深红 黄 紫 红紫 蓝 橙红 深红 绿 波 长 / nm 670.8 589.2 766.5 780.0 455.5 714.9 687.8 553.5 碱金属和碱土金属的化合物在无色火焰中燃烧 时,会呈现出一定的颜色,称为焰色反应 (flame reaction)。可以用来鉴定化合物中某元素的存在,特 别是在野外
(3) 焰色反应 (flame reaction) 元 素 Li Na K Rb Cs Ca Sr Ba 颜 色 深红 黄 紫 红紫 蓝 橙红 深红 绿 波 长 / nm 670.8 589.2 766.5 780.0 455.5 714.9 687.8 553.5 碱金属和碱土金属的化合物在无色火焰中燃烧 时,会呈现出一定的颜色,称为焰色反应 (flame reaction)。可以用来鉴定化合物中某元素的存在,特 别是在野外