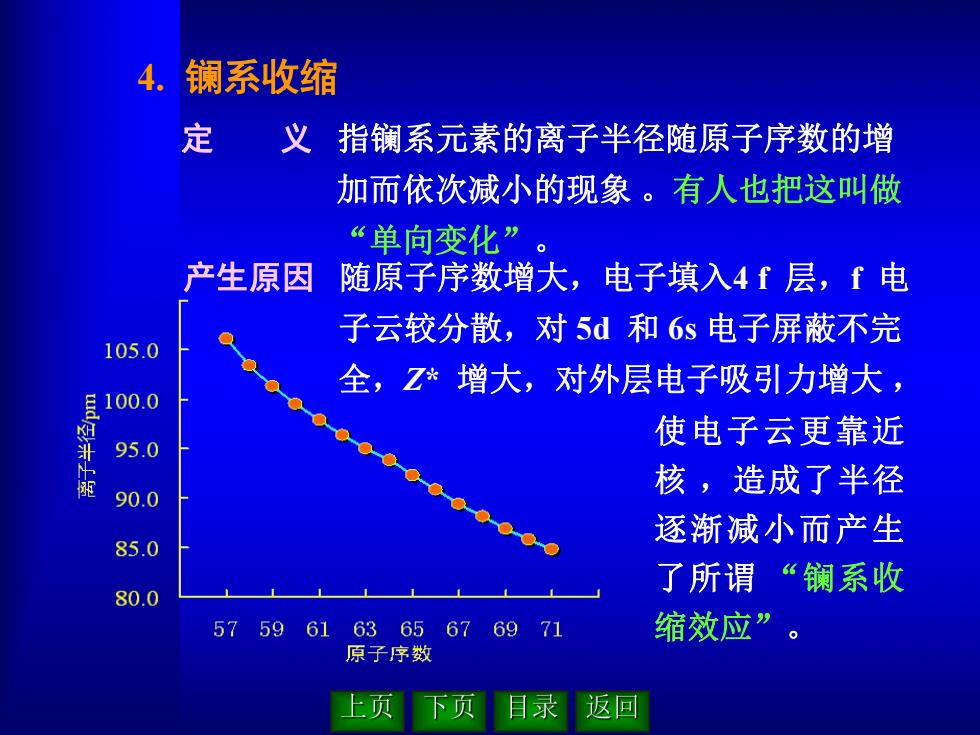
4. 镧系收缩 定 义 指镧系元素的离子半径随原子序数的增 加而依次减小的现象 。有人也把这叫做 “单向变化” 。 产生原因 随原子序数增大,电子填入4 f 层,f 电 子云较分散,对 5d 和 6s 电子屏蔽不完 全,Z* 增大,对外层电子吸引力增大 , 使电子云更靠近 核 ,造成了半径 逐渐减小而产生 了所谓 “镧系收 缩效应”
4. 镧系收缩 定 义 指镧系元素的离子半径随原子序数的增 加而依次减小的现象 。有人也把这叫做 “单向变化” 。 产生原因 随原子序数增大,电子填入4 f 层,f 电 子云较分散,对 5d 和 6s 电子屏蔽不完 全,Z* 增大,对外层电子吸引力增大 , 使电子云更靠近 核 ,造成了半径 逐渐减小而产生 了所谓 “镧系收 缩效应”

● 使 Y 的原子半径处于 Ho 和 Er 之间,其化学性质 与镧系元素非常相似,在矿物中共生,分离困难, 故在稀土元素分离中将其归于重稀土一组。 ● 收缩缓慢是指相邻两个元素而言,两两之间的减小 幅度不如其他过渡元素两两之间的减小幅度大,使 镧系元素内部性质太相似,增加了分离困难 ; ● 使镧系元素后的第三过渡系的离子半径接近于第二 过渡系同族,如 Zr 4+(80 pm) 和 Hf 4+ (81 pm), Nb5+ (70 pm) 和 Ta5+ (73 pm),Mo6+ (62 pm) 和 W6+ (65 pm), 化学性质相似,矿物中共生,分离困难;
● 使 Y 的原子半径处于 Ho 和 Er 之间,其化学性质 与镧系元素非常相似,在矿物中共生,分离困难, 故在稀土元素分离中将其归于重稀土一组。 ● 收缩缓慢是指相邻两个元素而言,两两之间的减小 幅度不如其他过渡元素两两之间的减小幅度大,使 镧系元素内部性质太相似,增加了分离困难 ; ● 使镧系元素后的第三过渡系的离子半径接近于第二 过渡系同族,如 Zr 4+(80 pm) 和 Hf 4+ (81 pm), Nb5+ (70 pm) 和 Ta5+ (73 pm),Mo6+ (62 pm) 和 W6+ (65 pm), 化学性质相似,矿物中共生,分离困难;

为什么在镧系中离子半径会出现 单向变化呢?为什么在 Gd 处出现一种 不连续性呢? 由于镧系元素三价离子的外围电子很有规律(离子 结构为 f 0 至 f 14 ),因此离子半径会出现“单向变化” 。 镧系元素三价离子半径的变化中,在 Gd 处出现了 微小的可以察觉的不连续性,原因是 Gd3+ 离子具有半 充满的 4 f 7电子结构 ,屏蔽能力略有增加,有效核电荷 略有减小,所以 Gd3+ 离子半径的减小要略微小些,这 叫 “钆断效应” 。 Question 1 Solution
为什么在镧系中离子半径会出现 单向变化呢?为什么在 Gd 处出现一种 不连续性呢? 由于镧系元素三价离子的外围电子很有规律(离子 结构为 f 0 至 f 14 ),因此离子半径会出现“单向变化” 。 镧系元素三价离子半径的变化中,在 Gd 处出现了 微小的可以察觉的不连续性,原因是 Gd3+ 离子具有半 充满的 4 f 7电子结构 ,屏蔽能力略有增加,有效核电荷 略有减小,所以 Gd3+ 离子半径的减小要略微小些,这 叫 “钆断效应” 。 Question 1 Solution
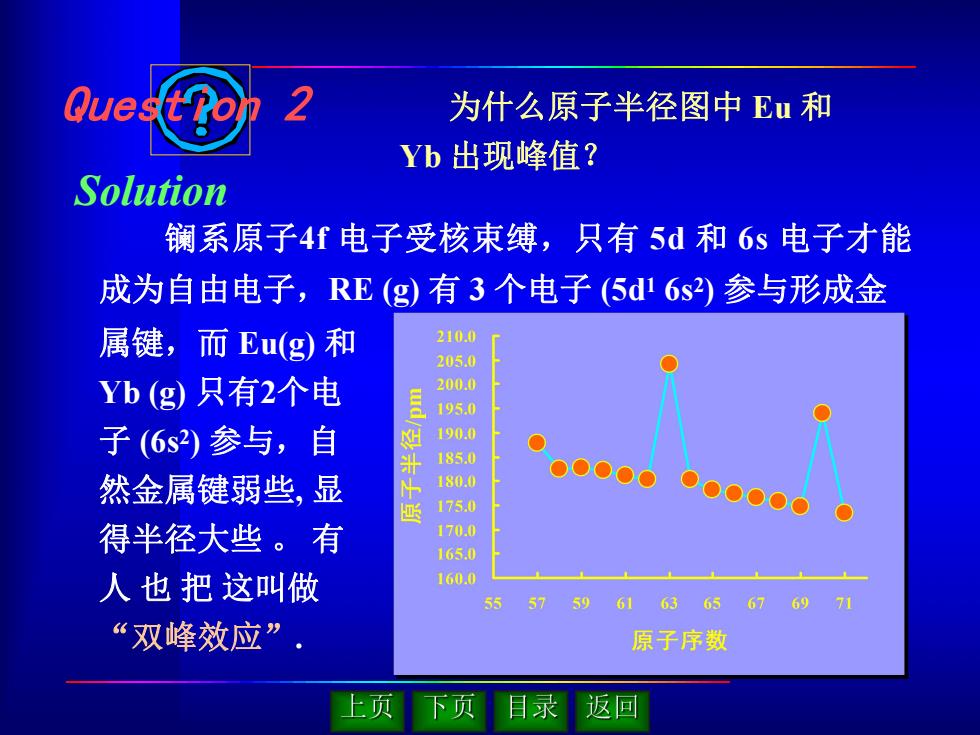
为什么原子半径图中 Eu 和 Yb 出现峰值? Question 2 Solution 镧系原子4f 电子受核束缚,只有 5d 和 6s 电子才能 成为自由电子,RE (g) 有 3 个电子 (5d1 6s 2) 参与形成金 属键,而 Eu(g) 和 Yb (g) 只有2个电 子 (6s 2) 参与,自 然金属键弱些, 显 得半径大些 。 有 人 也 把 这叫做 “双峰效应
为什么原子半径图中 Eu 和 Yb 出现峰值? Question 2 Solution 镧系原子4f 电子受核束缚,只有 5d 和 6s 电子才能 成为自由电子,RE (g) 有 3 个电子 (5d1 6s 2) 参与形成金 属键,而 Eu(g) 和 Yb (g) 只有2个电 子 (6s 2) 参与,自 然金属键弱些, 显 得半径大些 。 有 人 也 把 这叫做 “双峰效应
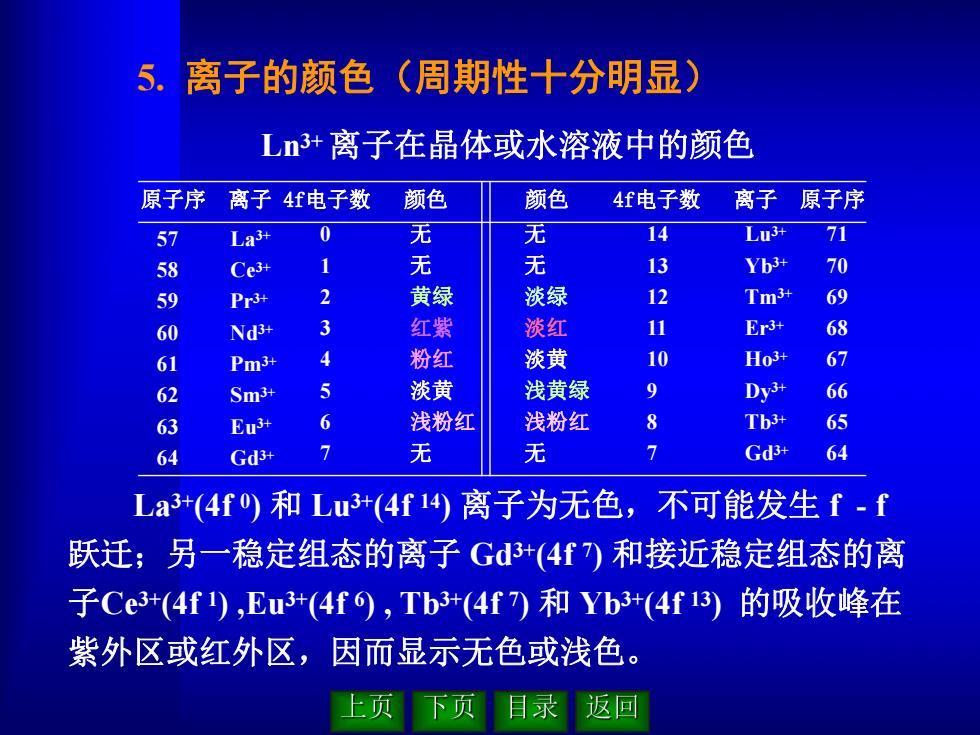
5. 离子的颜色(周期性十分明显) Ln3+离子在晶体或水溶液中的颜色 原子序 离子 4f电子数 颜色 颜色 4f电子数 离子 原子序 57 58 59 60 61 62 63 64 La 3+ Ce 3+ Pr 3+ Nd3+ Pm3+ Sm3+ Eu3+ Gd3+ 0 1 2 3 4 5 6 7 无 无 黄绿 红紫 粉红 淡黄 浅粉红 无 无 无 淡绿 淡红 淡黄 浅黄绿 浅粉红 无 14 13 12 11 10 9 8 7 Lu3+ Yb3+ Tm3+ Er 3+ Ho 3+ Dy 3+ Tb3+ Gd3+ 71 70 69 68 67 66 65 64 La 3+(4f 0) 和 Lu3+(4f 14) 离子为无色,不可能发生 f - f 跃迁;另一稳定组态的离子 Gd3+(4f 7) 和接近稳定组态的离 子Ce 3+(4f 1) ,Eu3+(4f 6) , Tb3+(4f 7) 和 Yb3+(4f 13) 的吸收峰在 紫外区或红外区,因而显示无色或浅色
5. 离子的颜色(周期性十分明显) Ln3+离子在晶体或水溶液中的颜色 原子序 离子 4f电子数 颜色 颜色 4f电子数 离子 原子序 57 58 59 60 61 62 63 64 La 3+ Ce 3+ Pr 3+ Nd3+ Pm3+ Sm3+ Eu3+ Gd3+ 0 1 2 3 4 5 6 7 无 无 黄绿 红紫 粉红 淡黄 浅粉红 无 无 无 淡绿 淡红 淡黄 浅黄绿 浅粉红 无 14 13 12 11 10 9 8 7 Lu3+ Yb3+ Tm3+ Er 3+ Ho 3+ Dy 3+ Tb3+ Gd3+ 71 70 69 68 67 66 65 64 La 3+(4f 0) 和 Lu3+(4f 14) 离子为无色,不可能发生 f - f 跃迁;另一稳定组态的离子 Gd3+(4f 7) 和接近稳定组态的离 子Ce 3+(4f 1) ,Eu3+(4f 6) , Tb3+(4f 7) 和 Yb3+(4f 13) 的吸收峰在 紫外区或红外区,因而显示无色或浅色