
§3.2浓度对反寇速车的影响 速牵方程 ©>3.2.1化学反应速率方程 3.2.2 由实验确定反应速率方程的 简单方法一初始速率法 3.2.3浓度与时间的定量关系
§3.2 浓度对反应速率的影响 —速率方程 3.2.1 化学反应速率方程 3.2.3 浓度与时间的定量关系 3.2.2 由实验确定反应速率方程的 简单方法—初始速率法

3.2.1化学反应速率方程 40℃,CC14中N20s分解反应的r:c(N205) t/s r:cN.O,)/s- t/s r:dNO)/s- 0 3.65×104 1800 3.64×104 300 3.59×104 2400 3.62×10-4 600 3.60×10-4 3000 3.69×104 无机化学电 900 3.62×104 4200 3.61×104 1200 3.61×104 5400 3.68×104 NOs的分解速率与NOs浓度的比值是 恒定的,即反应速率r与cNOs)成正比。 闲 可见:r=kdN2Os)
40℃,CCl4中N2O5分解反应的r:c( N2O5 ) t /s t /s 0 1800 300 2400 600 3000 900 4200 1200 5400 ( ) 1 5 : N O /s 2 − r c 4 3.65 10− 4 3.60 10− 4 3.62 10− 4 3.61 10− 4 3.59 10− 4 3.69 10− 4 3.62 10− 4 3.64 10− 4 3.68 10− 4 3.61 10− ( ) 1 5 : N O /s 2 − r c 3.2.1 化学反应速率方程 N2O5的分解速率与N2O5浓度的比值是 恒定的,即反应速率r与c(N2O5 )成正比。 可见: (N O ) 2 5 r = kc

对于一般的化学反应: aA+bB->yY+zZ r=kcc哈 a,B-反应级数:若a=1,A为一级反应; B=2,B为二级反应,则a+B=3,总 反应级数为3。,B必须通过实验确定其值。 霸 通常o≠a,B≠b。 k一反应速率系数:零级反应molL1sl; 学电子 级反应sl;二级反应(molL)1sl;k不 随浓度而变,但受温度的影响,通常温度升高 k增大
对于一般的化学反应: α,β—反应级数:若α=1,A为一级反应; β=2,B为二级反应,则α+β=3,总 反应级数为3。α,β必须通过实验确定其值。 通常α≠a,β≠b。 k —反应速率系数:零级反应 mol·L-1 ·s-1; 一级反应 s -1;二级反应 (mol·L -1 ) -1 ·s-1; k 不 随浓度而变,但受温度的影响,通常温度升高, k 增大。 aA +bB→ yY + zZ A B r = kc c

化学计量 速率 反应 方程 方程 级数 NO2 (g)+CO(g) <500K 2 NO(g)+CO2 (g) r=k[c(NO2)】] H2(g)+I2(g)→2HI(g) r=kdH,)c(I, 1+1 2NOg)+O,(g)-→2NO(g) r=k[c(NO)]2c(O2) 2+1 无机 2NO(g)+2H2 (g)>N2 (g)+H2O(g) r=k[c(NO)]2c(H2) 2+1 化学电 S208(aq)+3I(aq)→ r=ka(S,O )c(I) 1+1 2SO2 (aq)+I (aq) 5Br-(aq)+BrO(aq)+6H*(aq)>r=kc(Br) 教 3Br2(aq)+3H2O(aq) c(BrO)·[c(H)] +1*
化 学 计 量 方 程 速 率 方 程 反 应 级 数 2 1+1 2+1 2+1 1+1 1+1+2 (S O ) (I ) 2- - 2 8 r = k c c [ (NO)] (O ) 2 2 r = k c c 2 2 r = k[c(NO )] - 2 3 - (BrO ) [ (H )] (Br ) + = c c r kc ( ) ( ) NO(g) CO (g) NO g CO g 2 500K 2 + + ⎯ ⎯⎯→ H (g) I (g) 2HI(g) 2 + 2 → 2NO(g) O (g) 2NO (g) + 2 → 2 ( ) ( ) 2SO (aq) I (aq) S O aq 3I aq 3 2 4 2 2 8 − − − − + + → ( ) ( ) ( ) 3Br (aq) 3H O(aq) Br aq BrO aq 6H aq 2 2 3 + 5 − + − + + → 2NO(g) 2H (g) N (g) H O(g) + 2 → 2 + 2 [ (NO)] (H ) 2 2 r = k c c (H ) (I ) 2 2 r = kc c
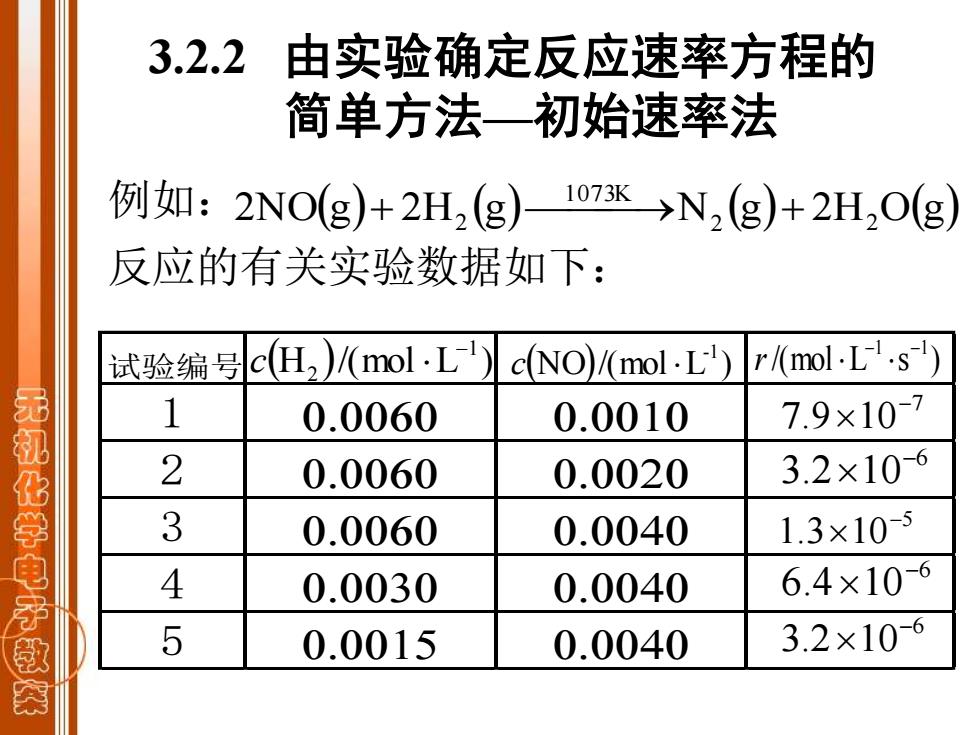
3.2.2 由实验确定反应速率方程的 简单方法一初始速率法 例如:2NOg)+2H2(g)107K→N2(g)+2H,O(g) 反应的有关实验数据如下: 试验编号c(H2)(mol·L)cNo)molL】 r/(mol.L.s) 1 0.0060 0.0010 7.9×107 无机化学电子数 2 0.0060 0.0020 3.2×106 3 0.0060 0.0040 1.3×105 4 0.0030 0.0040 6.4×10-6 5 0.0015 0.0040 3.2×10-6
例如: 反应的有关实验数据如下: 2NO(g) 2H (g) N (g) 2H O(g) 2 2 1073K + 2 ⎯⎯⎯→ + 试验编号 1 6 2 6 3 6 4 4 3 4 5 5 4 (H )/(mol L ) 1 2 − c (NO)/(mol L ) -1 c /(mol L s ) −1 −1 r 7 7.9 10− 6 3.2 10− 5 1.3 10− 6 6.4 10− 6 3.2 10− 3.2.2 由实验确定反应速率方程的 简单方法—初始速率法