
酸碱反应类型与平衡常数1、溶剂分子之间的质子转移反应一质子自递反应H,O=H +OHH,O+H,O = H,O*+OHK, =[H,O* [OH ] =[H ][OH ] = 1' 10- 14SH+SH = SH,++SK, =[SH, I[S" ]K一溶剂分子的质子自递常数山东翟工大学11HANDONGUNIVTSTOTTCHINOLOGAnalytical Chemistry
Analytical Chemistry 11 1、溶剂分子之间的质子转移反应—质子自递反应 K—溶剂分子的质子自递常数 二、酸碱反应类型与平衡常数

2、酸碱溶质与溶剂分子间的反应一酸碱的解离HAc=Ac'+HHAc +H,O= Ac +H,OK, =[Ac' IIH/HAcK =[Ac 1H,O+/[HAc]K一酸的解离常数NH,+H,O = NH +OHK一碱的解离常数K, =NHJIOHJ/NH,酸碱的强弱取决于给出质子或接受质子的能力通常用解离常数的大小衡量。K,或(K或K)K,越大,酸碱强度越强。山东翟工大学12HANDONGUNIVSRTOTICHNOLOGAnalytical Chemistry
Analytical Chemistry 12 2、酸碱溶质与溶剂分子间的反应—酸碱的解离 Ka—酸的解离常数 Kb—碱的解离常数 酸碱的强弱取决于给出质子或接受质子的能力, 通常用解离常数(Ka 或 Kb)的大小衡量。 Ka 或 Kb越大,酸碱强度越强

①共轭酸碱对的酸碱强度关系[H+][AcHAc+H,U Ac +H,OKO[HAc][HAc][OH-Ac +H,OU HAc+OHK,[Ac ][H ][A] [HAc][OH']=1.0°10-14K. xK.[H+]XOH] =K[Ac][HAC]pK.+pK, =pK=14.00种酸的酸性越强,其共轭碱的碱性越弱山东翟工大学13HANDONGUNIVTSTOTICINOLOGAnalytical Chemistry
Analytical Chemistry 13 Ø共轭酸碱对的酸碱强度关系 一种酸的酸性越强,其共轭碱的碱性越弱
酸的强度,例如:HAc>NH+>HS碱的强度,例如:S2->NH,> Ac问题:H,PO.水溶液中的共轭酸碱对及其酸碱强度关系如何?Ka2KalKa3PO,3-2HPO4H,POH,PO4Kb3Kp2KblpKal + pKb3= 14.00KVKbipKa2 + pKb2 = 14.00Ka(n-i+l)pKa3 + pKb1 = 14.00多元酸H,A,一般K >Ka2 >Ka3>Kbl > Kb2 > Kb3 >山东翟工大学14HANDONGUNIVTSTOTICINOLOGAnalytical Chemistry
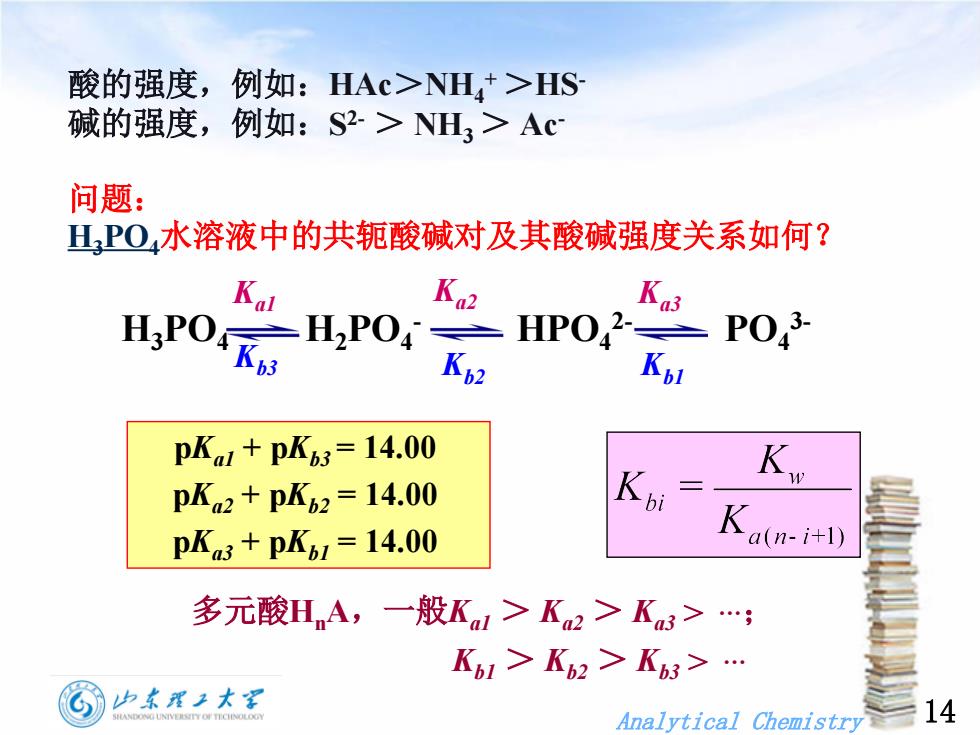
Analytical Chemistry 14 酸的强度,例如:HAc>NH4 + >HS- 碱的强度,例如:S 2- > NH3 > Ac- 问题: H3PO4水溶液中的共轭酸碱对及其酸碱强度关系如何? H3PO4 H2PO4 - HPO4 2- PO4 3- Kb2 Kb1 Kb3 Ka1 Ka2 Ka3 pKa1 + pKb3 = 14.00 pKa2 + pKb2 = 14.00 pKa3 + pKb1 = 14.00 多元酸HnA,一般Ka1 > Ka2 > Ka3 > .; Kb1 > Kb2 > Kb3 >

3、酸碱中和反应(滴定反应)一酸碱解离反应的逆反应K一滴定反应常数(1)强酸强碱中和H+OH' =H,O反应十分完全。K, =1/[H+I[OH J=1/ K(2)强碱(酸)和弱酸(碱)中和OH+HAc=H,O+AcNh, +h+ = nh+K, =[Ac ]/[OH J[HAc]= K,/ K,K, =[NH ]/[NH,I[H+]= K, / K,酸(碱)越弱,K,(K)越小,K越小,反应越不完全山东翟工大学15HANDONGUNIVSTOTICINOAnalytical Chemistry
Analytical Chemistry 15 3、酸碱中和反应(滴定反应)—酸碱解离反应的逆反应 Kt—滴定反应常数 (1)强酸强碱中和 (2)强碱(酸)和弱酸(碱)中和 反应十分完全。 酸(碱)越弱,Ka(Kb)越小,Kt越小,反应越不完全