
铁盐和亚铁盐 素养目标 教学重点、难点 1.依据化合价理论,结合实验探 究,掌握Fe2+、Fe3+相互转化的途 1.Fe3+、Fe2+的检验 径,强化变化观念。 2.通过实验探究学会Fe2+、Fe3+ 2. 探究Fe2+与Fe3+的 的检验方法,培养证据推理意识, 相互转化的条件 提升实验探究能力与创新意识
素养目标 1. Fe3+、Fe2+的检验 2. 探究Fe2+与Fe3+的 相互转化的条件 教学重点、难点 1.依据化合价理论,结合实验探 究,掌握Fe2+、Fe3+相互转化的途 径,强化变化观念。 2.通过实验探究学会Fe2+、Fe3+ 的检验方法,培养证据推理意识, 提升实验探究能力与创新意识
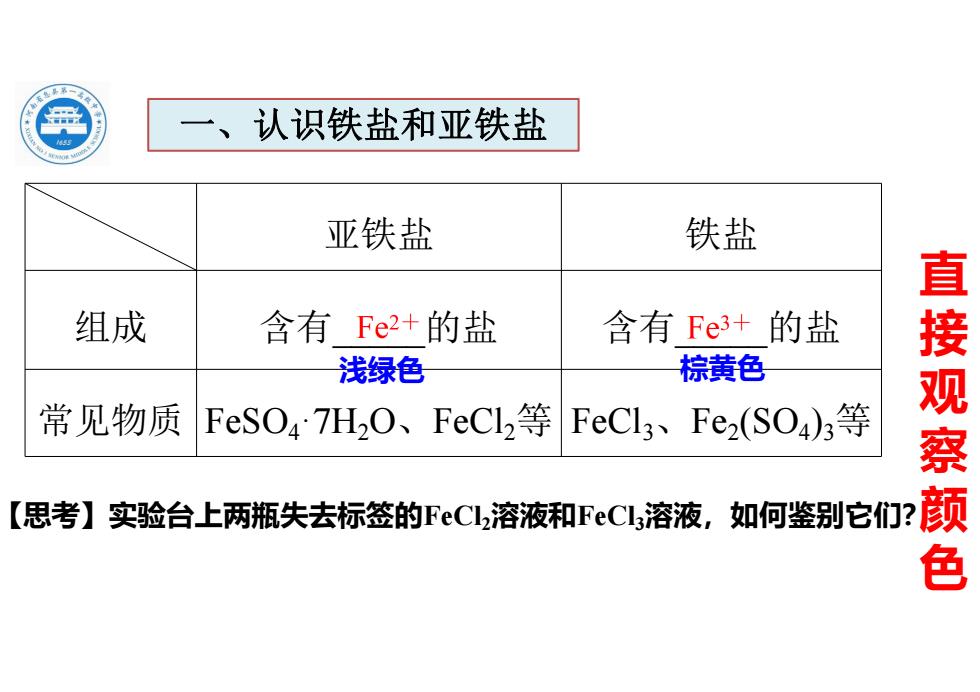
一、认识铁盐和亚铁盐 亚铁盐 铁盐 组成 含有Fe2+的盐 含有Fe3+的盐 浅绿色 棕黄色 常见物质 FeS04'7HO、FeCl2等 FeCl3、Fe2(SO4)3等 【思考】实验台上两瓶失去标签的FeCL2溶液和FeCla3溶液,如何鉴别它们? 直接观察颜色
亚铁盐 铁盐 组成 含有 _ 的盐 含有 _ 的盐 常见物质 FeSO 4ꞏ7H 2 O 、FeCl 2 等 FeCl 3 、Fe 2(SO 4 ) 3 等 一、认识铁盐和亚铁盐 【思考】实验台上两瓶失去标签的FeCl 2溶液和FeCl 3溶液,如何鉴别它们? 直 接 观 察 颜 色 浅绿色 棕黄色

二、Fe3+和Fe2+的检验 请同学们再结合上节课学过的铁的氢氧化物知识,自主阅读学 习课本60一61页内容,分组讨论,总结出Fe3+、e2+的检验方法。 方法 Fe3+ Fe2+ ①观察颜色 黄色 浅绿色 白色沉淀迅速变灰 立即产生红褐色沉淀 ②加NaOH溶液 绿色最后呈红褐色 Fe3++30H=Fe(OH)3 Fe2++20H Fe(OH)2
请同学们再结合上节课学过的铁的氢氧化物知识,自主阅读学 习课本60—61页内容,分组讨论,总结出Fe3+、Fe2+的检验方法。 二、 Fe3+和Fe2+的检验 方法 Fe3+ Fe2+ ① ② 黄色 浅绿色 白色沉淀迅速变灰 立即产生红褐色沉淀 绿色最后呈红褐色 Fe3+ + 3OH- = Fe(OH)3↓ Fe2+ + 2OH- = Fe(OH)2↓ 观察颜色 加NaOH溶液

二、Fe3+和Fe2+的检验 【实验3-10】在两支试管里分别加入5mL的FeCl3溶液和 5 mLFeCl,溶液,各滴入几滴KSCN溶液。观察并记录现象 ③滴入KSCN溶液 硫氰化钾 FeCl3溶液 变成红色溶液 FeCl2溶液 溶液颜色没有明显变化 →溶液呈红色→含有Fe3+ 未知 KSCN溶液 溶液 溶液不变红→不含有Fe3+
③滴入KSCN溶液 硫氰化钾 FeCl3溶液 FeCl2溶液 【实验3-10】在两支试管里分别加入5mL的FeCl3溶液和 5mLFeCl2溶液,各滴 入几滴KSCN溶液。观察并记录现象。 二、 Fe3+和Fe2+的检验 变成红色溶液 溶液颜色没有明显变化 不

【实验探究一】Fe2+→Fe3+ 【提出问题】向久置FeCl2溶液中滴入 几滴KSCN溶液,为什么会变红色? 原理分析(从化合价角度) 02氧化剂 Fe2+ Fe3+ 还原性
三、 Fe3+和Fe 【实验探究一】2+Fe的相互转化 2+→Fe3+ Fe2+ 氧化剂 Fe3+ 原理分析(从化合价角度) 还原性 O2 【提出问题】向久置 FeCl2溶液中滴入 几滴KSCN溶液,为什么会变红色?